初中 化学
如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是 ( )

| 选项 | A | B | C | D |
| 目的 | 比较呼出气体和空气中CO2的含量 | 配制质量分数10%的NaCl溶液 | 验证质量守恒定律 | 验证与氧气接触是燃烧的条件之一 |
| 实验 | | | | |

-
(1) 实验过程中,红磷燃烧的现象是,燃烧匙里为什么要盛放过量的红磷?;
-
(2) 这个实验除了可以得出氧气约占空气体积的
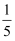 的结论外,还可推出氮气 (填“易”或“难”)溶于水和其化学性质(填“活泼“或“不活泼”)的结论。
的结论外,还可推出氮气 (填“易”或“难”)溶于水和其化学性质(填“活泼“或“不活泼”)的结论。
-
(3) 在此实验过程中能否用碳代替红磷?;原因是;
-
(4) 如果反应后进入集气瓶中的水的体积不到总体积的
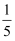 ,可能的原因是(写出一条)。
,可能的原因是(写出一条)。
 B .
B .  D .
D . 

-
(1) 汉防己碱属于(填“无机物”或“有机物”);
-
(2) 汉防己碱由种元素组成,1244gC38H42N2O6中含氮g;
-
(3) 汉防己碱中碳元素与氧元素的质量比是(化成最简比)。
化学兴趣小组用如图装置探究炼铁的原理.
(1)加热Fe2O3之前要先通一会儿CO,目的是 .
(2)方框中要连接其它装置,目的是 .
(3)玻璃管A中发生反应的化学方程式为 ,现象是
(4)装置B中发生反应的化学方程式为 .

(查阅资料)①NaOH在空气中变质不会生成NaHCO3;
②CO2不溶解于饱和NaHCO3溶液中,也不与NaHCO3反应;
③Fe(OH)3呈红褐色,难溶于水;BaCl2溶液呈中性。
-
(1) (提出猜想)猜想一:是NaOH
猜想二:是Na2CO3
猜想三:
-
(2) (实验探究)小军进行了下列实验探究
实验操作
实验现象
实验结论
①取少量白色固体于试管中,加水溶解,再加入足量BaCl2溶液
猜想二正确
②过滤,在滤液中加入FeCl3溶液
无红褐色沉淀生成
-
(3) (问题分析)实验操作①中加入足量BaCl2溶液的作用是,实验操作②还有其他实验方案吗?如有,请写出一种实验方案(必须指明试剂和现象)。
-
(4) 为了提高实验结论的准确性,小军又设计了如图所示的实验对该白色固体的性质进行进一步探究:

(实验现象)A中有大量气泡产生,C中实验现象是
-
(5) (实验结论)白色固体是Na2CO3
(分析与反思)小军在与老师进行交流后得知,自己所设计的实验存在一定的缺陷,他对自己实验中存在的问题进行了反思:装置B中也能产生CO2。写出装置B中产生CO2的化学反应方程式。改进措施:。
-
(1) 【实验方案】
实验步骤
实验现象
实验结论
小东
用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH
pH试纸变色
pH7(填“>”或“<”)
该溶液是氢氧化钠溶液
小南
取适量溶液于试管中,加入经打磨过的铝条
有气泡产生
该溶液是稀硫酸
-
(2) 【提出问题】为什么我们取相同溶液而实验结论却不同呢?
【解决问题】小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是 , 于是一致认为该溶液是氢氧化钠溶液,为什么小南加入铝条会有气泡产生呢?通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
-
(3)
【拓展延伸】利用老师要求鉴别的那两种溶液,测定镁铝铜合金中各成分的含量.实验设计如下:

【回答问题】
(1)写出操作Ⅰ中玻璃棒的作用: .
(2)a溶液是 , 选择该溶液的理由是 .
(3)金属铜的质量为 g,固体A含有的物质是 , 溶液A中所含溶质是 .
-
(1) 某学生用托盘天平称量2.5g食盐,在称量中发现指针偏向分度盘左边,接下来应采取的措施是________(填写序号)A . 增加砝码 B . 减少砝码 C . 添加食盐 D . 减少食盐
-
(2) 该同学接下来想量取18mL液体,应选用___________。A . 10mL量筒 B . 20mL量筒 C . 50mL量筒 D . 胶头滴管
-
(3) 该同学在读数时视线与量筒内凹液面最低处保持水平,然后倾倒一部分液体后,俯视凹液面最低处读数,读数为12mL。则该同学倾倒液体体积6mL(选填“大于”或“小于”或“等于”)。
 B . 软塑料瓶变瘪
B . 软塑料瓶变瘪 C . 石蕊溶液变红
C . 石蕊溶液变红 D . 气球上浮
D . 气球上浮
-
(1) “玉不琢不成器”中发生的变化是(填“物理变化”或“化学变化”)。
-
(2) “钻石恒久远,一颗永流传”说明钻石具有的性质是。
-
(3) “春蚕到死丝方尽,蜡炬成灰泪始干”。下列关于“泪”的说法正确的是________。A . “泪”是指石蜡燃烧生成的水 B . “泪”说明石蜡熔点低,受热易熔化 C . “泪”说明化学变化的同时伴随有物理变化
-
(1) "菜篮子"中包含多种蔬菜和水果,它们富含维生素C,人体缺乏维生素C,会引起
-
(2) 食盐几乎是每道菜不可或缺的调味品,加碘食盐中的"碘"指的是碘(填"单质""原子"或"元素")。
-
(3) 为提高粮食产量,农业生产中要合理使用化肥,(填"氮肥"或"钾肥")能增强抗病虫害和抗倒伏能力;
-
(4) 下列有关饮食安全的说法正确的是
a.甲醛有防腐作用,可以用来浸泡食材
b.青少年多喝牛奶能补充钙元素
c.脂肪、蛋白质是人体必需的营养素,吃得越多越好
d.恢复生猪生产,为提高产量和瘦肉率,在饲料中添加瘦肉精

欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液。下列说法正确的是( )
A.过滤时,用玻璃棒在漏斗中搅拌加快过滤速度
B.蒸发滤液时,待蒸发皿中滤液蒸干时才停止加热
C.用精盐配制上述溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
D.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、试管、玻璃棒等
第 24 届冬季奥运会将于 2022 年在北京举办,为落实 “绿色冬奥”的理念,冬奥会使用的汽车燃料从环保的角度考虑,最理想的是
A . 氢气 B . 天然气 C . 酒精 D . 汽油
某物质在氧气中充分燃烧生成二氧化碳和水。
(1)设计实验证明二氧化碳和水的存在。
(2)运用质量守恒定律解释:该物质中一定有碳、氢两种元素。
下列对质量守恒定律的理解错误的是( )
A. 质量守恒定律只适用于化学反应,不适用于物理变化
B.质量守恒定律研究的内容仅是指“质量”,不能推广到其它物理量
C.催化剂可以改变其它物质的化学反应速率,有催化剂参加的反应也遵守质量守恒
定律
D.蜡烛燃烧后质量减轻,不符合质量守恒定律
- .下列各项加点字读音全都正确的一项是 A.贿赂(lù) 瑰(guī)怪 荫(yīn)庇 哺(
- 对下列现象或事实的解释中,不正确的是选项 事 实 解 释A 二氧化碳吸入过多,会使人窒息死亡 二氧化碳有
- 依次填入下面的一段文字横线处的语句,衔接最恰当的一组是 真正精致的石头虽则应该暗示雄伟或出尘超俗的感觉,然而线条
- 下列不属于“长大”的内涵是 ( )A.懂得自我约束和自我控制,老师家长在与不在时都一个样B.懂得自立自强,尊重理解他
- ---- How is theman injured in the accident? ---- The doct
- 26.— How is the campus cleaning going?
- (北京卷)31.指出,有监督比没有监督好,一部分人出主意不如大家出主意。从一个角度看问题,民主党派可以从另一个角度看问题
- 客流强度用来反映城市间联系的密切程度。下图为安徽省内各市每日发往合肥的客流强度及客流比例图。读图,完成1-2题。1.客流
- 如图是模拟膈肌变化与呼吸之间关系的装置图,下列表述中正确的是() A. 甲图表示吸气,膈肌收缩 B. 乙图表示吸气
- 下列词语中加点的字,读音没有错误的一组是( ) A.嗔(chēn)怪 缜(zhěn)密 殉(xùn)难 徇(xú
- 下列字形没有错别字的一项是 ( ) A.自力更生 寅吃卯粮 画地为牢 B.各行其事 适得其反 徇私舞弊C.淋漓尽至 叠床
- 如图,一条公路的转弯处是一段圆弧(图中的),点O是这段弧的圆心,C是上一点,OC⊥AB,垂足为D,AB=300m,CD=
- 已知椭圆与双曲线有相同的焦点,若是的等比中项,是与的等差中项,则椭圆的离心率是 A. B.
- 肺动脉中血液成分是( ) A.含氧多,含养料少 B.含氧多,含养料也多 C.含氧少,含养料多
- 在元素周期表中锡元素的某些信息如图右图所示,下列有关锡的说法正确的是 A.属于非金属元素 B.原
- Lastweek, only two people came to look at the house, _______
- 生活在高原上的人们,血液中的红细胞数量较多,出现此生理现象的主要原因是下列哪种生态因素造成的A.空气B.水分C.光照D.
- 右图的矩形,长为5,宽为2,在矩形内随机地撒300颗黄豆,数得落在阴影部分的黄豆数为138颗,则我们可以估计出阴影部分的
- 质量为9.7g 的Cu、Zn合金与足量的稀HNO3反应,还原产物只有NO气体,其体积在标准状况下为2.24L,将溶液稀释
- 用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是A、漂白粉被氧化了







