高考化学试题
A. 原子半径:X > Y > Z > W
B. X与Y元素的最高价氧化物的水化物一定能发生反应
C. 工业上常用电解Y和Z形成的化合物来制备Y单质
D. W与X形成的化合物中只含有离子键

已知:ZnS 可与稀硫酸反应;CuS 不溶于稀硫酸,也不与其发生反应。 请回答下列问题:
(1)可用图装置进行第一次浸出,烧杯中盛放的是______溶液。

(2)滤液Ⅰ中的 Fe2+最好用______来检验。
a.氯水 b.双氧水 c.KSCN 溶液 d.K3[Fe(CN)6]溶液
(3)物质 A 是含有 X 元素的氧化物(XO),则 X 是______(填元素符号),由滤液Ⅱ、Ⅳ滤液获得 ZnSO4•7H2O 的操作是______________。
(4)第二次浸出时的化学方程式为_______________。
(5)加 A 调节溶液的 pH 约为______时,可以完全除去其中的杂质离子。
(当溶液中离子浓度小于等于 10-5mol/L 时视为沉淀完全;实验条件下部分物质的溶度积常数为:Ksp[Fe(OH)3]=10-38,Ksp[Fe(OH)2]=10-17,Ksp[Zn(OH)2]=10-17,Ksp[Cu(OH)2]=10-20)
(6)实验最后获得了 5.74gZnSO4•7H2O 晶体(假设实验中没有损耗),但不能由此确定原催化剂中锌元素的质量分数,原因是_________________。
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | - | - |

请回答下列问题:
(1)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl制取无水FeCl2并测定FeCl3的转化率。按上图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯。打开K1、K2,关闭K3,通一段时间H2后关闭K2,控制三颈烧瓶内反应温度在128-139℃,反应一段时间。反应完成后打开K2再通氢气一段时间。
①仪器a的名称是______,装置B中盛装的试剂是______。
②反应后再通入H2的目的是______。
③冷却实验装置,将三颈烧瓶内物质倒出,经过滤、用苯洗涤、干燥后,得到粗产品,回收滤液中C6H5Cl的操作方法是______。
④反应后将锥形瓶中溶液配成250mL溶液,取25.00mL所配溶液,用0.4mol•L-1NaOH溶液滴定,消耗NaOH溶液23.60mL,则氯化铁的转化率为______。
(2)打开K1、K3,关闭K2,通氢气与氯化铁反应制取无水FeCl2。
①写出反应的化学方程式______。
②实验制得FeCl2后并防止氧化的操作是______。
③请指出该制备方法的缺点______。
(1)对于该反应,用各物质的反应速率与时间的关系曲线表示如下,示意图中的___________(填序号)正确。

(2)若该密闭容器绝热,实验测得B的转化率随温度变化如右图所示。由图可知,Q_________0(填“大于”或“小于),c点v正__________v逆(填“大于”、“小于”或“等于”)。

(3)在T℃时,反应进行到不同时间测得各物质的物质的量如表:

①T℃时,该反应的平衡常数K=___________。
②30min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是___________(填字母编号)。
a.通入一定量的B b.加入一定量的固体A c.适当缩小容器的体积 d.升高反应体系温度
③同时加入0.2mol B、0.1molD、0.1mol E后,其他反应条件不变,该反应平衡________移动。(填“向右”、“不”、“向左”)
④维持容器的体积和温度T℃不变,若向该容器中加入1.60molB、0.20molD、0.20molE和0.4molA,达到平衡后,混合气体中B的物质的量分数是___________。

A. 水电离出的H+浓度:a<b<c<d
B. 氢氟酸的电离平衡常数:Ka=
C. V=20
D. b点溶液中:c(F-)>c(HF)
A. 向
B. 向
C. 向
D. 向
A. 硫酸钠 B. 氯化铝 C. 酒精 D. 一水合氨
合金材料的制造与使用在我国已有数千年历史,下列文物不是由合金制作的是
A.越王勾践剑 B.司母戊鼎 C.秦兵马俑 D.马踏飞燕
A.X、Y生成H2的物质的量之比一定为
B.X、Y消耗酸的物质的量之比一定为
C.产物中X、Y化合价之比一定为
D.由
元素代号 | I1 | I2 | I3 | I4 | I5 |
Q | 800.6 | 2427.1 | 3659.7 | 25025.8 | 32826.7 |
R | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
S | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
T | 1402.3 | 2856 | 4578.1 | 7475.0 | 9444.9 |
U | 2080.7 | 3952.3 | 6122 | 9371 | 12177 |
(1)在这五种元素中,最可能处于同一族的两种元素是_________(填元素符号),S元素最可能是_____区元素
(2)基态Q元素原子的价电子排布式是____________。Q和T同周期。化合物QT中T元素的化合价为_______;第一电离能介于Q、T之间的同周期元素有______种。
(3)化合物RT3中化学键类型为_______,RT3的阴离子的几何构型为________。
(4)下列元素中,化学性质和物理性质最像U元素的是_____________
A.硼 B.铍 C.锂 D.氦 E.碳
(5)R的某种氧化物X晶胞结构如图所示,晶胞参数a=0.566 nm,X的化学式为_____;列式并计算晶体X的密度(g·cm-3)_____。
已知: 

和
发生反应,
时达到平衡状态 I ,在
时改变某一条件,
时重新达到平衡状态 Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是

A . 容器内压强不变,表明反应达到平衡
B . 时改变的条件:向容器中加入 C
C . 平衡时 A 的体积分数 

D . 平衡常数 K : 
已知:

I、核磁共振氢谱显示E分子中有两组峰,且峰面积比为2:1
Ⅱ、
Ⅲ、

回答下列问题:
(1)丙烯的结构简式为_______________;E的分子式为_____________________;
(2)B分子中官能团的名称为__________________;G的名称为_______________________。
(3)由甲苯生成F的反应类型为_________________。
(4)写出C→D的化学方程式________________________________________________。
(5)满足下列条件的G的同分异构体有_________种。
①苯环上有三个取代基。②遇
③能和
(6)写出1,3-丁二烯(
 的合成路线________________(无机试剂任选)。
的合成路线________________(无机试剂任选)。
Ⅰ.制备O2
该小组同学设计了如下气体发生装置(夹持装置省略)

(1)甲装置中主要仪器的名称为___________。
(2)乙装置中,用粘合剂将MnO2制成团,放在多孔塑料片上,连接好装置,气密性良好后打开活塞K1,经长颈漏斗向试管中缓慢加入3% H2O2溶液至___________。欲使反应停止,关闭活塞K1即可,此时装置中的现象是___________。
(3)丙装置可用于制备较多O2,催化剂铂丝可上下移动。制备过程中如果体系内压强过大,安全管中的现象是___________,此时可以将铂丝抽离H2O2溶液,还可以采取的安全措施是___________。
(4)丙装置的特点是___________(填序号)。
a.可以控制制备反应的开始和结束
b.可通过调节催化剂与液体接触的面积来控制反应的速率
c.与乙装置相比,产物中的O2含量高、杂质种类少
Ⅱ.氧化C2H5OH
该小组同学设计的氧化C2H5OH的装置如图(夹持装置省略)

(5)在图中方框内补全干燥装置和干燥剂。___________
Ⅲ.检验产物
(6)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
实验①~③中的结论不合理的是___________(填序号),原因是___________。

A. 单质S不溶于水,微溶于酒精,易溶于二硫化碳
B. 含氧酸的酸性:Cl>S>P
C. 沸点:H2O<H2S<PH3
D. 由H和S形成共价键的过程:
在给定条件下,下列选项所示的物质转化均能实现的是
A.S![]() SO2
SO2![]() CaSO4
CaSO4
B.Si![]() SiO2
SiO2![]() SiCl4
SiCl4
C.Fe![]() Fe2O3
Fe2O3![]() Fe(OH)3
Fe(OH)3
D.Na![]() NaOH(aq)
NaOH(aq) ![]() NaHCO3(aq)
NaHCO3(aq)
对于下列实验,不能正确描述其反应的离子方程式是
A . 向氢氧化钡溶液中加入盐酸: H + +OH - =H 2 O
B . 向硝酸银溶液中滴加少量碘化钾溶液: Ag + +I - =AgI↓
C . 向烧碱溶液中加入一小段铝片: ![]()
D . 向次氯酸钙溶液中通入少量二氧化碳气体: ClO - +CO 2 +H 2 O=HClO+HCO 
部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是

A . 

B . 既可被氧化,也可被还原
C . 可将 

D . 可存在 的循环转化关系
微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是

A. 负极反应为 ![]()
B. 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C. 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D. 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
(1)A、C、D、F形成的简单离子半径由大到小的顺序是_______(用元素符号填写)。
(2)B、C、E、F、G形成的气态氢化物数目最多的元素是________(填元素符号),所形成的气态氢化物中最不稳定的是__________(填化学式)。
(3)B、E、F、G最高氧化物对应的水化物酸性由强到弱的顺序是________(用化学式填写)。
(4)由A、C、D形成的化合物所含的化学键类型有_______________。
(5)化合物M和N都由A、C、D、F四种元素组成,它们在溶液中相互反应的离子方程式是____________________________;G单质的水溶液中通入F的氧化物,其反应的化学方程式为______________________________________。

已知:H3AsO3为弱酸,热稳定性差。
(1)写出一条“碱浸”时提高浸取率的方法____;“碱浸”中H3AsO3转化成Na3AsO3的离子方程式为____。
(2)“氧化”时常在向混合液中通入O2时对体系加压,目的是____。
(3)“沉砷”过程中有如下反应:
①
②
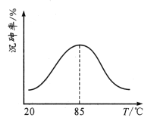
沉砷率与温度关系如图。沉砷最佳温度为____,高于85℃时,沉砷率下降的原因是____。
(4)“还原”过程中获得H3 AsO3的化学反应方程式为____;“操作A”为:____、过滤;滤液Ⅱ的主要成分是____。
(5)若每步均完全反应,“氧化’’和“还原”时消耗相同条件下O2和SO2体积分别为xL、yL,则废水中n(H3AsO3):n(H3AsO4)=____(写出含x、y的计算式)。
- 将NO+Zn+OH-+H2ONH3+Zn(OH)配平后,离子方程式中H2O的系数是 A.2
- 如图,AB∥DE,AC∥DF,AC=DF,下列条件中不能判断△ABC≌△DEF的是() A. AB=DE B. ∠B=∠
- 阅读下面的材料,按要求作文。 春天到了,家园前的草坪露出了红红绿绿的生机。一位新搬来的中年人回家不忍心践踏那片草坪,便绕
- Qingdao is _______ most beautiful coastal city and I think I
- (16分) 阅读下列材料: 材料一:魏源在《海国图志•序》中指出:“不善师外夷者,外夷制之。”夷之长技三:一战舰,二火器
- 我国领土绝大部分位于( ) A.热带 B.北温带 C.南温带 D.北寒带
- 已知一个圆锥的底面半径为3cm,母线长为10cm,则这个圆锥的侧面积为( ) A.30πcm2
- 关于作用力与反作用力,下列说法错误的是( ) A.作用力和反作用力可以是接触力,也可以是非接触力
- 根据下列图示,回答相关问题.(1)A、B、C、D四种粒子中属于同种元素的是(填字母,下同),与B的化学性质相似的是 .
- 世界上使用人数最多的语言是:A.汉语 B.英语 C.阿拉伯语 D.西班牙语
- 现有甲、乙两个烟草品种(2n=48),其基因型分别为aaBB和AAbb,这两对基因位于非同源染色体上,且在光照强度大于8
- 已知正四棱柱ABCD—A1B1C1D1的底面边长为2,侧棱长为.(1)求二面角B1—AC—B的大小;(2)求点B到平面A
- 下列比例尺中,最大的是( ) A. 图上1厘米代表实地距离20千米 B. 一千万分之
- 已知氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列有关叙述中不正确的是() ①NH4H是离子
- 如图,三棱锥S-ABC中,SA=AB=AC=2,,M、N分别为SB、SC上的点, 则△AMN周长最小值为 .
- 平面α∥平面β,aα,bβ,且a、b为异面直线,若α和β的距离为1,则a、b的距离为___________.
- 下图中A为一种混合气体,经分析只含两种元素,根据图中转化关系回答问题:(1)写出下列标号物质的化学式:B
- 为了改进银行的服务质量,随机抽查了30名顾客在窗口办理业务所用的时间(单位:分钟).下图是这次调查得到的统计图.请你根据
- 用惰性电极电解1L 4mol/ CuSO4溶液时,在电路上通过0.5mol电子后,发现电极接反了,纠正后又通过1mol电
- 观察身边的物理现象——下列估测最接近实际的是:A、电吹风正常工作电流约0.5安; B、29吋电视机正常工作电流约



