高三化学试题
甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如图所示转化关系(反应条件及部分产物已略去)。下列有关物质的推断不正确的是( )
![]()
| 选项 | 假设 | 结论 |
| A | 甲为Al(OH)3 | 丁可能是盐酸 |
| B | 甲为Na2CO3溶液 | 戊可能是CO2 |
| C | 甲为Fe | 丁可能是盐酸 |
| D | 甲为N2 | 戊可能是O2 |
实验室制取氧气的试管壁上会沾有MnO2,最好用下列哪种试剂除去
A、热的浓盐酸 B、稀盐酸 C、水 D、NaOH溶液
今有室温下四种溶液,有关叙述正确的是
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH ①=②>③=④
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4, 则Va ∶Vb= 11∶9
下列各组物质,前者属于电解质,后者属于非电解质的是( )
A.NaCl晶体、BaSO4 B.铝、二氧化硫
C.液态的醋酸、酒精 D.熔融的KNO3、硫酸溶液
食品卫生与身体健康密切相关,下列做法会导致食品对人体有害的是
①在沥青公路上翻晒粮食 ②香肠中加过量亚硝酸钠以保持肉类新鲜
③用生活用煤直接烧烤鸡、鸭 ④用“瘦肉精”(一种含激素的饲料) 喂饲生猪
⑤用小苏打做发酵粉做面包 ⑥用福尔马林保鲜鱼肉等食品
A.①②③④⑥ B.①②③④⑤⑥ C. ①②③④⑤ D.①②③④
下列叙述不正确的是
| A | B | C | D | ||
|
|
|
|
| ||
| 放电 N2 + O2 === 2NO | 玛瑙主要成分SiO2 | 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 | 漂白粉主要成分 Ca(ClO)2和CaCl2 |
钻钼系催化剂主要用于石油炼制等工艺,从废钴钼催化剂(主要含有![]() 、CoS和
、CoS和![]() )中回收钴和钼的工艺流程如图:
)中回收钴和钼的工艺流程如图:

已知:浸取液中的金属离子主要为![]() 、
、![]() 、
、![]() 。
。
(1)钼酸铵![]() 中
中![]() 的化合价为________,
的化合价为________,![]() 在空气中高温焙烧产生两种氧化物:
在空气中高温焙烧产生两种氧化物:![]() 和________(填化学式)。
和________(填化学式)。
(2)为了加快酸浸速率,可采取的措施为________(任写一条)。
(3)若选择两种不同萃取剂按一定比例(协萃比)协同萃取![]() 和
和![]() ,萃取情况如图所示,当协萃比
,萃取情况如图所示,当协萃比![]() ________,更有利于
________,更有利于![]() 的萃取。
的萃取。

(4)操作Ⅰ的名称为________。
(5)向有机相1中滴加氨水,发生的离子方程式为________。
(6)![]() 萃取的反应原理为
萃取的反应原理为![]() ,向有机相2中加入
,向有机相2中加入![]() 能进行反萃取的原因是________(结合平衡移动原理解释)。
能进行反萃取的原因是________(结合平衡移动原理解释)。
(7)水相2中的主要溶质除了![]() ,还有________(填化学式)。
,还有________(填化学式)。
(8)![]() 可用作电极,若选用
可用作电极,若选用![]() 电解质溶液,通电时可转化为
电解质溶液,通电时可转化为![]() ,其电极反应式为________。
,其电极反应式为________。
清华大学的科学家将古老的养蚕技术与时兴的碳纳米管和石墨烯结合,发现通过给蚕宝宝喂食含有碳纳米管和石墨烯的桑叶,可以获得更加牢固的蚕丝纤维。已知:当把石墨片剥成单层之后,这种只有一个碳原子厚度的单层就是石墨烯。下列说法正确的是( )
A. 蚕丝纤维的主要成分是纤维素
B. 石墨烯像烯烃一样,是一种有机物
C. 碳纳米管和石墨烯互为同素异形体
D. 碳纳米管具有丁达尔效应
取三张蓝色石蕊试纸放在玻璃棒上,然后按顺序分别摘加69% HNO3,98.3% H2SO4和新 制氯水,三张试纸最后呈现的颜色依次为
A 白 红 白 B 红 黑 红 C 红 红 红 D 白 黑 白
VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途。
请回答下列问题:
(1)砷的基态原子的电子排布式为___________________。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______________。
(3)NH3的沸点比PH3高,原因是___________;PO43-离子的立体构型为___________。
(4)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为______________。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因_____________________。
(6)磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如下图。已知最近两个白磷分子间的距离为 a pm(1pm=10-12m),阿伏加德罗常数的值为NA,则该晶体的密度为__________________g/cm3(只要求列算式,不必计算)。

实验室用如下图所示装置验证苯与溴反应的产物以及反应类型。

(1)由分液漏斗往烧瓶中滴加苯与溴的混合液时,反应很剧烈,可明显观察到烧瓶中充满了______________色气体。反应方程式: ;
(2)洗气瓶中产生的现象是: ,四氯化碳的作用是: ,如果省略洗气瓶, (填“能”或“不能”得到正确结论;
(3)则烧杯中产生的现象: ,说明苯与溴的反应是 反应;
(4)用离子方程式表示除去溴苯中溶解的溴: 。
下列有机化合物中沸点最高的是
A.乙烷 B.乙烯 C.乙醇 D.乙酸
高锰酸钾和氢溴酸溶液可以发生下列反应:KMnO4+HBr→Br2+MnBr2+KBr+H2O,其中还原剂是 (填物质的化学式),若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是 mol。
在CH3COOH![]() CH3COO-+H+的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是:
CH3COO-+H+的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是:
A、加入NaOH B、加入盐酸 C、加水 D、升高温度
.下列各组离子在给定条件下一定能大量共存的是
A.滴加甲基橙显红色的溶液中:Na+、K+、Cl-、ClO-
B.滴入KSCN显血红色的溶液中:Na+、Mg2+、SO42-、Br-
C.c(OH-)/c(H+)﹦1012的溶液中:K+、Na+、NO3-、HCO3-
D.由水电离的c(H+)﹦1.0×10-13 mol·L-1的溶液中:NH4+、Fe2+、NO3-、SO42-
A、B、C、D、E、F是前四周期原子序数依次增大的六种元素。A元素原子的核外电子数等
于其电子层数,B元素基态原子有三个能级且各能级电子数相同,![]() A与D可形成两种常见液态化合物
A与D可形成两种常见液态化合物
G、H,其原子数之比分别为1:1和2:1,E元素原子的K、L层电子数之和等于其M、N层电子数之
和,F被称为继铁、铝之后的第三金属,可用于制造飞机、火箭、人造卫星、宇宙飞船等领域。请回
答下列各题(涉及元素请用相应化学符号表示):
(1)B、C、D中第一电离最大的元素其基态原子有 种不同能量的电子。
(2)G分子中D原子的杂化方式为____,F2+的基态价电子排布式为____。
 (3) BA3-离子的空间构型为____,与其互为等电子体的一种阳离子的电子式为____。
(3) BA3-离子的空间构型为____,与其互为等电子体的一种阳离子的电子式为____。
(4)某化合物晶胞结构如右图所示, E2+的配位数是 。
(5)用高能射线照射液态H时,一个H分子能释放出一个电子,同时产生一种阳离子。
①释放出来的电子可以被若干H分子形成的“网”捕获,你认为H分子间能形成“网”的原因是 。
②由H分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与S02的水溶液反应
的离子方程式 ;该阳离子还能与H分子作用生成羟基,经测定此时的H
具有酸性,写出该过程的离子方程式 。
稀土有工业“黄金”之称,我国稀土资源丰富。目前从氟碳铈矿(主要化学成分为CeFCO3)提取铈族稀土元素的冶炼处理工艺已经发展到十几种,其中一种提取铈的工艺流程如下:

已知:①焙烧后烧渣中含+4价的铈及+3价的其他稀土氟氧化物;
②Ce4+能与SO![]() 结合成[CeSO4]2+,Ce4+能被萃取剂[(HA)2]萃取。
结合成[CeSO4]2+,Ce4+能被萃取剂[(HA)2]萃取。
请回答下列问题:
(1)CeFCO3中,Ce元素的化合价为________。
(2)“酸浸Ⅰ”过程中CeO2转化为Ce3+,且产生黄绿色气体,用稀硫酸和H2O2,替换HCl 就不会造成环境污染。则稀硫酸、H2O2与CeO2反应的离子方程式为_________________。
(3)“沉淀”步骤中发生的反应为Ce(BF4)3(s)+3KCl(aq)===3KBF4(s)+CeCl3(aq)。已知Ce(BF4)3、KBF4的Ksp分别为a、b,则该反应的平衡常数为________(用含a、b 的代数式表示)。
(4)“浸出液”中含有少量Ce4+及其他稀土元素的离子,可以通过“萃取”与“反萃取”作进一步分离、富集各离子。“萃取”时Ce4+与萃取剂[(HA)2]存在的反应为Ce4++n(HA)2![]() Ce(H2n-4A2n)+4H+。 用D表示Ce4+分别在有机层中与水层中存在形式的浓度之比:D=
Ce(H2n-4A2n)+4H+。 用D表示Ce4+分别在有机层中与水层中存在形式的浓度之比:D=![]() ,其他条件不变,在浸出液中加入不同量的Na2SO4以改变水层中的c(SO
,其他条件不变,在浸出液中加入不同量的Na2SO4以改变水层中的c(SO![]() ),D随浸出液中c(SO
),D随浸出液中c(SO![]() )增大而减小的原因是____________________________。
)增大而减小的原因是____________________________。
(5)“操作Ⅰ”后,向溶液中加入NaOH溶液,调节溶液的pH 可获得Ce(OH)3沉淀,当溶液中离子浓度小于1.0×10−6 mol·L−1时视为沉淀完全,常温下加入NaOH 调节溶液的pH应大于_______
_[已知:Ce(OH)3的Ksp=8.0×10−21;lg2=0.3]。
(6)写出“氧化”步骤的化学方程式:________________________________。
(7)CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着CeO2![]() CeO2(1-x)+xO2↑(0≤x≤0.25)的循环。写出CeO2消除CO 尾气的化学方程式:________________________________________________。
CeO2(1-x)+xO2↑(0≤x≤0.25)的循环。写出CeO2消除CO 尾气的化学方程式:________________________________________________。
过氧化钙是一种安全无毒的物质,带有数量不等的结晶水,通常还含有部分氧化钙.
(1)称取0.542g过氧化钙样品,灼热时发生如下反应:2(CaO2•xH2O)![]() 2CaO+O2↑+2xH2O,得到的O2在标准状况下体积为67.2ml.该样品中CaO2的物质的量为 .
2CaO+O2↑+2xH2O,得到的O2在标准状况下体积为67.2ml.该样品中CaO2的物质的量为 .
(2)另取同一样品0.542g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g.
①试计算样品中CaO的质量.
②试计算样品中CaO2•xH2O的x值.
一种熔融碳酸盐燃料电池原理示意如图,下列有关该电池的说法正确的是( )
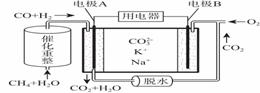
A.反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移8mol电子
3H2+CO,每消耗1molCH4转移8mol电子
B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C.电池工作时,CO32-向电极B移动 D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
反应N2O4(g)![]() 2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.A、C两点气体的平均相对分子质量:A>C
D.由状态B到状态A,可以用加热的方法
- 为了逐步改善人民的居住条件,国家一方面大力遏制房价的过快增长,另一方面不断加大对保障性安居住房建设的投入力度.2011年
- 如图所示,从点光源S发出的一束细白光以一定的角度入射到三棱镜的表面,经过三棱镜的折射后发生色散现象,在光屏的ab间形成一
- 北京市某区依托智慧城市理念,整合各类服务资源,构建一个全响应式社会服务管理平台,通过管理平台,政府部门能够快速掌握服务对
- 我国幅员辽阔,农业历史悠久。各地农业发展条件差异很大,农业发展方向也不尽相同。回答下题。 东营地区农业发展的不利条件是
- 下列物质在氧气中燃烧,火星四射,有黑色固体生成的是 ( ) A.红磷 B.木炭
- 氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2
- 【物理选修3-5】 (1)目前,在居室装修中经常用到花岗岩、大理石等装修材料,这些岩石都不同 程度地含有放射
- 有人设想将碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(即碳酸钙粒子直径达到纳米级),这将引起建筑材料的性能发生巨大变化。
- 如图,在菱形ABCD中,AB=5,对角线AC=6,若过点A作AE⊥BC,垂足为E,则AE的长为.
- 2012年就业高峰已经来临,有关人士呼吁大学生进一步树立正确的择业观念,形成毕业生面向基层就业的良好氛围。劳动者应树立的
- It is a great for a person to be able to drive when
- 在我国,人民行使国家权力需要有适当的组织形式。坚持人民代表大会制度,能使社会主义民主更加完善,人民的政治.经济和文化权益
- 儒家思想是中华民族宝贵的精神财富,也是世界文明史中极为重要的组成部分。在历史的长河中,有无数先哲曾留下若干睿智的言论。下
- 当碳、氢、氧、氮、溴等元素的原子量均取整数时,下列说法一定正确的是( ) A.a一氨基酸的式量均为偶数;
- 动物运动的方式多种多样,动物运动所消耗的能量主要来自( )A.肌细胞内有机物的分解 B.肌细胞内含有
- 用食用白醋(醋酸浓度约1 mol/L)进行下列实验,能证明醋酸为弱电解质的是( ) A.白醋中滴入石蕊试液呈红色 B
- 已知集合A={1,2,4},则集合B={(x,y)|x∈A,y∈A}中元素的个数为 A.3
- 某城市进行旧城区人行道的路面翻新,准备对地面密铺彩色地砖,有人提出了以下种地砖的形状供设计选用.其中不能进行密铺的地砖的
- 已知:(1)有机物可归属于酯类,但该种酯一般不能由相应的羧酸直接制得。(2)有机物A的结构为,有机物B的。(3)有机物C
- 现实生活中我们发现男性的声音一般低沉而浑厚,女性的声音高亢而尖细,这主要是因为人们在说话或唱歌时,气体经过( )引








