高三化学试题
“富勒烯“材料家族包括C60、C70、N60、B40,下列说法正确的是
A.B40和C70都属于新型化合物 B.B40、C60、C70、N60分子内都只含共价键
C.C60和C70属于同分异构体 D. B40、C60、C70、N60都属于烯烃
下列实验中,对应的实验现象和实验结论都正确且具有因果关系的是( )
| 实验方法或操作 | 实验现象 | 实验结论 |
| 将小块Na放入CuSO4溶液中 | 钠浮在水面上四处游动,溶液中有红色沉淀生成 | 金属Na比Cu活泼 |
| 在淀粉粉末中加入适量浓硫酸 | 淀粉变黑 | 浓硫酸具有吸水性 |
| 在AlCl3溶液中逐滴滴入NaOH溶液至过量,然后通入CO2气体 | 先出现白色沉淀,后沉淀消失,最后又出现白色沉淀 | Al(OH)3是两性氢氧化物,但不能溶解在某些弱酸中 |
| 将装满氯水的圆底烧瓶倒置在有氯水的水槽中,日光照射 | 烧瓶内有气泡向上逸出 | 日光照射时,溶解的Cl2逸出 |
下列有关有机物结构和性质的说法错误的是( )
A. 分子式为C4H10O且能与 Na反应放出气体的结构共有4种
B. 石油是混合物,可通过分馏得到汽油、煤油等纯净物
C. 苯甲酸(![]() )分子中所有原子可能位于同一平面
)分子中所有原子可能位于同一平面
D. 1mol盐酸美西律(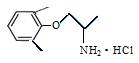 )最多可与3 mol H2发生加成
)最多可与3 mol H2发生加成
Ⅰ.化合物E可以通过下图所示的路线合成:

(1)A中含有的官能团名称为 。除不稳定的乙烯醇(CH2=CHOH)外,A的另一种同分异构体的结构简式是____________。
(2)写出D与过量NaOH溶液完全反应的化学方程式。(有机物用结构简式表示)_________________
(3)若化合物E中带“*”号的C原子来自D中的①甲基,且该反应的副产物是甲醇,则D→E的反应类型是 。
Ⅱ.我国盛产山茶籽精油,其主要成分柠檬醛可以合成具有工业价值的β紫罗兰酮。

(4)①要检验柠檬醛中含有碳碳双键,需要使用下列试剂中的 (按反应顺序填试剂序号)。
A.氢氧化钠溶液 B.酸性高锰酸钾溶液
C.银氨溶液 D.碳酸钠溶液
②写出柠檬醛和新制氢氧化铜反应的化学方程式: 。
③柠檬醛有多种同分异构体,能满足下列条件的同分异构体有 种。
A.含有一个![]() 的六元环结构,六元环上只有一个取代基
的六元环结构,六元环上只有一个取代基
B.能发生银镜反应
在下列各溶液中,离子一定能大量共存的是( )
A. 强碱性溶液中:K+、Mg2+、Cl—、SO42—
B. 室温下,pH=1的盐酸中:Na+、Fe3+、NO3—、SO42—
C. 含有Ca2+的溶液中:Na+、K+、CO32—、Cl—
D. 由水电离产生的c(H+)=1×10—3溶液中:Na+、K+、Cl—、SiO32—
下面有关电化学的图示,完全正确的是( )





A. Cu﹣Zn原电池 B. 粗铜的精炼 6题图
C. 铁片镀锌 D. 验证NaCl溶液(含酚酞)电解产物
在下列物质间的转化关系中,A是一种正盐,Z通常为液态,D的相对分子质量比C的相对分子质量大16,当X无论是强酸还是强碱时,其转化关系如图所示:
A![]() B
B![]() C
C![]() D
D![]() E
E
(1)当X是强酸时,A,B,C,D,E均含有同一元素,请回答(填化学式):
A是 ,Y是 ,Z是 。
(2)当X是强酸时,E是 ;当X是强碱时,E是 。
相对分子质量为128的有机物A,完全燃烧只生成二氧化碳和水,A分子中含有一个六元碳环,A能与NaHCO3溶液反应生成CO2,则其碳环上的一溴代物有( )
A. 3种 B. 4种 C. 5种 D. 6种
标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,则该混合气体中,CO的质量为 g,CO2的体积为 L
硫酸是中学化学中最常用的试剂之一。请回答下列问题:
(1)甲同学稀释浓硫酸的操作如下:用100mL量筒量取20mL 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100mL刻度线,再搅拌均匀。该同学操作中的两处错误之处是__________、___________。
(2)乙同学准确配制3.6mol/L稀硫酸的操作为:量取20mL 18mol/L 浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①该实验中两次用到玻璃棒,其作用分别是_________、________。
②使用容量瓶前必须进行的一步操作是__________。
③在该实验中,以下操作正确的是_________(填字母)。
a.洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
b.待稀释后的H2SO4溶液冷却至室温再转移到容量瓶中
c.转移前应将使用的容量瓶烘干
d.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④若定容时不小心使液面超过了刻度线,应采取的措施是_______
(3)丙同学用已知物质的量浓度的硫酸来测定未知物质的量浓度的NaOH溶液时,以酚酞作指示剂。
①滴定时,当观察到溶液_____________,即为滴定终点。
②某同学根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测NaOH溶液 的体积/mL | 0.0500mol/L硫酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.15 |
| 第二次 | 25.00 | 0.56 | 30.30 |
| 第三次 | 25.00 | 0.20 | 26.45 |
则待测NaOH溶液的浓度为___________,下列操作中可能使所测NaOH溶液的浓度数值偏低的是_________(填字母)。
A.酸式滴定管未用标准硫酸润洗就直接注入标准硫酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取硫酸体积时,开始仰视读数,滴定结束时俯视读数
下列图中,表示2A(g)+B(g)⇌ 2C(g) ΔH<0可逆反应的图像为

A. B. C. D.
炼锌厂的铜镉废渣中含有铜、锌、镉、铁、砷等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得ZnSO4‧7H2O实现资源的再利用。其流程图如下。已知FeAsO4难溶于水;ZnSO4‧7H2O易溶于水,难溶于乙醇。

| 金属离子 | Fe3+ | Zn2+ | Mn2+ | Cu2+ | Cd2+ |
| 开始沉淀pH | 2.7 | 6.5 | 7.7 | 5.2 | 6.9 |
| 沉淀完全pH | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
请回答下列问题:
(1)提高浸出率可以采用的方法是(写出其中一点即可)______________。
(2)滤液I中有少量的AsO33-,AsO33-与Cd反应会产生一种有毒氢化物气体,该气体的分子式为_________。向滤液I中滴入酸性KMnO4溶液可发生如下反应,完成该反应的离子方程式:___ Fe2++ ___ AsO33-+___MnO4-+ ___□= ___Mn 2++___FeAsO4↓+___□,
判断该滴定终点的现象是_____________________________________ 。
(3)流程中②调节pH时可以选用的试剂为__________,滤渣Ⅱ的主要成份为________。
(4)制得的ZnSO4‧7H2O需洗涤,洗涤晶体时可选用试剂为( )。
A.水 B.乙醇 C. 饱和硫酸锌溶液 D.稀硫酸
碳、氮和铝的单质及其化合物在工农业生产和生活中有重要用途.
(1)真空碳热还原一氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlC13(g)+3C(s)═ 3AlCl(g)+3CO(g) △ H=a kJ•mol﹣1
3AlCl(g)═ 2Al(l)+AlC13(g) △ H=b kJ•mol﹣1
用含a、b的代数式表示反应:Al2O3(s)+3C(s)=2Al(l)+3CO(g)的
△H=_____kJ•mol﹣1.
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g)△H=Q kJ•mol﹣1.在T1℃时,反应进行到不同时间测得各物质的浓度如下(时间单位为min,浓度单位为mol/L):
|
| 0 | 10 | 20 | 30 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 |
| N2 | 0 | 0.16 | 0.25 | 0.25 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 |
①0~ 10min内,NO的平均反应速率v( NO)=_____,T1℃ 时,该反应的平衡常数K=_____.
②30min后升高温度至T2℃ ,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q_____0(填“> ”、“< ”或“═ ”)
③在恒容条件下,能判断该反应一定达到化学平衡状态的依据是 _____(填选项编号).
a.单位时间内生成2nmolNO( g)的同时消耗nmolCO2( g)
b.反应体系的压强不再发生改变
c.混合气体的密度保持不变
d.混合气体的平均相对分子质量保持不变
④若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c( NO)=_____mol/L.NO的转化率_____(填“增大”、“减小”或“不变”).
(3)直接排放煤燃烧产生的烟气会引起严重的环境问题,将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图.电极b表面发生的电极反应式为_____.

现有CuO和Fe2O3组成的混合物ag,向其中加入2mol·L-1的硫酸溶液50mL,恰好完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量为 ( )
A. 1.6a g B.(a-1.6)g C.(a-3.2) g D. 1.6 g
下列关于硅及其化合物的说法不正确的是
A.水玻璃可用作木材防火剂 B.硅是制造光导纤维的材料
C.硅是制造太阳能电池的常用材料 D.硅是构成一些岩石和矿物的基本元素
某烃A,可做水果的催熟剂,其蒸汽密度是氢气密度的14倍。一定条件下,它能发生如下的转化(已知:2CH3CHO+O2![]() 2CH3COOH,框图中部分生成物略去)。
2CH3COOH,框图中部分生成物略去)。

(1)写出A→B的反应方程式:_____________________。
(2)写出B+D→E的反应方程式:___________________,反应类型为_____________。
(3)写出F→G的反应方程式:_____________________,反应类型为______________。
能够说明氨水是弱碱的事实是 ( )
A.氨水具有挥发性 B.1 mol·L-1氨水溶液pH≈ll
C.氨水溶液能导电 D.氨水与HCl溶液反应生成NH4Cl
下列类比关系正确的是
A. Na2O2 与 CO2 反应生成 Na2CO3 和 O2,则 Na2O2 与 SO2 反应可生成 Na2SO3 和 O2
B. Fe 与 Cl2 反应生成 FeCl3,则 Fe 与 I2 反应可生成 FeI3
C. 钠与氧气在不同条件下反应会生成两种不同的氧化物,则 Li 与氧气反应也能生成 Li2O 或 Li2O2
D. Al 与 Fe2O3 能发生铝热反应,则与 MnO2 也能发生铝热反应
设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A.标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA
B.某密闭容器盛0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA
C.1 mol Na与足量O2在一定条件下完全反应时转移电子数为NA
D.1 mol·L-1Na2SO4溶液中,Na+和SO![]() 离子数的总和一定为3NA
离子数的总和一定为3NA
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
【探究一】
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是___________
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+应选用________(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.KMnO4酸性溶液
②乙同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:[SO2+Br2+2H2O=2HBr+H2SO4 然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为________。
【探究二】
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。


(3)装置B中试剂的作用是___________________
(4)认为气体Y中还含有Q的理由是________________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于________(选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是__________
(7)若要测定336mL气体中H2的含量(标准状况下约有28 mL H2),可否用托盘天平称量D或E反应前后的质量差的方法?做出判断并说明理由__________
- 将两株生长状况基本相同的玉米幼苗,分别在土壤浸出液和蒸馏水中培养,结果如图,此现象说明植物的生活需要() A. 水
- 依据下面语句,仿写两句,要求三句话语意互相关联。 种子如果害怕遭遇泥土埋没,就可能永远难以体味嫩芽破土而出时的那一种
- 如图为我国古代建造宫殿移动大石料的情景,此图提供的信息解释合理的是( ) A.左边的人所使用的撬棒相当于费力杠
- _____ book looks moreinteresting than ______. A.Your; mine
- 已知回归方程为=0.50x-0.81,则x=28时,y的估计值为___________.
- 下列各句中,没有语病的一项是( ) A.户籍制度像一堵无形的墙,不仅催生出大都市与中小城市、沿海城市与内地城
- 如图所示,细杆的一端与一小球相连,可绕过O点的水平轴自由转动。现给小球一初速度,使它做圆周运动,图中a、b分别表示小球轨
- 对危险化学品要在包装标签上印有警示性标志。天然气应选用的标志是( ) A B
- 下列各句中,没有语病的一句是A. 2008年的奥运会,全球聚焦北京,但根据台湾《远见》杂志近日所作“两岸交流大调查”结果
- 某科学家用14C标记的CO2来追踪光合作用中的碳原子,这种碳原子的转移途径为:CO2→C4→C3→糖类,那么其研究对象最
- Does ______ matter if he can’t be here on time? A. this
- 在①分子、②原子、③质子、④中子、⑤电子、 ⑥离子;这些微粒中,(1)物质的微粒有 ; ⑵显示电中性的微
- (8分)小明的妈妈买了一个自动电热水壶,其部分技术参数如表中所列。型号额定电压频率额定功率容量FY-TS1010A220
- 给下列句子排序,最恰当的一项是(3分)( )①1978年2月,荣毅仁被解救复出,现在他是中国国际信托投资公司的董事长。
- 已知函数的定义域为A,函数的值域为B,(1)求集合A、B;(2)求AB,AB
- 世博会被誉为世界经济科技文化的盛会,2010年上海世博会的主题是“城市,让人生活更美好(Better City,Bet
- 将下列我国主要的牧区与牧区类型、主要畜种连线
- 为了更好治理和净化运河,保护环境,运河综合治理指挥部决定购买10台污水处理设备.现有A、B两种型号的设备,其中每台的价格
- 小肠来的血液到达右手必须经过( ) ①心脏一次 ②心脏二次 ③肺 ④肝 ⑤脑 A
- (09年山东实验中学诊断三文)已知函数,且是偶函数,则的大小关系是A. B. C.




