第一章 从实验学化学 知识点题库
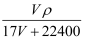 B . ω=
B . ω= 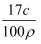 C . ω=
C . ω= 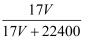 D . ρ=
D . ρ= 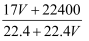
①放置酒精灯; ②固定铁圈位置; ③放上蒸发皿;
④加热搅拌; ⑤停止加热,余热蒸干
-
(1) 该气体所含原子总数为 个。
-
(2) 该气体若溶于1L水中(不考虑反应),设溶液的密度为ρg/cm3 , 则该溶液的物质的量浓度为 mol/L。
-
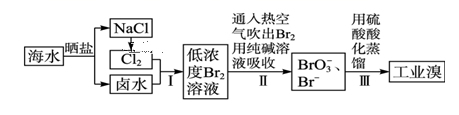
(1) 以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是。
-
(2) 步骤Ⅱ通入热空气吹出Br2,利用了溴的__________。A . 氧化性 B . 还原性 C . 挥发性 D . 腐蚀性
-
(3) 步骤Ⅱ中涉及的离子反应如下,请在下面横线上填入适当的化学计量数:Br2+CO32-= BrO3-+Br-+CO2↑
-
(4) 上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:。
-
(5) 实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是__________。A . 乙醇 B . 四氯化碳 C . 烧碱溶液 D . 苯
-
(1) 酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是 (填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作符合题意。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
-
(2) 氧化还原滴定——取一定量的草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,表格中记录了实验数据:
滴定次数
待测液体积
(mL)
标准KMnO4溶液体积(mL)
滴定前读数
滴定后读数
第一次
25.00
0.50
20.40
第二次
25.00
3.00
23.00
第三次
25.00
4.00
24.10
①滴定时发生的离子反应方程式,KMnO4溶液应装在 (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是。
②该草酸溶液的物质的量浓度为。
-
(3) 沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是______(填选项字母)。
难溶物
AgCl
AgBr
AgCN
Ag2CrO4
AgSCN
颜色
白
浅黄
白
砖红
白
Ksp
1.77×10-10
5.35×10-13
1.21×10-16
1.12×10-12
1.0×10-12
A . NaCl B . NaBr C . NaCN D . Na2CrO4
|
84消毒液 [有效成分] NaClO [规格] 1000mL [质量分数] 25% [密度] 1.192g·cm-3 |
回答下列问题:
-
(1) 工业上常用氯气与烧碱溶液反应制取84消毒液,写出反应的离子方程式。
-
(2) 84消毒液使用时需要稀释。某化学实验小组用上述84消毒液配制480mL0.2mol·L-1的稀溶液。
①量取84消毒液mL。
②洗涤时需要将仪器(填名称)洗涤2~3次。
③定容时加蒸馏水不慎超过了刻度线,此时应采取的处理方法是;该小组同学用量筒量取84消毒液时,仰视观察液面,所配溶液的浓度会(填“偏高”、“偏低”或“无影响")。
-
(3) 向84消毒液中加入少量稀硫酸可以增强漂白消毒效果,请解释其原因(用化学方程式回答)。
-
(1) 上述实验所利用的过氧化钠跟水反应的特点是:
第一,有氧气生成,第二,。Na2O2 跟水反应的离子方程式是。
-
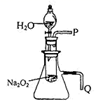
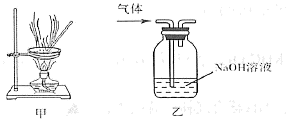
(2) 某研究性学习小组拟用如图所示装置(气密性良好)进行实验,以证明上述特点。用以验证反应的第一个特点的实验操作及现象是:。
用以验证第二个反应特点的实验操作及现象是:。
-
(3) 实验(2)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液,发现溶液先变红后褪色,为探究其原因,该小组同学从查阅有关资料中得知:Na2O2 与水反应可生成 H2O2 , H2O2 具有强氧化性和漂白性。
请设计一个简单的实验,验证 Na2O2 跟足量水充分反应后的溶液中有 H2O2 存在。(只要求写出实验所用的试剂及观察到的现象)试剂:;现象:。
-
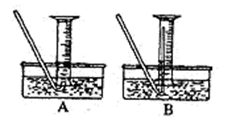
(4) 该小组同学提出用定量的方法探究 Na2O2 跟水反应后的溶液中是否含有 H2O2 , 其实验方法为: 称取 2.6gNa2O2 固体,使之与足量的水反应,测量产生 O2 的体积并与理论值比较,即可得出结论: 测量气体体积时,必须等到试管和量筒内的气体都冷却至室温时进行,应选用如图装置中的(忽略导管在量筒中所占的体积,导管伸入量筒的长度不同)(填字母)

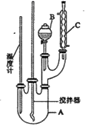
下列有关说法正确的是( )
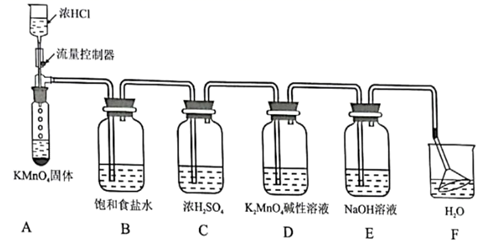
-
(1) 饱和食盐水的作用是。装置F可吸收微量氯气制得氯水,使用倒置漏斗的目的是。
-
(2) 装置A中产生Cl2的化学方程式为,可推知氧化性:Cl2
 (填“>”或“<”)。
(填“>”或“<”)。
-
(3) 装置D中可观察到溶液变紫红色,则该反应的离子方程式为,可推知氧化性Cl2
 (填“>”或“<”)。
(填“>”或“<”)。
-
(4) 通过对比(2)和(3)可判断的氧化性强弱的影响因素是。利用本实验充分反应所得溶液设计实验验证你的判断。实验方案为。
-
(5) 有同学认为无需流量控制器,你是否认可?并简要说明理由。
-
(1) I.如图所示,使用试剂和装置探究二氧化硫的还原性:
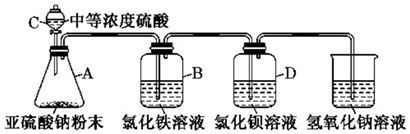
A中反应的离子方程式为。装置C中硫酸质量分数大约为70%,用此浓度硫酸的理由是。
-
(2) 装置B中溶液的现象为。
-
(3) 学生甲预测装置D中没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。学生乙经过查阅资料发现少量白色沉淀可能是硫酸钡,因为装置或溶液中少量的氧气参与了氧化反应,请写出装置D中反应的化学方程式:。
-
(4) II.学习小组又设计了如下装置,检验SO2在无氧干扰时,是否与氯化钡反应生成沉淀。(所配制的溶液均使用无氧蒸馏水)
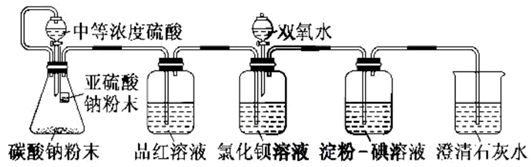
加入碳酸钠粉末的目的是。
-
(5) 当时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
-
(6) 结合实验目的分析装置中选用澄清石灰水而不用氧化钠溶液的原因是。
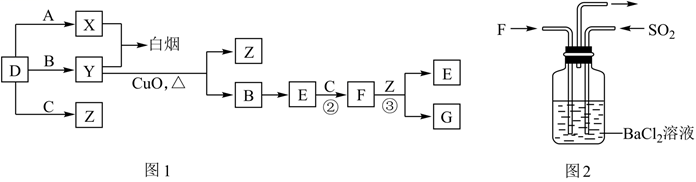
请回答下列问题:
-
(1) Y的化学式为。
-
(2) Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为。
-
(3) Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为。
-
(4) 气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图2所示),洗气瓶中白色沉淀是。
-
(5) 标准状况下,将NO2充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度为mol·L﹣1(分数或小数表示均可)
 在生产、生活中有广泛用途,如饮用水的净化、造纸工业的施胶剂、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含
在生产、生活中有广泛用途,如饮用水的净化、造纸工业的施胶剂、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含  及少量
及少量  和
和 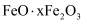 )可制备明矾,工艺流程如图:
)可制备明矾,工艺流程如图:  回答下列问题:
回答下列问题:
-
(1) “滤渣①”的主要成分是(填化学式)。
-
(2) 加入稀硫酸酸化后,再经“一系列操作”可得到明矾晶体
 ,则“一系列操作”是、、、洗涤、干燥。
,则“一系列操作”是、、、洗涤、干燥。
-
(3) 流程中加入
 的作用是,写出反应的离子方程式:。
的作用是,写出反应的离子方程式:。
-
(4) 若将铝灰投入过量的氢氧化钠溶液中,所得溶液的溶质除
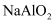 外,还含有(填化学式)。写出生成气体的该反应的化学方程式:。
外,还含有(填化学式)。写出生成气体的该反应的化学方程式:。
-
(1) NaOH溶液的物质的量浓度为 mol·L-1。(含a、b的代数式表示)
-
(2) 当生成物中NaNO2和NaNO3的物质的量之比为4:1时,则a∶b= 。(要求写出计算过程)
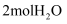 的摩尔质量是36g
B . 1mol水的质量是
的摩尔质量是36g
B . 1mol水的质量是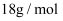 C .
C .  含有的电子数为10NA
D . 标准状况下,1mol水的体积约是22.4L
含有的电子数为10NA
D . 标准状况下,1mol水的体积约是22.4L
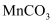 是重要化工原料,由
是重要化工原料,由 制备
制备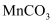 的一种工艺流程如下:
的一种工艺流程如下:Ⅰ. 研磨 , 加水配成浊液。
, 加水配成浊液。
Ⅱ.  浊液经还原、纯化、制备等过程,最终获得
浊液经还原、纯化、制备等过程,最终获得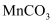 固体。
固体。

资料:①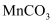 不溶于水。该工艺条件下,
不溶于水。该工艺条件下, 与
与 不反应。
不反应。
②难溶电解质的溶度积: 、
、
-
(1) 研磨
 的目的是。
的目的是。
-
(2) 加入铁粉除去
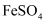 溶液中的
溶液中的 , 反应的离子方程式是。
, 反应的离子方程式是。
-
(3)
 氧化
氧化 的反应如下:
的反应如下: 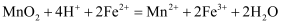
①根据上述反应,还原
 所需的
所需的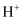 与
与 的物质的量比值应为2.而实际比值(1~1.25)小于2,原因是。
的物质的量比值应为2.而实际比值(1~1.25)小于2,原因是。②取少量母液,滴加
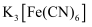 溶液,未产生蓝色沉淀,说明。
溶液,未产生蓝色沉淀,说明。 -
(4) 纯化
向母液中滴加氯水调
 , 除去残留的
, 除去残留的 。若母液中
。若母液中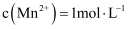 , 使
, 使 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中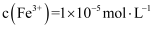 , 此时是否有
, 此时是否有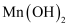 沉淀生成?(列式计算,已知
沉淀生成?(列式计算,已知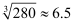 )。
)。 -
(5) 制备
将
 纯化液与稍过量的
纯化液与稍过量的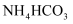 溶液混合,得到含
溶液混合,得到含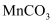 的浊液。将浊液过滤,洗涤沉淀,干燥后得到
的浊液。将浊液过滤,洗涤沉淀,干燥后得到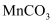 固体。
固体。①通过检验
 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是。
的操作是。②生成
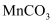 的离子方程式是。
的离子方程式是。
- 如图所示,一个半径为R的导电圆环与一个轴向对称的发散磁场处处正交,环上各点的磁感应强度B大小相等、方向均与环面轴线方向成
- 下列对Na2O和Na2O2的叙述中正确的是A.Na2O、Na2O2均能与盐酸反应生成NaCl,二者都是碱性氧化物B.Na
- 秦岭-淮河一线大致同哪些界线相一致?( ) ①1月0℃等温线
- 政府决定用“对社会的有效贡献率”对企业进行评价,用表示某企业第n年投入的治理污染的环保费用,用表示该企业第n年的产值.
- 甲乙两个电阻的阻值分别为4Ω和8Ω,若将它们串联后接在6V的电源两端(电源电压保持不变),则通过甲电阻的电流是
- 7、下列各项中加点词的活用类型,与其他三项不同的一项是() A.策扶老以流憩 B.或棹孤舟 C.
- 下列简称所表示的省份相邻的是 A.京沪 B.云冀 C.湘鄂 D.陕闽
- 《孙中山选集》下卷载“因此吾人欲证实民族主义实为健全之反帝国主义,则当努力于赞助国内各种平民阶级之组织,以发扬国民之能力
- The United Nations hopes every country can be ________ in pr
- 阅读下面一段文字,完成7-9题。 什么是“和谐社会”?社会学认为,社会是由人群组成的一种特殊形态的群体形式,是相当
- 党的十八届五中全会提出,坚持共享发展,要建立更加公平可持续的社会保障制度,实施全民参保计划,实现职工基本养老金全国统筹,
- 右图是产品生命周期与销售利润曲线图。如果要阻止产品生命周期从A点到B点运动,企业应该采取的措施是( )①增加产品
- ________excited Geoff Marcy most was ________ there were pl
- 全称命题x∈R,x2+5x=4的否定是( )A.x∈R,x2+5x=4 B.x∈R,x2+
- Somestudents goes to school ______ bike, others goes to sch
- 下图为华北地区局地地形及地下水位剖面图,读图回答34~35题。 34. 下列说法正确的是 A. 海拔越高地
- 天时不如地利, 。(《<孟子>两章》
- 如图抛物线过 A(-1,0)、B(4,0)、C(0,2)三点。 (1)求抛物线解析式 (2)点C,D关于抛物线对称轴对称
- 正三棱锥V―ABC的底面边长为2a,E、F、G、H分别是VA、VB、BC、AC的中点,则四边形EFGH的面积的取值范围是
- 目前,黄河三角洲地区拥有未利用地近8007万亩,人均未利用地0.81亩,比我国东部沿海地区平均水平高近45%。图11是黄



