第一章 从实验学化学 知识点题库
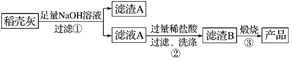
通过如下流程可由稻壳灰制备较纯净的二氧化硅。
请回答下列问题:
-
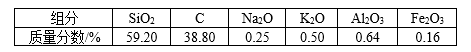
(1) 根据氧化物的性质进行分类,稻壳灰中属于两性氧化物的是。
-
(2) 步骤①中涉及SiO2的离子反应方程式为。
-
(3) 滤渣A的成分有和(填化学式)。
-
(4) 滤渣B的成分是(填化学式)。
-
(5) 过滤所需的玻璃仪器除烧杯和玻璃棒外,还有。
-
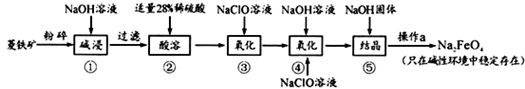
(1) Na2FeO4中铁元素的化合价为,高铁酸钠用于杀菌消毒时的化学反应类型为(填“氧化还原反应”、“复分解反应”或“化合反应”)。
-
(2) 按照上述流程,步骤①中碱浸时能否用较便宜的Ca(OH)2替代NaOH (填“能”或“不能”),理由是。
-
(3) 步骤③中检验Fe2+全部转化成Fe3+的方法是:。
-
(4) 步骤④中除生成Na2FeO4外,还有NaCl生成,其离子方程式为。已知步骤⑤是向Na2FeO4溶液中继续加入氢氧化钠固体得到悬浊液,则操作a的名称为。
-
(5) 生产过程中,理论上每获得0.5mol的FeO42-消耗 NaClO的总质量为。
-
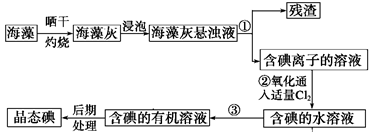
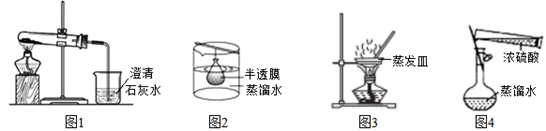
(1) 指出提取碘的过程中有关的实验操作名称:
①;写出过程②中有关反应的离子方程式:
-
(2) 灼烧海带用到的仪器有
-
(3) 提取碘的过程中,可供选择的有机试剂是()
A .酒精 B .四氯化碳
C .甘油 D .醋酸
-
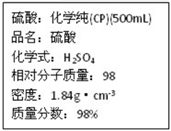
(1) 该硫酸的物质的量浓度为mol/L。
-
(2) 某化学小组进行硫酸酸性实验探究时,需要240 mL4.6 mol/L的稀硫酸,则需要取上述的浓硫酸mL。
-
(3) 在配制4.6 mol/L稀硫酸的过程中,下列情况对所配制硫酸溶液物质的量浓度有何影响?(填“偏高”“偏低”或“无影响”)
①未经冷却趁热将溶液注入容量瓶中;
②定容时仰视刻度线;
③用量筒量取浓硫酸时俯视;
④移液时不慎将少量溶液滴在容量瓶外面。
-
(4) 实验过程中出现下列情况应如何处理?
①向容量瓶中加入蒸馏水至距刻度线1~2 cm时,应;
②加蒸馏水时不慎超过了刻度,应。

-
(1) 该盐酸的物质的量浓度为
-
(2) 下列实验操作会导致实验结果偏低的是()
①配制100g 10%的CuSO4溶液,称取10g 硫酸铜晶体溶于90g水中
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为0.2g,所得溶液的浓度
④用酸式滴定管量取用98%,密度为1.84g/cm3的浓H2SO4配制200mL 2mol•L-1的稀H2SO4时,先平视后仰视。
A.只有① B.只有② C.②③④ D.①③④
-
(3) 已知CO和CO2的混合气体14.4g,在标准状况下所占的体积为8.96L。则该混合气体中,CO的质量为g,CO2的物质的量为mol。
-
(4) 1mol氧气在放电条件下,有30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是(____________)A . 16 B . 17.8 C . 18.4 D . 35.6
-
(1) 同温同压下,同体积的甲烷(CH4)和二氧化碳原子总数之比为,密度之比为。
-
(2) 在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则其中CO2为 mol。
-
(3) 9.03×1023个NH3含mol氢原子,在标准状况下的体积为L。
-
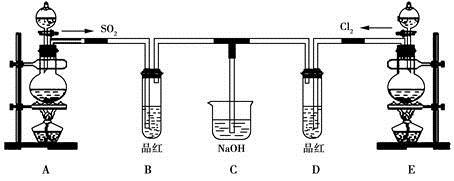
(1) 实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:;
-
(2) 实验室用装置E制备Cl2 , 其反应的化学化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O;若有6 mol的HCl参加反应,则转移的电子总数为;
MnCl2+Cl2↑+2H2O;若有6 mol的HCl参加反应,则转移的电子总数为;
-
(3) ①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:,D:。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:,D:。
-
(4) 另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)。
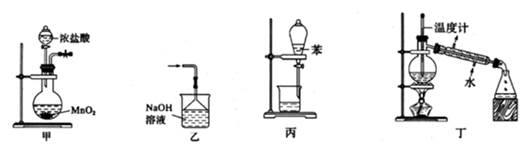
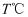 时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:
时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下: | 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
-
(1) ①在2~3 min时间段内,用盐酸的浓度变化表示的反应速率为.
②在0~5min内,反应速率最大的时间段是(填 “1~2 min”、“2~3 min”或“3~4 min”)。
-
(2) 若完全反应后放出15.2 kJ的热量,则反应Zn(s) + 2HCl(aq)=ZnCl2(aq) + H2(g)的△H=
-
(3) 为了减缓反应速率但不减少产生气体的量,可向反应物中分别加入等体积的下列液体,你认为可行的是(填字母)。
a. 蒸馏水 b. Na2CO3溶液 c. NaNO3溶液
-
(4) 为了加快反应速率但不减少产生气体的量,某同学向反应物中加入了少量CuSO4固体,该同学操作(填 “合理”或“不合理”),理由是
 、Ni2+以及少量的Zn2+、Cu2+、Fe2+、Fe3+等),采用如图工艺流程回收其中的镍制备NiSO4晶体。
、Ni2+以及少量的Zn2+、Cu2+、Fe2+、Fe3+等),采用如图工艺流程回收其中的镍制备NiSO4晶体。 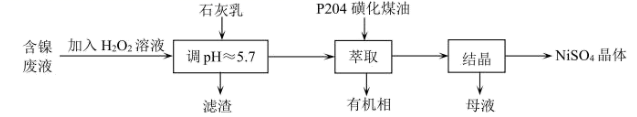
资料:
P2O4为磷酸二异辛酯(可用HA表示),不溶于水,是一种弱酸性萃取剂。其酸根离子(A-)可与某些金属离子发生反应。
-
(1) 写出H2O2的电子式。
-
(2) 加入H2O2溶液发生反应的离子方程式为。
-
(3) 加石灰乳的作用是。
-
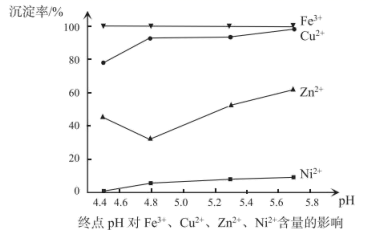
(4) 在萃取过程中,若溶液酸度过高,会导致萃取效率变低,其原因是。
-
(5) 在结晶过程中,需要加浓硫酸调pH至2~4,再进行,过滤出的固体洗涤、干燥,得NiSO4晶体。
NiSO4在不同温度下的溶解度
温度/℃
20
30
40
60
80
90
100
溶解度/g
44.4
46.6
49.2
55.6
64.5
70.1
76.7
-
(6) NiSO4在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式。
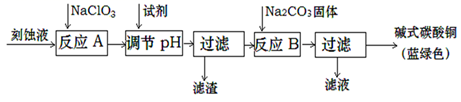
Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
回答下列问题:
-
(1) NaClO3中氯元素的化合价为。
-
(2) 完成反应A的离子方程式:
 +Fe2++_=Cl-+Fe3++_,。
+Fe2++_=Cl-+Fe3++_,。
-
(3) 滤渣的成分是,调节pH的范围是,选用的试剂较好的是(填以下字母编号)。
A.硫酸 B.氨水 C.氧化铜 D.氢氧化钠
-
(4) 反应B有气泡产生,则反应B的离子方程式为。
-
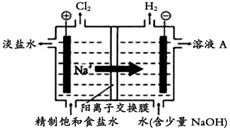
(5) 滤液中回收的副产物主要是NaCl,常用于氯碱工业,电解饱和食盐水的原理示意图如下所示,溶液A的溶质是,电解时用盐酸控制阳极区pH在2~3,用平衡移动原理解释盐酸的作用。
下列说法正确的是( )
选项 | 混合物 | 除杂试剂 | 分离方法 |
A | 苯(苯酚) | 浓溴水 | 过滤 |
B | 溴苯(溴) | NaOH溶液 | 分液 |
C | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
D | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
- 补写出下列名篇名句中的空缺部分。(任选1题) (1)且夫天地之间,物各有主,苟非吾之所有,_______________
- 阅读下列材料,回答问题。 2002年春季,席卷半个中国的沙尘暴正是沙漠化严重的结果和表现。沙尘暴发生的原因:一是大风;二
- 若某空间几何体的三视图如图所示,则该几何体的体积是 [ ] (A)2
- 使至塞上 王维 单车欲问边,属国过居延。 征蓬出汉塞,归雁入胡天。 大漠孤烟直,长河落日圆。 萧关逢候骑,都护在燕然。
- 正确读写化学符号是学好化学的基础。铝元素符号书写正确的是( ) A.AL B.al
- Our English teacher devoted herself to her teaching a
- 体积为1米3水的质量为(1)千克,全部变成冰后,冰的质量为(2)千克,冰的体积为(3)米3(冰的密度为0.9×103千克
- (09全国卷Ⅱ28)(15分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。回答下列问题
- 宋代我国精耕细作水平上升到一个新的高度,其主要标志是 A.出现间作、套作复种技术 B.实行轮作和
- 科研人员在研究某种植物时,从收获的种子开始做鲜重测量,画得如图所示曲线。下列对曲线变化原因的分析中,不正确的是() A
- 如图所示,玻璃缸的水中有金鱼,在鱼缸旁边拍掌,金鱼立即受惊,这时鱼接收到声波的主要途径是( )A.鱼缸→空气→水→鱼
- 如图,在△AEC中,点D和点F分别是AC和AE上的两点,连接DF,交CE的延长线于点B,若∠A=25°,∠B=45°,∠
- 图为一物体做直线运动的一t图象,由图象所给信息可以判断,在0一t1和t1一t2时间内 A.0一t1时间内物体走的位移比t
- 若l g水中含有m个氢原子,则阿伏加德罗常数可用含m的代数式表示为 ( ) A.m/9 B.9m
- 下面一段话中有四个错别字,把它们找出来填入表中,然后改正。(4分) 黄公望寄情尚湖,一幅幅画作描绘的是风景,也是
- 地球的体积和质量适中是其存在生命物质的重要条件。
- 阅读下面文言文 【甲】先生不知何许人也,亦不详其姓字,宅边有五柳树,因以为号焉。闲静少言,不慕荣利。好读书不求甚解每有会
- 读“水循环示意图”如图3-2,回答下列问题 图3-2 (1)写出图中各代号所代表的水循环的环节名称 A、
- 阅读下面的文字,完成后面的题。 揭开智力进化之谜 阿 碧 ①几百万年前,人类的祖先——南方古猿患上了一种“大头病”。古
- It isso wet there that the trees are extremely tall, some _



