第一章 从实验学化学 知识点题库
-
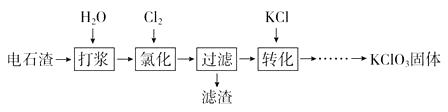
(1) 氯化过程控制电石渣过量、在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①电石与H2O反应的化学方程式为。生成Ca(ClO)2的化学方程式为。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有(填序号)。
A.适当加快通入Cl2速率
B.充分搅拌浆料
C.加水使Ca(OH)2完全溶解
-
(2) 氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:
6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。
75℃时,Ca(ClO)2进一步转化为Ca(ClO3)2的反应方程式为。
滤渣的主要成分为(填化学式)。
-
(3) 向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3的原因是。
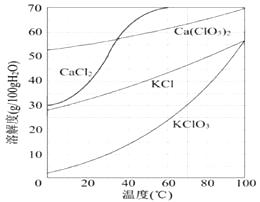
若溶液中KClO3的含量为100 g·L-1 , 从该溶液中尽可能多地析出KClO3固体的方法是。
分离或提纯物质的方法有:①过滤、②升华、③加热分解、④蒸馏、⑤结晶
-
(1) 除去氢氧化钙溶液中悬浮的碳酸钙颗粒。
-
(2) 从硝酸钾和氯化钠的混合液中获得硝酸钾。
-
(3) 除去固体碘中混有的少量氯化钠固体。
-
(4) 除去氯化钾中含有的氯酸钾。
-
(5) 分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
已知偏铝酸盐能与一般的酸反应,如:NaAlO2+HNO3+H2O→NaNO3+Al(OH)3↓
生产流程如图:

完成下列填空:
-
(1) 用氢氧化钠固体配制30%的氢氧化钠溶液,除烧杯、玻璃棒外还需(选填编号)。
A.
 B.
B.  C.
C.  D.
D. 
说出流程中产生的滤渣的一种用途是。制作一个过滤器需要。流程中操作x的名称是。
-
(2) 反应Ⅱ加入的硝酸必须适量,原因是。反应Ⅲ加入的硝酸要稍过量,原因是。
-
(3) 从反应Ⅲ所得的溶液制成产品的步骤依次为减压蒸发,,过滤,,低温烘干。
-
(4) 为测定所得的产品的纯度,质检人员称取产品Wg,溶于水配成500mL溶液,从中取出25.00mL,加入过量已知浓度的氨水充分反应后,剩余的氨水用已知浓度的盐酸溶液进行测定。通过计算便可得出产品的纯度。
①上述过程属于定量实验。其中除配制一定物质的量浓度的溶液外,还有一个是,该实验过程中要进行多次读数,读数的方法是读出与的刻度值。
②任意写出一个该测定过程中所涉及的化学反应的离子方程式:。
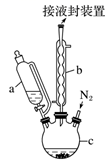
已知:Ⅰ.二茂铁熔点是173 ℃,在100℃时开始升华;沸点是249℃。
Ⅱ.制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O。
实验步骤为:
①在三颈烧瓶中加入25 g粉末状的KOH,并从仪器a中加入60 mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10 min;
②再从仪器a滴入5.5 mL新蒸馏的环戊二烯(C5H6 , 密度为0.95 g·cm-3),搅拌;
③将6.5 g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25 mL装入仪器a中,慢慢滴入仪器c中,45 min滴完,继续搅拌45 min;
④再从仪器a加入25 mL无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
-
(1) 仪器c的名称是。和普通分液漏斗相比,使用恒压滴液漏斗a的优点是。
-
(2) 步骤①中通入氮气的作用是。
-
(3) 步骤⑤用盐酸洗涤的目的是。
-
(4) 步骤⑦是二茂铁粗产品的提纯,该过程在如图装置中进行,其操作名称为;为了确认得到的是二茂铁,还需要进行的一项简单实验是;
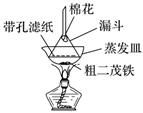
-
(5) 若最终制得纯净的二茂铁4.3 g,则该实验的产率为(保留小数点后一位)。
 数目为0.1 NA
D . 用惰性电极电解CuSO4溶液,外电路中通过电子数目为NA时,阳极产生5.6L气体
数目为0.1 NA
D . 用惰性电极电解CuSO4溶液,外电路中通过电子数目为NA时,阳极产生5.6L气体
请参照下表给出的数据填空。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
-
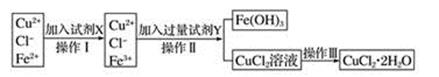
(1) 下列物质都可以作为X,适合本实验的X物质可以是___________(填字母)。A . KMnO4 B . NaClO C . H2O2 D . Cl2
-
(2) 操作II的Y试剂为(填化学式),并调节溶液的pH在范围。
-
(3) 实验室在配制CuCl2溶液时需加入少许(填物质名称),理由是(文字叙述并用有关离子方程式表示)。
-
(4) 若将CuCl2溶液蒸干灼烧,得到的固体是(填化学式);若要得无水CuCl2 , 请简述操作方法。
| 选项 | 物质(杂质) | 试剂 |
| A | CO2(NH3) | 浓硫酸 |
| B | H2(SO2) | 氢氧化钾溶液 |
| C | NO(NO2) | 水 |
| D | NH3(SO2) | 品红溶液 |
-
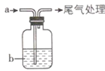
(1) Ⅰ.如图所示是完成1,2-二氯乙烷某些性质的实验装置。
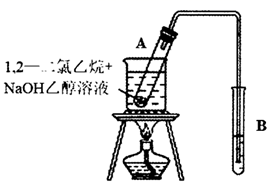
按图所示连接好仪器后,首先应进行的操作是。
-
(2) 在试管A里加入
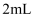 1,2-二氯乙烷和
1,2-二氯乙烷和 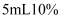 的
的  乙醇溶液,再向试管里加入几小块碎瓷片.加入碎瓷片的作用是。
乙醇溶液,再向试管里加入几小块碎瓷片.加入碎瓷片的作用是。
-
(3) 用水浴加热试管A里的混合物(其主要生成物仍为卤代烃,试管A中发生反应的化学方程式是,其反应类型是。
-
(4) 为检验产生的气体,可在试管B中盛放,现象是;向反应后试管A中的溶液里加入足量的稀硝酸,再加入几滴
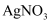 溶液,现象是。
溶液,现象是。
-
(5) Ⅱ.在制取乙酸乙酯中,有关浓硫酸的作用说法错误的是_______。A . 催化剂 B . 吸水剂 C . 脱水剂 D . 提高反应速率
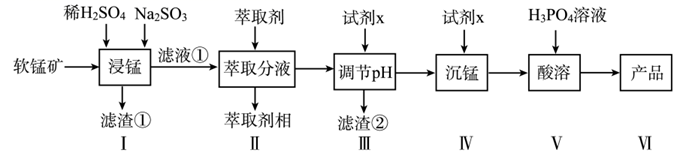
试回答下列问题:
-
(1) 滤渣①的主要成分是;浸锰时,FeO生成Fe3+的离子方程式为,适量的Na2SO3固体的作用是。
-
(2) 检验滤液①中是否含有Fe2+ , 除了用K3Fe(CN)6溶液外,还可以用试剂,若滤液①中含有Fe2+其现象是。
-
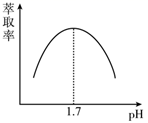
(3) 步骤II中,Fe3+的萃取率与pH的关系如图,如pH>1.7后,随pH增大,Fe3+萃取率下降的原因是。
-
(4) 试剂x为某种钠的正盐,从环保、经济角度,x最好为(写化学式);若c(Mn2+)=1.0 mol·L-1 , 调节pH范围应为(该条件下,Ksp[Al(OH)3]=1.0×10-33 , Ksp[Mn(OH)2]=1.0×10-14)。
-
(5) 步骤V酸溶时逐滴加入H3PO4溶液呈酸性才能保证生成物质较多为Mn(H2PO4)2·2H2O,试结合离子方程式说明原因。
-
(1) 实验室需要用到240mL0.5mol/L硫酸,现实验室只有物质的量浓度为1mol/L的硫酸,该同学需要自己稀释,他需要量取mL1mol/L的硫酸。
-
(2) 实验室某浓盐酸试剂瓶标签如下图所示,试根据标签上的有关数据回答下列问题:

该浓盐酸中HCl的物质的量浓度为。
-
(3) 某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol/L的Na2CO3溶液。溶液的配制过程如图所示:
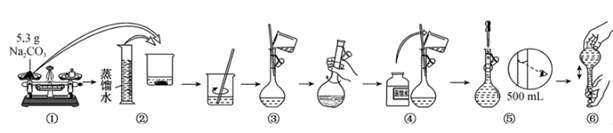
a.请把配制过程中两处明显不正确请改正过来、。
b.请分析下列情况对所配溶液浓度产生的影响:其中引起所配溶液浓度偏高的有(填序号)。
①用“左物右码”的方法称量(使用游码)
②碳酸钠不纯,其中混有氯化钠
③容量瓶未经干燥使用
④称量碳酸钠时所用砝码生锈
⑤移液过程中有少量溶液溅出
选项 | 实验目的 | 实验设计 |
A | 除去乙酸乙酯中的乙酸 | 加入饱和Na2CO3溶液,振荡后分液 |
B | 检验Na2SO3固体是否变质 | 取少量固体溶于水,加入硝酸酸化的Ba(NO3)2溶液,观察现象 |
C | 证明HClO的酸性比H2CO3的弱 | 用pH计测定NaClO溶液和Na2CO3溶液的pH,比较两溶液pH的大小 |
D | 配制100mL一定浓度的NaOH溶液 | 准确称取NaOH固体,放入100mL的容量瓶中,加水溶解,振荡摇匀,定容 |
- 下列物质的名称及其所对应的化学式均正确的是 A.乙酸乙脂:CH3COOCH2CH3 B.羟基:
- “你在桥上看风景/看风景的人在楼上看你/明月装饰了你的窗子/你装饰了别人的梦。”这是现代诗人卞之琳的《断章》中的诗句。其
- 为下面这段新闻拟一个标题,不超过10个字。(4分)明年起,江苏城镇居民特别是低收入群体、少年儿童、残疾人、低保户、无退休
- 下面对文学名著的点评不正确的一项是(3 分) A.《格列佛游记》是一部杰出的讽刺小说,作者用虚构的情节和幻想的手法,揭露
- (09吉林一中一模)关于细胞结构及其主要化学成分的叙述,错误的是 A.拟核和质粒的主要成分都是DNA
- 文中共有10处语言错误。每句中最多有两处。每处错误仅涉及一个单词的增加、删除或修改。格式错误不给分!!!
- 我国将加快百万千瓦级风电场的建设,同时建设甘肃河西走廊、沿海和内蒙古三个千万千瓦级风电基地,打造“风电三峡”。据此回答1
- 下列说法正确的是() A.任何状态下处于任何位置的物体都具有内能 B.机械能大的物体内能一定大 C.静止在地面上的物体无
- 某家用电能表上标有“220V 5A 3000r/KW·h”的字样,当家中用电器全部工作时, 电能表1min转45r,
- 从1L 1mol/LNaOH溶液中取出100mL,则这100mLNaOH溶液物质的量浓度是 mol/L,含
- 某物体由静止开始做直线运动,物体所受合力F随时间t的变化图象如图所示,则( ) A. 物体在2~4秒内做匀减速直线运
- 名著阅读与积累。(4分)(1)在鲁迅《朝花夕拾》的人物画廊里有纯朴善良的阿长,有严谨而热情的藤野先生,也有渴望革命又被迫
- 二氧化碳通入下列溶液中不发生反应的是( ) A.Na2CO3 B.Na2SiO3
- 右图是某种植物的叶肉细胞内以及细胞与外界环境的气体扩散或物质摄入情况,据图回答:([ ]里填字母,横线上填文字)(1)吸
- 下列说法中正确的是_____________ A.对物体做功不可能使物体的温度升高 B.即使
- 活中的一些事物,往往给人以理性的启迪。请你参考示例,在“钟表、天平、指南针”这几个事物中挑选两个,写两则事物的个人解读。
- 下列物质的变化过程中,有共价键明显被破坏的是( ) A.I2升华
- 一物体在几个力的共同作用下处于静止状态.现使其中向东的一个力F的值逐渐减小到零(其他力不变),又马上使其恢复到原值(方向
- 阅读下面的文字,根据上下文的提示,请补写出其中的空缺部分。要求:符合情境,简明得体。(4分) 有人曾问某位登山专家这样一
- 咽部发炎容易引起中耳炎,病菌由咽部到达中耳的结构是咽鼓管…………( )



