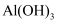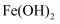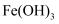第一章 从实验学化学 知识点题库
请填写下列空白:
-
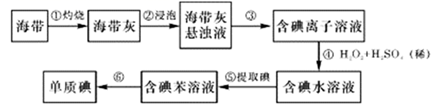
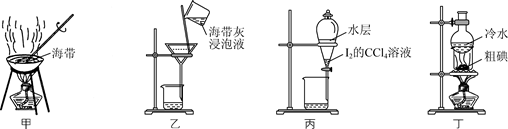
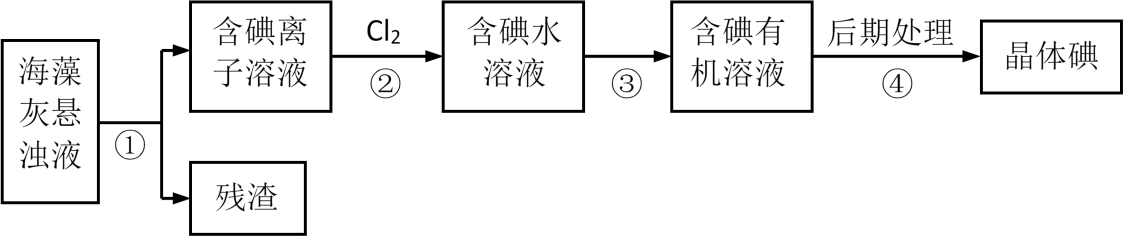
(1) 步骤③的操作名称是,碘离子在酸性环境中也能被氧气氧化,请写出相关离子方程式是。
-
(2) 步骤⑤中萃取剂也可用四氯化碳的理由是,该步骤所用主要玻璃仪器的名称是。
-
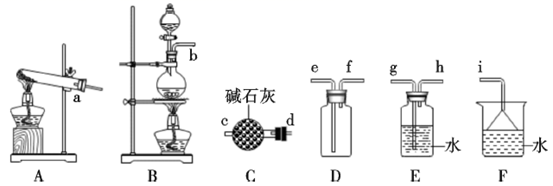
(1) 氨气的制备
①氨气的发生装置中反应的化学方程式为。装置C的仪器名称。
②欲收集一瓶干燥的氨气,选择上图中的装置,其接口连接顺序为a→(按气流方向,用小写字母表示)。
-
(2) 氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
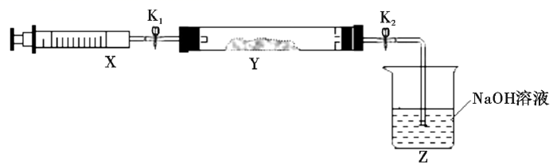
操作步骤
实验现象
解释原因
打开K1 , 推动注射器活塞,使X中的气体缓慢充入Y管中
①Y管中
②反应的化学方程式
将注射器活塞退回原处并固定,待装置恢复到室温
Y管中有少量水珠
生成的气态水凝聚
打开K2
③
④
 C . 标准状况下,22.4LNO与11.2LO2混合后气体的分子数为NA
D . 25℃,1LpH=9的CH3COONa溶液中,发生电离的水分子数为1×10-5NA
C . 标准状况下,22.4LNO与11.2LO2混合后气体的分子数为NA
D . 25℃,1LpH=9的CH3COONa溶液中,发生电离的水分子数为1×10-5NA
-
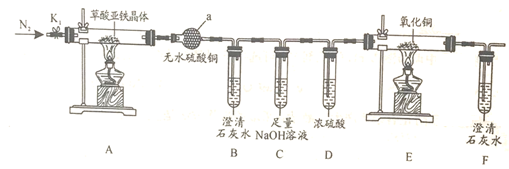
(1) 仪器a的名称是。
-
(2) 实验前先通入一段时间N2 , 其目的为。
-
(3) 实验证明了气体产物中含有CO,依据的实验现象为。
-
(4) 从绿色化学考虑,该套装置存在的明显缺陷是。
-
(5) 草酸亚铁晶体在空气易被氧化,请设计方案检验草酸亚铁晶体是否氧化变质。
 含有的质子数为2NA
B . 15g乙酸与甲酸甲酯的混合物中含氧原子总数为0.5NA
C . 2mol
含有的质子数为2NA
B . 15g乙酸与甲酸甲酯的混合物中含氧原子总数为0.5NA
C . 2mol  和1mol
和1mol  催化反应后分子总数为2NA
D . 物质的量均为1mol的
催化反应后分子总数为2NA
D . 物质的量均为1mol的  和
和 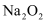 中所含阴离子数均为NA
中所含阴离子数均为NA
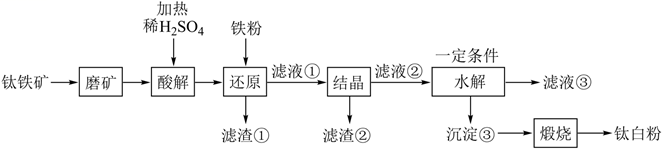 已知:①酸解后,钛主要以TiOSO4形式存在。强电解质TiOSO4在溶液中仅能电离出SO
已知:①酸解后,钛主要以TiOSO4形式存在。强电解质TiOSO4在溶液中仅能电离出SO  和一种阳离子。
和一种阳离子。
②H2TiO3不溶于水和稀酸。
-
(1) 磨矿的目的是。
-
(2) 滤渣①的主要成分是。
-
(3) 酸解过程中,写出FeTiO3发生反应的化学方程式。
-
(4) 还原过程中,加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某实验室做如下尝试。
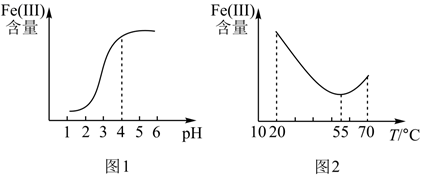
①在其它条件不变的情况下,体系中Fe(Ⅲ)含量随pH变化如图1,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:。
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图2,55℃后,Fe(Ⅲ)含量增大的原因是。
-
(5) 水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的化学式为。
②一定量Fe2+的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中Fe2+的含量。实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理。
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。 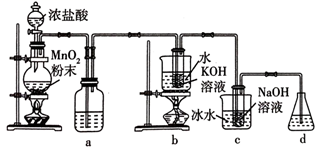
请回答下列问题:
-
(1) 盛放浓盐酸的仪器名称是,a的作用为。
-
(2) b中采用的加热方式的优点为,b中反应的化学方程式为。
-
(3) c中采用冰水浴冷却的目的是。
-
(4) d中可选用试剂___________(填标号)。A .
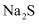 B . NaCl
C .
B . NaCl
C . 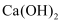 D .
D . 
-
(5) 反应结束后,取出b中试管,经冷却结晶,,洗涤,干燥,得到
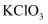 晶体。
晶体。
-
(6) 取少量
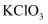 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入  振荡,静置后
振荡,静置后  层显色。可知该条件下NaClO的氧化能力
层显色。可知该条件下NaClO的氧化能力 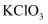 (填“大于”或“小于”)。
(填“大于”或“小于”)。
-
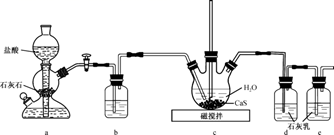
(1) 制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):
①装置a中反应发生的操作为 ;装置b中盛放的试剂是 。
②装置c中的长直导管的作用是。
-
(2) 制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是;该反应的化学方程式为。
-
(3) 探究硫脲的性质:①取少量硫脲溶于水并加热,验证有NH4SCN生成,可用的试剂是(填化学式,下同)
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为 。
③可用酸性KMnO4溶液滴定硫脲,已知MnO
 被还原为Mn2+ , CS(NH2)2被反应为CO2、N2及SO
被还原为Mn2+ , CS(NH2)2被反应为CO2、N2及SO  , 该反应中氧化剂与还原剂的物质的量之比为。
, 该反应中氧化剂与还原剂的物质的量之比为。
 回答下列问题:
回答下列问题:
-
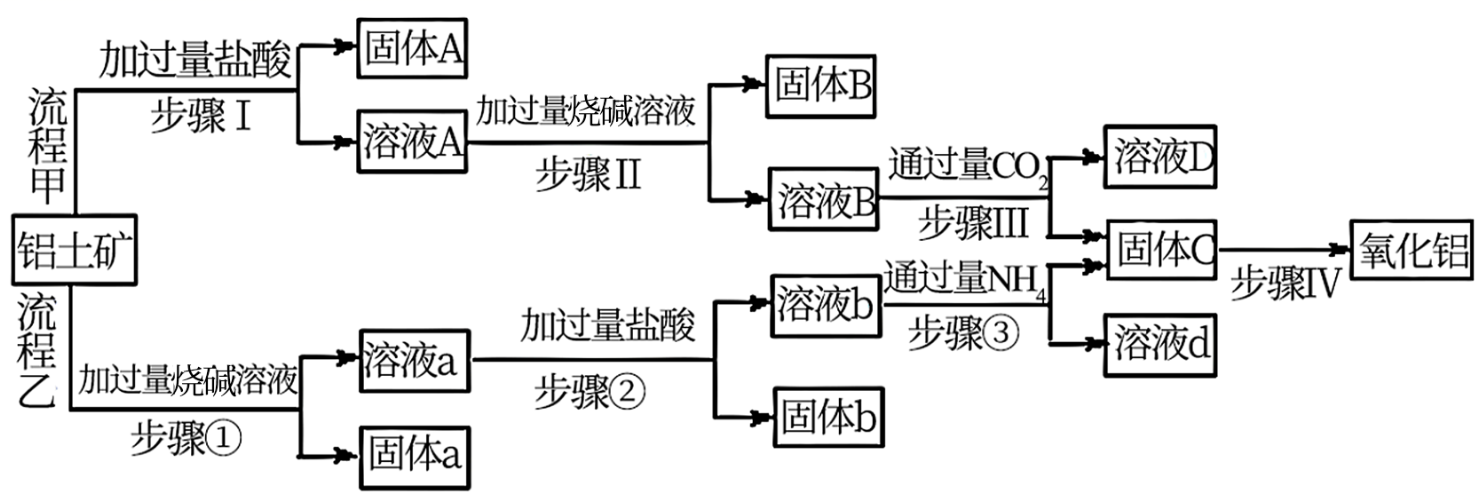
(1) 固体a的主要成分为(填化学式,下同),溶液A和溶液b中共同存在的溶质为。
-
(2) 能否将步骤Ⅱ中的烧碱溶液替换为氨水?请回答并简述理由。
-
(3) 步骤Ⅲ中发生反应的离子方程式为、;步骤②中Al元素发生反应的离子方程式为。
-
(4) 除步骤Ⅳ外,其余每个步骤都要采取的实验操作为。Al2O3、SiO2、MgO都可用于制造耐火坩埚,实验室熔融烧碱时可以选用(填标号)。
A.铁坩埚 B.氧化铝坩埚 C.石英坩埚 D.氧化镁坩埚
已知:金属离子沉淀的pH:
|
|
Fe3+ |
Fe2+ |
Mg2+ |
Mn2+ |
Co2+ |
|
开始沉淀时 |
1.5 |
6.3 |
8.9 |
8.2 |
7.4 |
|
完全沉淀时 |
2.8 |
8.3 |
10.9 |
10.2 |
9.4 |
-
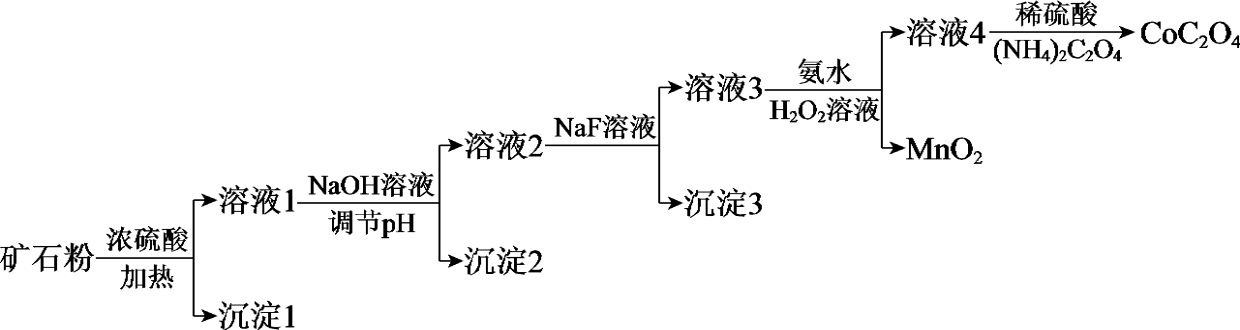
(1) Co2O3溶于浓硫酸,生成Co2+和一种可使带火星的木条复燃的气体,该气体是。
-
(2) 向溶液1中加入NaOH溶液,将Fe3+转化为Fe(OH)3沉淀,应调节pH至少大于。
-
(3) 向溶液2中加入NaF溶液,去除的离子是。
-
(4) 向溶液3中加入氨水和过氧化氢溶液,将Co2+转化为Co(NH3)63+。补充完整下列离子方程式:Co2++H2O2+ NH3-Co(NH3)63++ , 。
-
(5) 溶液4中,若将1 mol Co(NH3)63+全部转化为CoC2O4沉淀,需要消耗(NH4)2C2O4 mol。
-
(6) 关于上述流程,下列说法正确的是(填序号)。
a.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的CoC2O4
b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离
下列判断不正确的是( )
 的摩尔质量是18
B . 燃烧不一定需要氧气参与
C . 做焰色试验时可以用铁丝代替铂丝
D . 标准状况下,1mol空气的体积约为22.4L
的摩尔质量是18
B . 燃烧不一定需要氧气参与
C . 做焰色试验时可以用铁丝代替铂丝
D . 标准状况下,1mol空气的体积约为22.4L
回答下列问题:
-
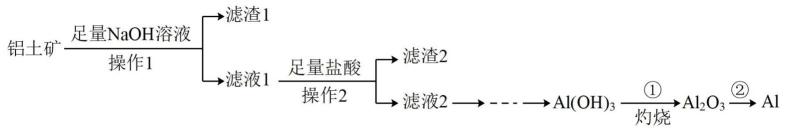
(1) 铝原子的结构示意图为。
-
(2) 冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,请写出铝与MnO2在高温下反应的化学方程式:。
-
(3) 第①步灼烧,在实验室进行时需要用到下列仪器中的____(填字母)。A . 蒸发皿 B . 烧杯 C . 酒精灯 D . 坩埚
-
(4) 第②步用电解法冶炼Al,化学反应方程式为。
-
(5) 滤渣1的成分为(填化学式),检验其中所含金属元素的化学方法是(写出实验操作步骤、现象和结论)。
 、
、 , 以及少量硅石和
, 以及少量硅石和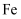 的氧化物,利用铝灰制备净水剂
的氧化物,利用铝灰制备净水剂 的工艺流程如图。
的工艺流程如图。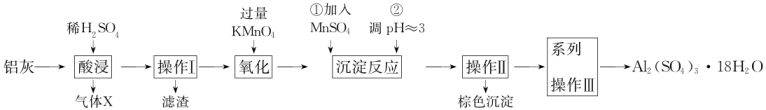
已知:金属离子浓度为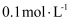 时生成氢氧化物沉淀的
时生成氢氧化物沉淀的
|
|
| |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
回答相关问题:
-
(1) 酸浸时为确保安全应注意,酸浸充分后溶液中的金属阳离子是。
-
(2) 操作I和II的名称是。
-
(3) 若无氧化步骤,对实验的影响是。
-
(4) 棕色沉淀含
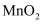 。操作①加入
。操作①加入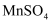 反应的离子方程式是,判断该反应完成的现象是。
反应的离子方程式是,判断该反应完成的现象是。
-
(5) 操作②调
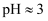 的原因是。
的原因是。
-
(6)
 可制作聚合硫酸铝(
可制作聚合硫酸铝(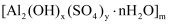 ),它是复合型高分子聚合物,净水效果优于传统的无机净水剂。若
),它是复合型高分子聚合物,净水效果优于传统的无机净水剂。若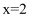 , 则
, 则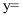 。引起聚合硫酸铝形态多变的基本成分是
。引起聚合硫酸铝形态多变的基本成分是 , 可用实验测定其含量。称取
, 可用实验测定其含量。称取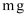 试样,将其移入锥形瓶中,用移液管加入
试样,将其移入锥形瓶中,用移液管加入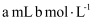 盐酸,充分溶解聚合物后,加
盐酸,充分溶解聚合物后,加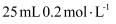 氟化钾溶液掩蔽掉全部铝离子,摇匀。加入3滴酚酞,用
氟化钾溶液掩蔽掉全部铝离子,摇匀。加入3滴酚酞,用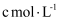 氢氧化钠标准溶液滴定至溶液呈微红色即为终点,消耗了标准液
氢氧化钠标准溶液滴定至溶液呈微红色即为终点,消耗了标准液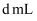 。则聚合硫酸铝中
。则聚合硫酸铝中 的质量分数为。
的质量分数为。
- 单项选择 在下列各题A、B、C、D四个选项中选择一个能填入题干空白处的最佳答案。 This pair of glasse
- There as on why Igave in is____if I didn’t. A.because
- 已知二次函数的图象如图所示,则满足 ( )A、a>0,b>0,c<0 B、a>0,b<
- 设NA代表阿伏加德罗常数,下列说法正确的是 ( )A. 2.7g金属铝变为铝离子
- 为了发展生产、改善生活,人们常引进一些外来物种,但有些外来物种会破坏当地的生态平衡,给当地造成生态灾难。这表明
- 与直线l : y=2x+3平行,且与圆x2+y2-2x-4y+4=0相切的直线方程是( ). A.x-y±=0
- 18. “他们不承认任何外界权威,不管这种权威是什么样的.宗教、自然观、社会、国家制度,一切都受到了最无情的批判.……以
- 水是生命之源,我们应该节约用水 (1)宏观上水是( )组成的,保持水的化学性质的最小微粒是( )。 (2)水是重
- 已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H=+74.9 kJ·mol-1,下列说法中正确的
- 贺知章《回乡偶书》中的“少小离家老大回,乡音无改鬓毛衰”的诗句反映了文化对人的影响的哪一特点?( ) A、文化对
- 基础知识;在下列各句的空白处填入一个适当的词,使句子意思完整、语法正确。 1. Please t______
- You are only allowed to take less than 30 kilograms of carry
- ①安安上小学了。半年之后,妈妈觉得他可以自己走回家,不必再接了,毕竟只 是十五分钟、拐三个弯的路程。 ②十五分钟过去了,
- 如图,已知AB=ED,BC=DF,AF=EC. 求证:(1)△ABC ≌△EDF; (2)BC∥DF.
- ____________。
- 下列填入文中括号内的语句,衔接最恰当的一项是()2020年,是中国名副其实的“航天大年”。在北斗
- 2008年5月12日,四川汶川发生了8.0级大地震。灾区人民、全国各族同胞,在战胜灾难、重建家园、团结互助中凝结成抗战精
- 斩木为兵,揭竿为旗,天下云集响应,__________________。(贾谊《过秦论》)
- 一串小彩灯,每个小彩灯规格为“4V 0.3A”,如图所示,在正常情况下,细金属丝由于表面氧化铜而与灯丝支架不导通,若加
- 晓强的一个朋友这样介绍自己的家乡:“我的家乡阳光斜射的很厉害,甚至有一段时间太阳总在地平线以下,气候终年寒冷。”晓强的这