第一章 从实验学化学 知识点题库
![]()
-
(1) 反应1中硫酸的作用是提供酸性环境,则试剂a的作用是。
-
(2) 试剂b应选择______(填序号)。A . CCl4 B . 苯 C . 酒精 D . 醋酸
-
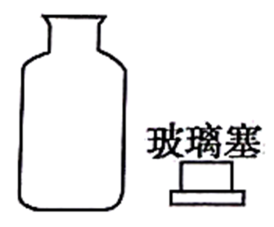
(3) 操作1的名称是。实验室里进行操作1需要的玻璃仪器除烧杯外,还需要。
-
(4) 反应2为:3I2+6NaOH=5NaI+NaIO3+3H2O,单线桥标出此反应电子转移。此反应氧化剂是,氧化产物是。
-
(5) 反应3的离子方程式是。
-
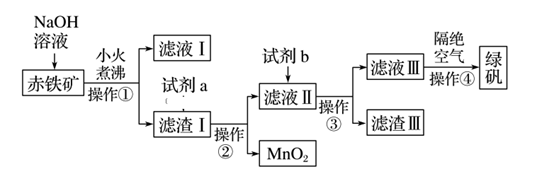
(1) 实验室中操作①的名称为。所需的玻璃仪器有烧杯、、。
-
(2) 氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为。
-
(3) 加入滤渣Ⅰ中的试剂a是,滤液Ⅱ中的主要金属阳离子有。
-
(4) 试剂b为。
-
(5) 滤渣Ⅲ中的主要成分是。操作④隔绝空气的目的是。
| | | | |
![]()
 +MnO2
+MnO2 
![]()
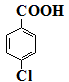
常温条件下的有关数据如下表所示:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
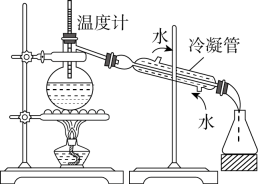
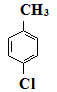
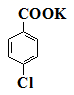
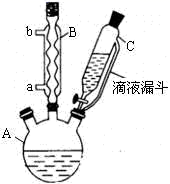
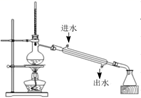
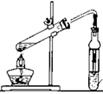
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g。
请回答下列问题:
-
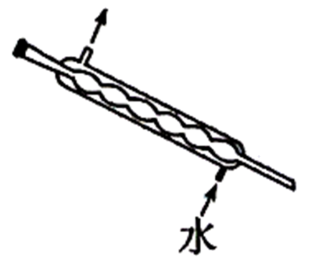
(1) 装置B的名称是,冷凝水由(选填“a”或者“b”)处通入。
-
(2) 量取6.00mL对氯甲苯应选用的仪器是____________。(填选仪器序号)A . 10mL量筒 B . 50mL容量瓶 C . 50mL酸式滴定管 D . 50mL碱式滴定管
-
(3) 控制温度为93℃左右的方法是。
-
(4) 第一次过滤的目的是。滤液中加入稀硫酸酸化,可观察到的实验现象是。
-
(5) 第二次过滤所得滤渣要用冷水进行洗涤,其原因是。
-
(6) 本实验的产率是(保留3位有效数字)。
-
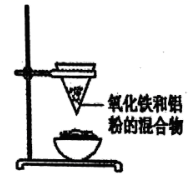
(1) 该实验中还缺;所缺实验用品的作用是;引发铝热反应的操作为。
-
(2) Al、Al2O3、 Fe、 Fe2O3熔点、沸点数据如下:
物质
Al
Al2O3
Fe
Fe2O3
熔点/℃
660
2054
1535
1462
沸点/℃
2467
2980
2750
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是, 当观察到时,说明熔融物中含有金属铝。
③实验室欲完全溶解该熔融物,常选用稀硫酸,而不用稀硝酸,其理由是。
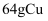 完全溶于适量浓硝酸中,收集到氮的氧化物(含
完全溶于适量浓硝酸中,收集到氮的氧化物(含 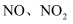 )的混合物,这些气体恰好能
)的混合物,这些气体恰好能 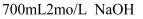 溶液完全吸收,生成只含
溶液完全吸收,生成只含 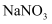 和
和 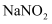 的盐溶液,其中
的盐溶液,其中 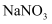 的物质的量为( )
的物质的量为( )
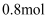 B .
B . 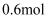 C .
C . 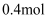 D .
D . 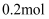
 制乙烯,应将温度计插入反应液中,迅速加热至140℃
D . 从海带灰中提取
制乙烯,应将温度计插入反应液中,迅速加热至140℃
D . 从海带灰中提取 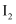 溶解→过滤→酸化→氧化→萃取→分液
溶解→过滤→酸化→氧化→萃取→分液
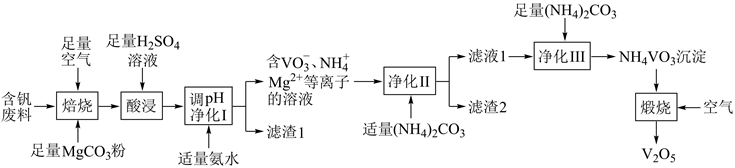 已知:含钒离子在溶液中的主要存在形式与溶液pH的关系:
已知:含钒离子在溶液中的主要存在形式与溶液pH的关系:
| 溶液pH | <4.0 | 6.0—8.0 | 8.0—10.0 |
| 钒元素主要存在形式 | | | |
请回答下列问题:
-
(1) 含钒废料中的有机物主要在工序中除去。
-
(2) “焙烧”产物之一是Mg(VO3)2 , 写出它在“酸浸”(溶液pH<2)过程中发生反应的化学方程式。
-
(3) 常温时,若“调pH净化I”工序中最终溶液pH=7,通过计算判断,此时Cu2+是否已经沉淀完全(已知离子浓度<1.0×10﹣5mol·L﹣1认为沉淀完全;Ksp[Cu(OH)2]=4.8×10﹣30)。
-
(4) “净化Ⅱ”时若加入过量的(NH4)2CO3 , 可能导致的后果为。
-
(5) “滤渣2”中含有Mg2(OH)2CO3 , 写出生成Mg2(OH)2CO3的离子方程式。
-
(6) “煅烧”时,除生成V2O5外,还生成了参与大气循环的气体,写出煅烧时的化学方程式。
-
(1) 合成该物质的步骤如下:
步骤1:配制0.5mol·L-1 MgSO4溶液和0.5mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三颈烧瓶中,开启搅拌器。温度控制在50℃。
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1h后,过滤,洗涤。
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
①步骤2控制温度在50℃,较好的加热方法是。
②步骤3生成MgCO3·nH2O沉淀的化学方程式为。
③步骤4检验沉淀是否洗涤干净的方法是。
-
(2) 测定生成的MgCO3·nH2O中的n值。
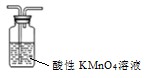
称量1.000碳酸镁晶须,放入如图所示的广口瓶中加入适量水,并滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后将烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。
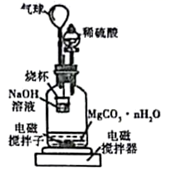
①图中气球的作用是。
②上述反应后期要升温到30℃,主要目的是。
③测得每7.8000g碳酸镁晶须产生标准状况下CO2为1.12L,则n值为。
-
(3) 碳酸镁晶须可由菱镁矿获得,为测定某菱镁矿(主要成分是碳酸镁,含少量碳酸亚铁、二氧化硅)中铁的含量,在实验室分别称取12.5g菱镁矿样品溶于过量的稀硫酸并完全转移到锥形瓶中,加入指示剂,用0.010mol/L H2O2溶液进行滴定。平行测定四组。消耗H2O2溶液的体积数据如表所示。
实验编号
1
2
3
4
消耗H2O2溶液体积/mL
15.00
15.02
15.62
14.98
①H2O2溶液应装在(填“酸式”或“碱式”)滴定管中。
②根据表中数据,可计算出菱镁矿中铁元素的质量分数为 %(保留小数点后两位)。
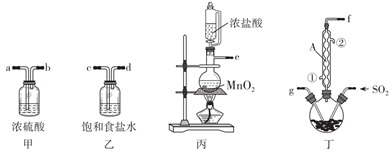
 是一种重要的有机合成试剂。
是一种重要的有机合成试剂。  的熔点为
的熔点为 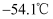 ,沸点为69.1℃。它在常温下较稳定,遇水剧烈水解,100℃以上易分解。实验室可利用
,沸点为69.1℃。它在常温下较稳定,遇水剧烈水解,100℃以上易分解。实验室可利用  和
和  在活性炭催化下反应制取少量
在活性炭催化下反应制取少量  ,装置如图(部分夹持裝置已省略)。
,装置如图(部分夹持裝置已省略)。 已知:  。请回答:
。请回答:
-
(1) 仪器A的名称是,冷凝水应从(填“①”或“②”)口通入。
-
(2) 实验前,检查丙装置气密性的方法是。
-
(3) 装置丙中发生反应的化学方程式为,上述仪器正确的连接顺序是
 (填仪器接口字母编号)。
(填仪器接口字母编号)。
-
(4) 为提高本实验中磺酰氯的产率,在实验操作中需要注意的事项有(填序号)。
①实验开始时先通气体,再通冷凝水
②控制气流速率,不宜过快
③可给三颈烧瓶适当降温
-
(5) 该实验装置存在的不足之处是(写出一点即可)。
| 选项 | 物质(杂质) | 方法 |
| A | | 在氧气流中灼烧 |
| B | | 加热升华 |
| C | HCl气体( | 通过KI溶液 |
| D | | 加入盐酸溶解、过滤、洗涤及干燥 |
-
(1) I.金属及其化合物在生产生活中有着广泛的应用。
小苏打可用于治疗胃酸过多,请写出对应的化学方程式;(填“能”或“不能”)用氢氧化钠溶液代替。
-
(2) 将
 与稀硫酸混合,二者不能反应,滴入
与稀硫酸混合,二者不能反应,滴入 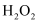 后,溶液很快变成蓝色,该反应的化学方程式为。
后,溶液很快变成蓝色,该反应的化学方程式为。
-
(3)
 是一种酸式盐,写出
是一种酸式盐,写出  在水中的电离方程式:。
在水中的电离方程式:。
-
(4) Ⅱ.物质的量是学习化学的基础。
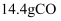 和
和  的混合气体在标准状况下所占的体积为
的混合气体在标准状况下所占的体积为 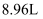 ,其中
,其中  的质量为。
的质量为。 -
(5)
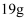 某二价金属的氯化物
某二价金属的氯化物  中含有
中含有 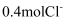 ,金属A的相对原子质量是。
,金属A的相对原子质量是。
-
(6) 根据反应
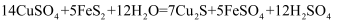 ,可知当有
,可知当有 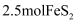 参加反应时,被氧化的硫元素的物质的量为
参加反应时,被氧化的硫元素的物质的量为 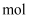 。
。
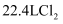 (标准状况)与水充分反应转移
(标准状况)与水充分反应转移 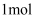 电子
B .
电子
B . 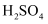 和
和 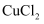 均可通过化合反应得到
C . 将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D .
均可通过化合反应得到
C . 将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D .  与
与 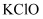 溶液反应:
溶液反应: 
选项 | 物质(括号内为杂质) | 除杂试剂 | 分离方法 |
A |
|
| 加热 |
B |
| 饱和 | 洗气 |
C |
| 盐酸 | 过滤 |
D |
| 饱和食盐水 | 洗气 |

已知:ⅰ.GeO2与碱反应生成Na2GeO3.ⅱ.GeCl4极易水解,GeCl4沸点86.6℃。
ⅲ.As位于同主族P的下一周期,As2O3+2NaOH = 2NaAsO2+H2O。
-
(1) Ge位于同主族Si的下一周期,则Ge在周期表中的位置是。
-
(2) 从原子结构角度解释Ge和Si金属性递变的原因。
-
(3) “氧化”过程是将NaAsO2氧化为Na3AsO4 , 其离子方程式为。
-
(4) 加盐酸蒸馏生成GeCl4 , 反应的化学方程式为。
-
(5) 高纯二氧化锗的含量采用碘酸钾滴定法进行测定。称取ag高纯二氧化锗样品,加入氢氧化钠在电炉溶解,用次亚磷酸钠还原为Ge2+ , 以淀粉为指示剂,用bmol/L的碘酸钾标准溶液滴定,消耗碘酸钾的体积为V mL。(20℃以下,次亚磷酸钠不会被碘酸钾和碘氧化)
资料:3Ge2++IO
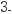 +6H+ = 3Ge4++I-+3H2O,IO
+6H+ = 3Ge4++I-+3H2O,IO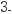 +5I-+6H+ = 3I2+3H2O。
+5I-+6H+ = 3I2+3H2O。此样品中二氧化锗的质量分数是(用表达式表示)。
A | B | C | D |
盛装 | 钠在空气中加热 | 准确量取一定体积 | 蒸馏用冷凝管 |
|
|
|
|
A | B | C | D |
|
|
|
|
分离苯和甲苯 | 验证乙酸酸性强于苯酚 | 制备溴苯 | 制备并检验乙炔 |
- 数据26000用科学记数法表示为2.6×10n,则n的值是( )A. 2 B.3
- 有机化合物A经李比希法测得其中含碳 64.3 %、含氢7.1 %,其余为氧。经质谱法分析得知其相对分子质量为56,经核磁
- A、B、C、D四种有机物分子中碳原子数相同,A为气态,标况下的密度为1.16 g・-1 ;B或D跟溴化氢反应都生成C ;
- 下列对右图的认识,正确的是()①反映了战国时期农业发展的状况 ②这种牛耕方式被称为“二牛抬杠”的耦犁 ③图中的犁是在当时
- 如图,甲电路可测出电压表内阻,已知电源内阻忽略不计,R为变阻箱,其取不同值时电压表示也变化,图象如图乙,则电压表内阻Rv
- 下列高分子化合物是由两种单体通过加聚或缩聚反应而合成得到的是( )
- 据不完全统计,西藏现有60余座学经班,学经僧人约6000人。活佛转世作为藏传佛教特有的传承方式得到国家尊重。20世纪80
- 人间四月芬芳菲,春天校园百花开,阵阵花香,沁人心脾。花香四溢的现象说明 A.分子是由原子组成的
- 2008年我国城乡收入差距由2007年的3.33:1扩大到3.36:1,绝对差距首次超1万元。这一现象①降低社会总体消费
- 已知氨基酸的平均分子量为128,有100个氨基酸形成3条肽链的蛋白质,分子量约为() A.12800 B.1
- 锤头松了,用手抓住锤头在地上把锤柄用力碰几下,锤头就会紧套在锤柄上,这是为什么?
- 如图4-3-7所示,用相同的均匀导线制成的两个圆环a和b,已知b的半径是a的两倍.若在a内存在着随时间均匀变化的磁场,b
- “劝君更尽一杯酒,西出阳关无故人”。王维诗中的“君”将前往 A.西域都护府辖区 B.安
- 写出下列离子方程式: (1)Na3PO4水解的离子方程式
- 下列类型的反应中,一定发生电子转移的是 A. 化合反应 B.分解反应 C. 置换反应 D. 复分
- -- Why have you bought so much food? -- My good friends ___
- The judge ordered that the stranger______all the loss of the
- 在食盐中加入碘酸钾(KIO3)可以补充碘元素,碘酸钾中碘元素的化合价为( ) A.+1
- 在0.10mol·L-1NH3·H2O溶液中,加入少量NH4Cl晶体后,引起的变化是 A.NH3·H2O的电离程度减小B
- 静止的弹簧秤两端同时受到大小都为4N的力F1,F2 的作用,则弹簧秤的示数为A.0 B.4N
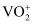

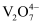
 (炭粉)
(炭粉)


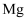 粉
粉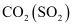
 溶液
溶液
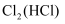
 溶液
溶液 标准溶液
标准溶液