第一章 从实验学化学 知识点题库
 B .
B . 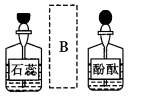 C .
C . 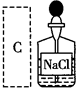 D .
D . 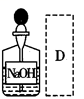
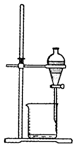 C .
C . 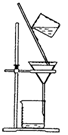 D .
D . 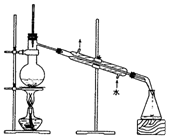
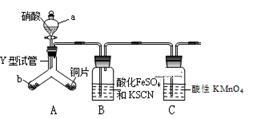
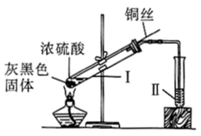
已知:FeSO4+NO  [Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
-
(1) 实验前需检验装置的气密性,简述操作。
-
(2) 仪器a的名称
-
(3) 实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是;
-
(4) 证明有NO2的实验现象
-
(5) 装置C的作用,反应离子方程式。
-
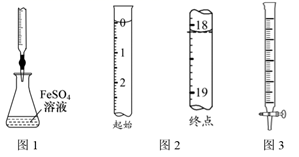
(6) 测定化学试剂绿矾(FeSO4·7H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4 , 用0.1000molL-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。KMnO4溶液盛放在棕色式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度。

-
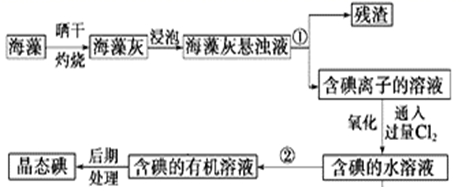
(1) 指出提取碘的过程中有关实验操作①和②的名称:;。
-
(2) 在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是图中的(注:试管中深色区为有色溶液),上层无色溶液的溶质是:,下层颜色是。
-
(3) 含碘离子的溶液中通入过量的Cl2发生的离子方程式为。
-
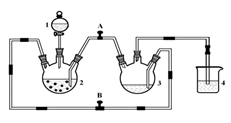
(1) 本实验中为制得氢氧化亚铁如何保证无氧条件。
-
(2) 在将硫酸亚铁压入制得氢氧化亚铁的操作之前必须要进行的操作是。
请回答下列问题:
-
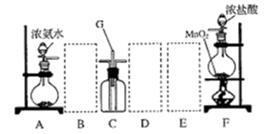
(1) 装置 F 中发生反应的离子方程式是。
-
(2) 装置 A 中的烧瓶内固体可选用(选填以下选项的代号)。
A 碱石灰 B 浓硫酸 C 生石灰 D 五氧化二磷 E 烧碱
-
(3) 虚线框内应添加必要的除杂装置,请从图的备选装置中选择,并将编号填入下列空格:
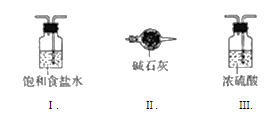
BDE
-
(4) 氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为: ;装置 C 内出现浓厚的白烟,该物质化学式为。
-
(5) 若从装置 C 中 G 处逸出的尾气中含有 N2 和少量 Cl2 , 应如何处理。
 为白色,难溶于水的固体,在电子工业中有泛应用。一种由天青石精矿(含
为白色,难溶于水的固体,在电子工业中有泛应用。一种由天青石精矿(含 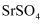 )制备高纯
)制备高纯 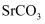 的方法如下:
的方法如下: 天青石精矿  粗
粗 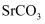
 含
含 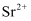 溶液
溶液  高纯
高纯 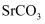
已知:
ⅰ. 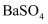 、
、 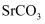 、
、 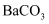 和
和 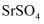 均难溶于水,在相同温度下的溶解度
均难溶于水,在相同温度下的溶解度 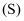 关系如下:
关系如下:
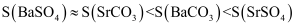
ⅱ.几种氢氧化物在不同温度下的溶解度:
| | 20 | 40 | 60 | 80 | 90 | 100 |
| | 1.77 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
| | 3.89 | 8.22 | 20.94 | 101.4 | - | - |
| | 0.173 | 0.141 | 0.121 | 0.094 | 0.086 | 0.076 |
-
(1) 粗
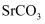 的制取
的制取 ①碳化剂一般选择
 溶液或
溶液或  溶液。写出
溶液。写出 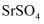 转化为
转化为 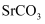 的离子方程式:。
的离子方程式:。②实验发现,当温度和碳化剂的物质的量浓度均相同时,
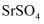 在
在  溶液中的转化速率大于在
溶液中的转化速率大于在  溶液中的。从盐类水解的角度解释其原因是。
溶液中的。从盐类水解的角度解释其原因是。 -
(2) 含
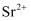 溶液的精制
溶液的精制 ⅰ.将粗
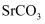 溶解于适量盐酸中,过滤得到滤液(金属阳离子有:
溶解于适量盐酸中,过滤得到滤液(金属阳离子有: 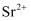 、
、  、
、  和
和  );
);ⅱ.加
 溶液调节上述滤液
溶液调节上述滤液  至12~13.过滤得到滤液X和滤渣A;
至12~13.过滤得到滤液X和滤渣A;ⅲ.将滤液X置于90~95℃的水浴中加热,生成白色沉淀B,趁热过滤弃去沉淀,得到滤液Y,并将ⅱ中的滤渣A重新投入滤液Y中浸泡(保持温度为90~95℃);
ⅳ.重复ⅱ和ⅲ3~4次,最后得到热的滤液Z;
ⅴ.趁热向滤液Z中加入适量稀硫酸,过滤得到精制含
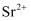 溶液。
溶液。①滤渣A中含有
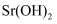 和。
和。②白色沉淀B的主要成分是。
③ⅳ的目的是。
④ⅴ中反应的离子方程式是。
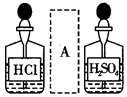
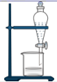
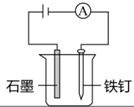
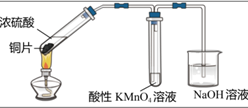
| A | B | C | D |
| | | | |
| 分离乙醇与乙酸 | 模拟外加电流的阴极保护法 | 证明 | 证明乙炔可使溴水褪色 |
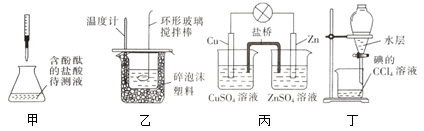
 萃取碘水中的碘的分离操作
萃取碘水中的碘的分离操作
| 目的 | 分离方法 | 原理 | |
| A | 分离水和乙醇 | 蒸馏 | 水和乙醇的沸点不同 |
| B | 分离溶于水中的碘单质 | 四氯化碳萃取 | 碘单质在四氯化碳中的溶解度远大于在水中的溶解度,四氯化碳难溶于水 |
| C | 除去CO2中少量HCl气体 | 通入足量NaHCO3溶液中洗气 | HCl会与NaHCO3溶液反应且产生更多CO2 |
| D | 除去NaCl固体中混有的少量KNO3杂质 | 加水溶解配成热的浓溶液,冷却结晶,过滤 | NaCl和KNO3溶解度随温度变化有较大差异 |
 、Cl-、NO
、Cl-、NO  。回答下列问题:
。回答下列问题:
-
(1) 下列离子中,能大量存在于该废水中的是_______(填标号)A . Ag+ B . Mg2+ C . OH- D . HCO

-
(2) 取100mL该废水于烧杯,逐滴加入NaOH溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是Na+、(用离子符号表示)。
-
(3) 某化学社团小组成员欲除去废水样品中的Cu2+和SO
 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图: 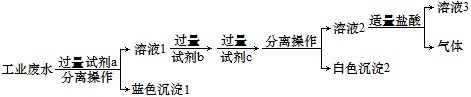
①试剂c为(写化学式);溶液3所含溶质离子有Cl-、。
②“分离操作”的名称是,需用到的玻璃仪器主要有。
③向“白色沉淀2”中加入足量盐酸,发生反应的离子方程式为。
-
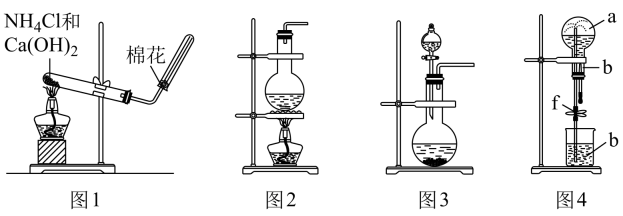
(1) 请写出图1实验室制取氨气的化学方程式。
-
(2) 用图1的装置为什么不能直接加热分解
 制取氨气?
制取氨气?
-
(3) 实验室若采用浓氨水和
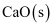 作用制取氨气,则选择的装置是(选填"图2"或"图3")。
作用制取氨气,则选择的装置是(选填"图2"或"图3")。
-
(4) 图4为探究气体溶解性的喷泉实验,圆底烧瓶收集满某易溶于水的气体A进行喷泉实验,若气体A全部被吸收,则所得溶液物质的量浓度为mol/L(可以分数表示或保留两位有效数字)。
-
(5) 现有
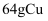 完全溶于适量的浓硝酸中,生成氮的氧化物的混合物(含
完全溶于适量的浓硝酸中,生成氮的氧化物的混合物(含 )共
)共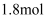 , 这些气体恰好能被
, 这些气体恰好能被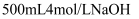 溶液完全吸收,生成只含
溶液完全吸收,生成只含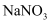 和
和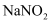 的盐溶液,其中
的盐溶液,其中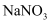 的物质的量为。
的物质的量为。
-
(1) 在一支试管中加入1mLNa2S溶液,向其中边振荡边滴加H2SO3溶液,用浸NaOH溶液的棉团塞住试管口,可能观察到现象为,试管中发生反应化学方程式。
氧钒(IV)碱式碳酸铵晶体的化学式为(NH4)5[(VO)6(CO3)4(OH)9]·10H2O,难溶于水,是制备热敏材料VO2的原料。实验室以V2O5为原料合成该晶体的流程如图。
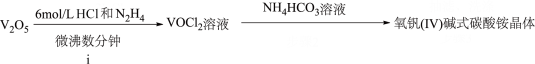
已知:+4价钒在弱酸性条件下具有还原性。
-
(2) N2H4的电子式为,只用浓盐酸与V2O5反应也能制备VOCl2溶液,但从环保角度分析,该反应不被推广的主要原因是(用化学方程式表示)。
-
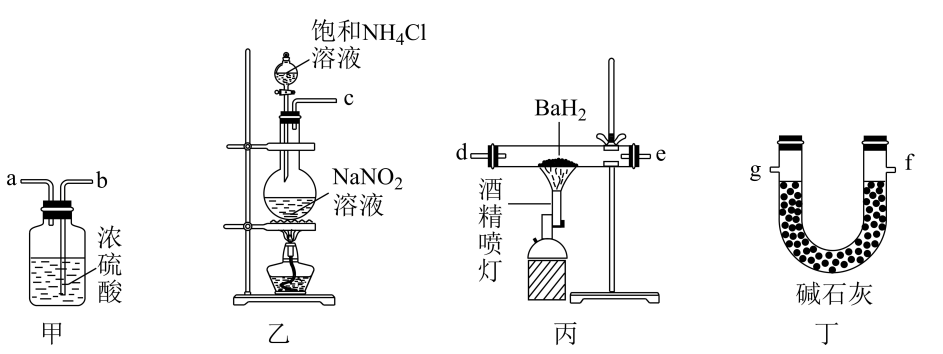
(3) 步骤ii可在如图装置中进行。
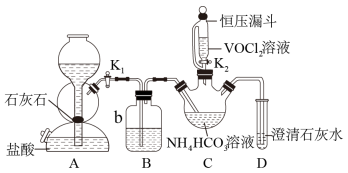
①仪器b的名称是,盛装的试剂是。
②实验时,先关闭K2 , 打开K1 , 当观察到D中出现白色浑浊时,再关闭K1 , 打开K2 , 这样操作的目的是。
③反应结束后,得到紫红色晶体,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次。检验用饱和NH4HCO3溶液洗涤沉淀是否干净的操作是。
-
(4) 称量ag粗产品,用KMnO4溶液氧化,再除去多余的KMnO4(方法略),最后用0.1mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(滴定过程只发生反应
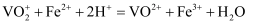 ),消耗标准溶液的体积为bmL。
),消耗标准溶液的体积为bmL。①粗产品中钒的质量分数为%(用含有a、b的式子表示)。
②若实验测得钒的质量分数偏大,则可能的原因是。
A.(NH4)Fe(SO4)标准溶液被氧化
B.滴定前平视读数,滴定终点时仰视读数
C.滴定前,滴定管内无气泡,滴定结束后尖嘴有气泡
- 如图所示的电路中,电源电压恒定不变,当电键K闭合时:A.伏特表示数变小,安培表示数变小,灯变暗;B.伏特表示数变大,安培
- 下列各项中字音不正确的一项是:( ) A.洞悉 佐证 思辨 画幅 B.撮合 篇什 颦蹙 抗
- 科学家根据元素周期律和原子结构理论预测,原子序数为114的元素属于第七周期Ⅳ A族,称为类铅元素。下面关于它的原子结构和
- 下列各组物质中,肯定全都属于纯净物的是 A.液氯和氯水 B.漂白粉和乙醇 C
- 在平面直角坐标系中,点P (3, -2)在----------------------()
- 阅读下面的文字,把文中拼音所代表的汉字和加点字的注音依次分类写在方框内。(2分) 常州篦箕巷,沿运河而建,自古就是商lǚ
- 在抗击“H1N1甲型流感”的日子里,人们体验了传统中医的神威。为中医临床医学奠定基础的著作是( ) A.《黄帝
- “可燃冰”是天然气水合物,下列有关说法错误的的是( ) A.可燃冰是一种洁净的新能源 B.可燃冰的主要成分是C
- 阅读下面的文章,完成后面的问题。 你就是自己的奇迹 姜钦峰 他是个阳光帅气的小伙子,一头飘逸的长发,再加上一副墨镜,
- 武汉是汇聚南腔北调的大都市,由于社会交往的需要和学校教学用语的影响,使得许多武汉孩子更喜欢说普通话。但是,武汉方言仍然富
- 下面这段话有三处错误,请指出来并加以改正。(6分) ①中华人民共和国第十届运动会10月12日隆重在江苏南京开幕。
- 小红同学将自己5月份的各项消费情况制作成扇形统计图(如图),从图中可看出( ) (A)各项消费金额占消费总金额的
- 右图为三个处于分裂期细胞的示意图,下列叙述中正确的是 A.三个细胞可能的分裂顺序是乙、丙、甲 B.三个细胞有可能来自同一
- 移栽植物时,常摘掉几个大叶片,目的是减少植物的() A.蒸腾作用 B.光合作用 C.呼吸作用 D.吸收作用
- —Tom wants toknow if you will have a picnic tomorrow. —Yes.
- ......
- 下列标点符号使用正确的一项是(3分) ( ) A.迎面走来一个七、八岁的红领巾,手里捧着鲜花,不知是要献给
- 在宏观、微观和符号之间建立联系是化学学科的特点. (1)氯化钠、汞、氢气三种物质中,由离子构成的是 (写化学式) (2)
- 将1、、、按右侧方式排列.若规定(m,n)表示第m排从左向右第n个数,则(5,4)与(15,7)表示的两数之积是

 有漂白性
有漂白性


