第一章 从实验学化学 知识点题库
下列实验操作中错误的是( )
A . 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B . 称量NaOH时,称量物放在称量纸上,置于托盘天平的左盘中
C . 过滤时,漏斗下端紧贴烧杯内壁
D . 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处
下列说法错误的是( )
A . 葡萄酒中SO2的检测可用酸性KMnO4溶液滴定葡萄酒试样进行测定
B . 改燃煤为燃气,可以减少废气中SO2等有害物质的排放量,是治理“雾霾”等灾害天气的一种措施
C . 实验室保存少量液溴时常加少量水液封,并用玻璃塞密封,不能用橡胶塞
D . 水玻璃是混合物,可用于生产黏合剂(矿物胶),做耐火阻燃材料
某酸溶液的pH=1,此酸溶液的物质的量浓度( )
A . 0.1 mol·L-1
B . 一定大于0.1 mol·L-1
C . 若为强酸一定等于0.1 mol·L-1 , 若为弱酸一定大于0.1 mol·L-1
D . 若为强酸一定≤0.1 mol·L-1 , 若为弱酸一定>0.1 mol·L-1
下列叙述正确的是( )
A . 10mL质量分数为98%的H2SO4 , 用10mL水稀释后,H2SO4的质量分数等于49%
B . 配制0.1mol/L的Na2CO3溶液190mL,需用200mL容量瓶
C . 将40克NaOH溶于1L水中,得到1mol/L的溶液
D . 常温常压下11.2LCl2含原子数小于NA
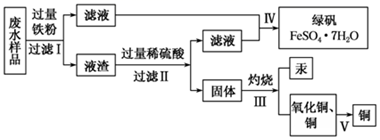
工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
-
(1) 步骤Ⅰ中加入过量铁粉的目的是。
-
(2) 步骤Ⅱ中(填“能”或“不能”),用盐酸代替硫酸,写出步骤Ⅱ中涉及反应的化学方程式:。
-
(3) 步骤Ⅳ得到绿矾的操作蒸发浓缩、、洗涤、干燥。现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是。
-
(4) 步骤 V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。从安全角度考虑,方案不好;从产品纯度考虑,方案不好。
下列有关使用托盘天平的叙述,错误的是( )
①称量前先调节托盘天平的零点;②称量时左盘放被称量物,右盘放砝码;③潮湿的或有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量; ④用托盘天平可以准确称量5.85g的固体食盐;⑤称完,应把砝码放回砝码盒中。
A . ②③
B . ②④
C . ③④
D . ③
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A . 等物质的量的CO和  所含分子数为
所含分子数为  B .
B . 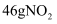 和
和  的混合物中含有的原子总数一定是
的混合物中含有的原子总数一定是 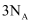 C . 在标准状况下,
C . 在标准状况下,  个任何分子所占的体积约为
个任何分子所占的体积约为 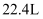 D .
D . 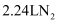 和
和  的混合气体所含原子数为
的混合气体所含原子数为 
 所含分子数为
所含分子数为  B .
B . 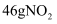 和
和  的混合物中含有的原子总数一定是
的混合物中含有的原子总数一定是 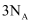 C . 在标准状况下,
C . 在标准状况下,  个任何分子所占的体积约为
个任何分子所占的体积约为 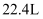 D .
D . 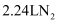 和
和  的混合气体所含原子数为
的混合气体所含原子数为 
《本草纲目》中“烧酒”条目写道:“自元时始创其法,用浓酒和糟人甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”文中所用之“法”是指 ( )
A . 蒸馏
B . 渗析
C . 萃取
D . 过滤
下列是学生课外实践活动的实验设计,其中不能达到们应的实验目的的是( )
| 选项 | 实验目的 | 实验设计 |
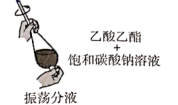
| A | 除去乙酸乙酯中的乙酸 | |
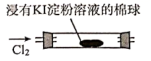
| B | 证明氧化性:Cl2>I2 | |
| C | 用NaOH标准溶液滴定某稀盐酸 | |
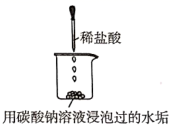
| D | 探究锅炉里的水垢样品在酸中的溶解 | |
A . A
B . B
C . C
D . D
将1 mL 0.1mol/L的硫酸加入纯水中制成200 mL溶液,稀释后硫酸中c(H+)水为( )
A . 1×10-13mol/L
B . 1×10-3mol/L
C . 1×10-7mol/L
D . 1×10-11mol/L
下列说法错误的是( )
A . 用铜丝燃烧法可定性确定有机物中是否存在卤素
B . 海水中碘的含量可达8×1010t,目前工业上直接用海水提取碘
C . 1828年,德国化学家维勒在制备无机盐氰酸铵时得到了一种结晶物尿素
D . 苯酚与水形成的油液静置后会分层,上层是溶有苯酚的水层,下层是溶有水的苯酚层。当温度高于65℃时,苯酚能与水以任意比例互溶
-
(1) I.由三种短周期元素组成的化合物A,按如下流程进行实验。已知相同条件下气态A物质的密度为氢气密度的49.5倍。
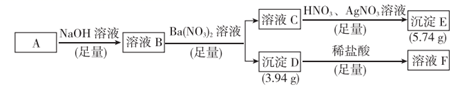
请回答:
组成A的三种元素为,A的化学式为。
-
(2) A与足量NaOH溶液反应的化学方程式为。
-
(3) A与足量氨气在一定条件下可以反应生成2种常见的氮肥,该反应的化学方程式为。
-
(4) II.某兴趣小组利用废铜屑制备硫酸铜晶体,装置如图所示(夹持装置和加热装置已略去),在实验中将适量硝酸逐滴加入到废铜屑与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶,制得硫酸铜晶体。
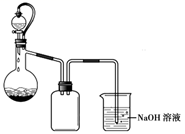
将硝酸逐滴加入到废铜屑与稀硫酸的混合物中的目的是。
-
(5) 实验过程中盛有NaOH溶液的烧杯上方仍然出现了红棕色气体,请对该实验装置提出改进意见:。
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下。下列说法错误的是( )
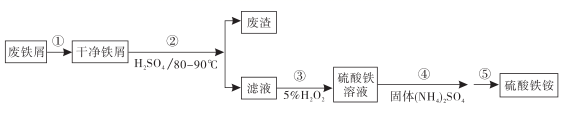
A . 步骤①的目的是去除废铁屑表面的油污,方法是碱煮水洗
B . 步骤②需要温度保持80-95 ℃,采用的合适加热方式是热水浴
C . 步骤③中分批加入过量H2O2 , 同时溶液要保持pH小于0.5的原因是为了不引入杂质和防止Fe2+水解
D . 步骤⑤的具体实验操作有加热浓缩、冷却结晶、过滤(洗涤),经干燥得到硫酸铁铵晶体样品
下列物质分离(括号内的物质为杂质)方法正确的是( )
A . 溴苯(Br2)—— 分液
B . 乙酸丁酯(正丁醇 )—— 过滤
C . 乙酸乙酯(乙酸)—— 蒸馏
D . 氯化铵(I2)—— 加热
图是某元素M的价类二维图,其中X是一种强碱,A为正盐,通常条件下Z是无色液体,D的相对分子质量比E小16,图中呈现了各物质的转化关系。下列说法正确的是( )
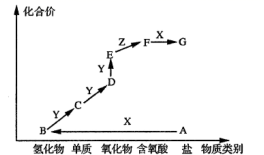
A . A中只含有离子键
B . B物质可以和Y反应直接转化为E
C . D,E均可以用向上排空气法收集
D . 通过氢氧化钠溶液可以除去D中含有的少量E
黄铁矿(主要成分  )是工业制硫酸的主要原料,在空气中煅烧黄铁矿,生成
)是工业制硫酸的主要原料,在空气中煅烧黄铁矿,生成  和
和  气体。某化学学习小组设计了如下实验,通过测量生成
气体。某化学学习小组设计了如下实验,通过测量生成  的质量来测定黄铁矿的纯度,根据要求回答下列问题。
的质量来测定黄铁矿的纯度,根据要求回答下列问题。
 )是工业制硫酸的主要原料,在空气中煅烧黄铁矿,生成
)是工业制硫酸的主要原料,在空气中煅烧黄铁矿,生成  和
和  气体。某化学学习小组设计了如下实验,通过测量生成
气体。某化学学习小组设计了如下实验,通过测量生成  的质量来测定黄铁矿的纯度,根据要求回答下列问题。
的质量来测定黄铁矿的纯度,根据要求回答下列问题。 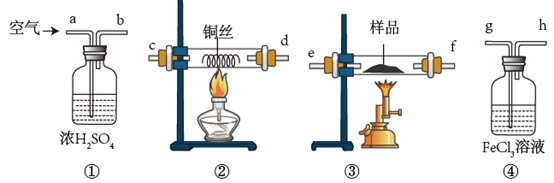
-
(1) 用各装置接口字母表示气流从左到右的顺序。
-
(2) 将样品研磨成粉末状再反应的目的是。
-
(3) 装置③中煅烧时发生反应的化学方程式为。
-
(4) 装置②中铜网的作用是。
-
(5) 反应结束后,关闭③处酒精喷灯仍需通一段时间的空气,其目的是。
-
(6) 写出装置④中发生反应的离子方程式。
-
(7) 该小组取8.0g样品进行实验,实验后装置④增重6.4g,则该样品纯度为。
现有硫酸钠溶液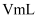 , 它的密度是
, 它的密度是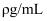 , 其中钠离子的质量分数是
, 其中钠离子的质量分数是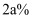 , 则有关该溶液的说法错误的是( )
, 则有关该溶液的说法错误的是( )
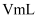 , 它的密度是
, 它的密度是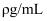 , 其中钠离子的质量分数是
, 其中钠离子的质量分数是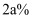 , 则有关该溶液的说法错误的是( )
, 则有关该溶液的说法错误的是( )
A . 硫酸钠的物质的量浓度是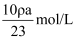 B . 溶质的质量分数是
B . 溶质的质量分数是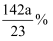 C . 溶质和溶剂的物质的量之比是
C . 溶质和溶剂的物质的量之比是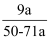 D . 硫酸根离子的质量分数是
D . 硫酸根离子的质量分数是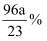
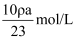 B . 溶质的质量分数是
B . 溶质的质量分数是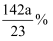 C . 溶质和溶剂的物质的量之比是
C . 溶质和溶剂的物质的量之比是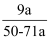 D . 硫酸根离子的质量分数是
D . 硫酸根离子的质量分数是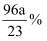
向200mL Na2CO3和 NaHCO3混合溶液中缓慢滴加0.1 mol•L-1稀盐酸,当加入的盐酸体积为100 mL后开始产生气体,加到 amL 时测得产生的气体在标准状况下体积为0.672L,继续滴加盐酸不再产生气体(不考虑气体的溶解)。下列说法错误的是( )
A . a=400
B . 原溶液中c(NaHCO3)=0.1 mol•L-1
C . 滴加稀盐酸50mL时,溶液中n(Na2CO3):n(NaHCO3)=1:2
D . 产生气体时反应的离子方程式为:H++ HCO =CO2↑+ H2O
=CO2↑+ H2O
 =CO2↑+ H2O
=CO2↑+ H2O
安全第一,预防为主。下列化学事故处理方法正确的是( )
A . 不慎将碱液溅到眼中,应立即用硫酸溶液冲洗,边洗边眨眼睛
B . 有大量的氯气泄漏时,用肥皂水浸湿软布蒙住口鼻,向高处撤离
C . 酒精灯着火时可用水扑灭
D . 蒸发操作时,应将溶液完全蒸干后停止加热
下列仪器名称为“容量瓶”的是( )
A .  B .
B .  C .
C .  D .
D . 
最近更新
- 小陆拆开收音机发现有一块电路板,其上面有许多元件和电阻联成网络,如果不拆下电阻,而要测量其中一只电阻的大小(如图所示的R
- 现要验证“当质量—定时,物体运动的加速度与它所受的合外力成正比”这一物理规律给定的器材如下:一倾角可以调节的长斜面(如图
- 设函数 (1) 求f(x)的定义域 (2) 求函数f(x)的值域
- 下列关于遗传实验和遗传规律的叙述,正确的是 A.非等位基因之间的自由组合会影响等位基因的分离 B.杂合子与纯
- 在希腊哲学思想中,主张把讨论的重点从认识自然转移到认识社会的是( ) A.泰勒斯 B. 苏格
- Zanzibar,Tanzania--Hundreds of dead dolphins were wa
- 读下图,下列说法正确的是( )A.A地受副热带高气压控制,为热带沙漠气候 B.B地与C地处于相同的风带控制下,气候
- D 解:
- 在西班牙内战时英国统治者说:“如果让现在正在西班牙和法国流行的共产主义传染病传播到其他国家,那么已经在自己的国土消失了传
- 5月21日,__________同志先进事迹首场报告会在北京人民大会堂举行。该同志是云南省迪庆军分区原副司令员,从军以来
- (3分)一只生活在室内的狗常常会扒地毯试图埋藏一块骨头,它的动作就像挖土一样,这是 行为(填“先天性”或“后
- 二战后资本主义国家发展迅速的最主要原因是 A、加强国际关系的联系 B、第三次科技革命的推动 C、阶
- 已知都是定义在上的函数,对任意的,存在常数则在A上的最大值为 A.
- 二战后期,涉及到实现战后德国民主化内容的重要国际会议有( ) ①开罗会议 ②华盛顿会议
- 已知函数. 求函数的最小正周期及在区间上的最大值和最小值;
- 请指出下列现象各反映了声音的哪种特征?(选填“音调”“响度”或“音色”) ①、男人说话的声音多数比女人低沉:______
- 日常生活中的一些小窍门或小常识往往包含着一些化学原理。下列做法正确的是() ①油锅着火时迅速加入大量青菜灭火;②用钢丝球
- 读“非洲某区域图”,回答7~8题。7.E为纳米布沙漠,它沿非洲西南大西洋海岸延伸2 100千米,该沙漠最宽处达160千米
- 面对层出不穷的类似“紫砂门”现象,从根本上要靠() A.企业增强道德自律 B.消费者提高辨别力
- 如图所示,将一根不可伸长、柔软的轻绳两端分别系于A、B两点上,一物体用动滑轮悬挂在绳子上,达到平衡时,两段绳子间的夹角为