第一章 从实验学化学 知识点题库
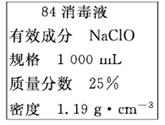
-
(1) 该“84消毒液”的物质的量浓度约为mol·L-1。(保留小数点后一位)
-
(2) 某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=mol·L-1。
-
(3) 该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是__(填字母)。
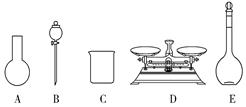 A . 如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 B . 容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 C . 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 D . 需要称量NaClO固体的质量为143.0 g
A . 如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 B . 容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 C . 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 D . 需要称量NaClO固体的质量为143.0 g -
(4) “84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2L2.3mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为mol·L-1。
②需用浓硫酸的体积为mL。
-
(1) 溶液中CuCl2的物质的量;
-
(2) 溶液中Cu2+和Cl-的物质的量。
①在制取氧气中排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
②进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
③水和碘的四氯化碳溶液分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出
④进行蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
⑤酒精着火时可用湿抹布或沙子扑灭
⑥用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
①化学原理为: 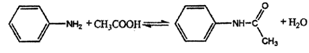 (已知:苯胺易被氧化)
(已知:苯胺易被氧化)
②相关物质的物理常数
| 物质 | 相对分子 质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度(g) | |
| 水 | 乙醇 | |||||
| 苯胺 | 93 | 无色液体 | 6 | 184 | 3.42(20℃) | 任意比混溶 |
| 冰醋酸 | 60 | 无色液体 | 17 | 118 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 135 | 白色片状固体 | 114 | 304 | 0.56(20℃)、3.45(50℃)、5.20(100℃) | 36.9(20℃) |
③制各乙酰苯胺的装置如图所示:韦氏分馏柱作用与原理类似于冷凝管。
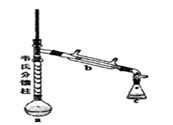
a b c
④制备方法和过程:

-
(1) 仪器a的名称。
-
(2) 制备过程中加入锌粒的作用:其一是、其二是防止暴沸。
-
(3) 从化学平衡的角度分析,步骤1要控制分馏柱上端的温度在105℃左右的原因。
-
(4) 步骤2中将反应液倒入冷水中的目的是。
-
(5) 步骤3中洗涤剂最好选择________。A . 冷水 B . 热水 C . 15%的乙醇溶液 D . NaOH溶液
-
(6) 步骤4重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→→冷却结晶→过滤→洗涤→干燥。
-
(7) 本实验所得到的乙酰苯胺产率是。
 L−1的CuCl2溶液中含有的氯离子数为4NA
L−1的CuCl2溶液中含有的氯离子数为4NA
-
(1) Ⅰ“侯氏制碱法”是我国化工专家侯德榜为世界制破工业作出的突出贡献。某实验小组模拟“侯氏法”的工艺流程及实验装置(部分夹持装置省略)如下:
气体A的饱和溶液
 A与食盐的饱和溶液
A与食盐的饱和溶液  悬浊液
悬浊液  晶体
晶体  纯碱
纯碱气体A为(填化学式)。
-
(2) 工业上粗盐(含Ca2+、Mg2+、SO
 等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为。
等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为。
-
(3) 第Ⅲ步操作用到的主要玻璃仪器是。
-
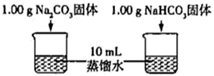
(4) Ⅱ、某小组利用传感器探究Na2CO3和NaHCO3的性质。已知:氢氧根离子的浓度越小,溶液碱性越弱,(具体过程如图)
编号
实验操作
实验Ⅰ
测量下面实验过程中温度的变化
实验Ⅱ
测量下面实验过程中溶液pH的变化
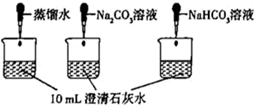
注:Na2CO3溶液和NaHCO3溶液的浓度相等
实验Ⅲ
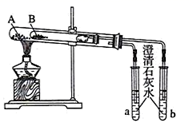
请回答:
实验Ⅰ中,溶解时吸收热量的物质是(填化学式)。
-
(5) 实验Ⅱ中,滴加NaHCO3溶液的烧杯中溶液酸碱性变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,(填离子符号)参与了反应。
-
(6) 若用方法Ⅲ验证Na2CO3和NaHCO3的稳定性,则试管B中装入的固体是 (填化学式)。由此可知方法Ⅲ(填“能”或“不能”)鉴别Na2CO3和NaHCO3。
-
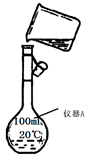
(1) 写出仪器A的名称:;
-
(2) 现需配制250 mL 0.2 mol·L-1 NaCl溶液,图为某同学转移溶液的示意图,图中有两处不正确分别是,。
-
(3) 下列操作,使所配溶液浓度偏小的是
①烧杯中NaOH溶液移入容量瓶后没有洗涤烧杯
②定容后摇匀,发现液面低于刻度线,再滴加蒸馏水至刻度线
③实验用的容量瓶洗净后未干燥,里面含有少量水
④定容时俯视
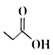 +
+ ![]()
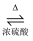
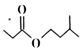 +H2O
+H2O
| 相对分子质量 | 密度/( | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.81 | 131 | 微溶 |
| 丙酸 | 74 | 0.99 | 141 | 易溶 |
| 丙酸异戊酯 | 144 | 0.87 | 156 | 微溶 |
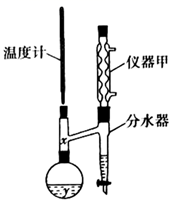
(实验步骤)在烧瓶中加入 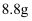 异戊醇、
异戊醇、 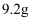 丙酸、数滴浓硫酸和2~3片碎瓷片;分水器中加入一定体积水;加热至70℃保持恒温半小时,然后提高温度使反应处于回流状态。分水器中液面不断上升,当液面达到分水器支管口时,上层液体返回到烧瓶中。
丙酸、数滴浓硫酸和2~3片碎瓷片;分水器中加入一定体积水;加热至70℃保持恒温半小时,然后提高温度使反应处于回流状态。分水器中液面不断上升,当液面达到分水器支管口时,上层液体返回到烧瓶中。
回答下列问题:
-
(1) 仪器甲的名称是。在70℃反应时温度计水银球置于(填“x”或“y”)处。
-
(2) 使用分水器能提高酯的产率,原因是(用平衡移动原理解释)。
-
(3) 升温回流过程中观察到(填标号)现象时,说明酯化反应已基本完成。
a.分水器中出现分层 b.分水器中有液体回流至烧瓶
c.分水器中水层高度不再变化 d.仪器甲中有液体滴落
-
(4) (产品提纯)
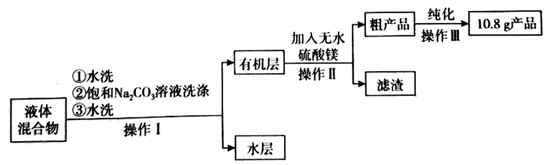
操作Ⅰ中,第二次水洗的主要目的是;操作Ⅱ中加入少量无水硫酸镁的目的是;操作Ⅲ的名称是。
-
(5) 丙酸异戊酯的产率是%;若反应前分水器中加水不足,会导致产率(填“偏高”、“偏低”或“无影响”)。
-
(1) I.酸法。矿渣经硫酸浸取后,浸取液通过电沉积得到单质Cr;向剩余溶液中加碱回收得到Al(OH)3。
为提高矿渣的浸取率,可采取的措施有(写出两点)。
-
(2) 电沉积时,阴极的电极反应式为。
-
(3) II. 碱法。工艺流程如下:
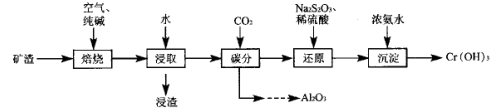
已知:①“焙烧”后固体成分为Na2CrO4、NaAlO2、NaFeO2。
②
 、Zn2+均可与EDTAl:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
、Zn2+均可与EDTAl:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。浸渣的主要成分为Fe(OH)3。则“浸取”时发生反应的离子方程式为。
-
(4) “浸取”后所得溶液中Al的含量可用EDTA滴定法测定:
①取20.00mL浸取液于锥形瓶中,加入c1mol•L-1EDTA标准液V1mL(稍过量);
②依次用盐酸、醋酸钠—醋酸缓冲溶液调溶液至酸性,加热后滴入PAN指示剂;
③用c2mol•L-1ZnSO4标准液滴定至溶液恰好呈紫红色,消耗标准液V2mL。则“浸取”后所得溶液中Al的含量为g•L-1(填计算式即可)。
-
(5) “碳分”时通入CO2后,通过 (填操作名称),即可得到纯净的Al2O3。
-
(6) “还原”时发生主要反应的离子方程式为。
-
(7) “沉淀”时,当c(Cr3+)≤10-5mol•L-1时,应调节溶液的pH至少为。(Ksp[Cr(OH)3]=1.0×10-32)
 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
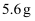 乙烯中含有的共用电子对数为
乙烯中含有的共用电子对数为  B .
B .  完全分解转移的电子数为
完全分解转移的电子数为  C . 等物质的量的
C . 等物质的量的  与
与  所含中子数之比为
所含中子数之比为 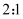 D . 标准状况下,
D . 标准状况下, 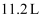 的苯中含有分子的数目为
的苯中含有分子的数目为 
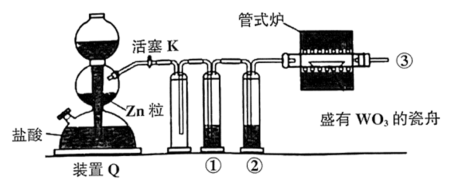
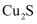 与氧气在高温条件下反应生成铜与
与氧气在高温条件下反应生成铜与 。欲用该方法生产
。欲用该方法生产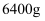 铜单质,请计算同时产生的
铜单质,请计算同时产生的 的体积(标准状况下)。
的体积(标准状况下)。
- 2010年6月12日是我国第五个“文化遗产日”。设立“文化遗产日”,就是要使文化遗产保护成为一种全民族的文化自觉。下列关
- 2015年底将在上海首飞的C919大型飞机采用了大量新型材料铝锂合金。下列关于铝锂合金的说法不正确的是( ) A.
- 老师设计了一个接力游戏,用小组合作的方式完成分式的运算,规则是:每人只能看见前一个人给的式子,并进行一步计算,再将结果传
- 下列叙述中错误的是( )。 A.原子半径:Cl>S>O B.还原性:Na>
- My son was badly hurt in a fire. After he 36 from a seri
- 18.在下面一段文字横绒处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过15个字。(5分) 全世
- 图中的文物属于夏、商、西周“青铜文明”的是
- 某混合气体通过溴水(使其褪色),再通过灼热的氧化铜(使其黑色变红色),再通过无水CuSO4白色粉末(使其变蓝色),再通过
- 已知函数(其中ω为正常数,x∈R)的最小正周期为π. (1)求ω的值; (2)在△ABC中,若A<B,且,求.
- 常温下,下列各组离子在指定溶液中可能大量共存的是( )A.滴入甲基橙显红色的溶液中: Na+、NO3-、I-、SO
- —Mr . Smith was really helpful when you were in financial di
- 近来,一些地方连续出现令人痛心的重大校车事故。国务院对此高度重视,责成有关 部门迅速制定《校车安全条例》,力求使校车成为
- 世界上面积最大的大陆是 ( ) A.亚欧大陆 B.美洲大陆 C.非洲大陆
- 2010年广州亚运的会徽以柔美上升的线条,构成了一个造型酷似火炬的五羊外形轮廓,把跑道、五羊、“海上丝路,广州是起点”等
- 若将一定质量的硝酸钾不饱和溶液变为饱和溶液,则( ) A.溶液的质量一定变小 B.溶液中溶质的质量分数
- 下列各句中,没有语病、句意明确的一句是 A.诚信教育已成为我国公民道德建设的重要内容,因为诚信不仅关系到国家的整体形象,
- 英国现代哲学家罗素说过:“如果世界上有‘骄傲到不肯打仗’的民族,那么这个民族就是中国。中国人天生的态度就是宽容和友好,以
- 根据句意,用括号内所给词的适当形式填空。 6.The Yellow Riveris the second _______
- —Tommy,do the dishes. —Mum,it’s a girl’s job.I would rather_
- 在研究匀变速直线运动的实验中,如图所示为一次记录小车运动情况的纸带图中A、B、C、D、E为相邻的记数点,相邻的记数点间的
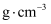 )
)


