第二节 金属的化学性质 知识点题库

【提出问题】黑色粉末A可能是什么呢?
-
(1) 【进行猜想】小明认为黑色粉末A全部是铁粉.请写出铁粉与CuSO4溶液反应的化学方程式.实验过程中采取了过滤,该操作中用到的玻璃仪器有,和玻璃棒,其中玻璃棒的作用是.
-
(2) 小华认为小明的猜想是错误的,理由是.
-
(3) 小华提出了猜想①和猜想②,请结合所学知识补充余下的一个猜想.
猜想①;黑色粉末A由铁粉和四氧化三铁(Fe3O4)组成
猜想②;黑色粉末A由铁粉和氧化亚铁(FeO)组成;
猜想③;.
【查阅资料】铁的氧化物都能与稀盐酸,稀硫酸反应,其中氧化铁为红棕色,其余都为黑色,并且只有四氧化三铁能被磁铁吸引.
【实验探究】
方案
实验操作
可能的现象
结论
①
取适量黑色粉末A 用磁铁吸引
黑色粉末全部被吸引
猜想①正确
②
取适量黑色粉末A 用磁铁吸引
黑色粉末部分被吸引
猜想②正确
③
取适量黑色粉末B加入足量稀盐酸
黑色粉末全部溶解
猜想②正确
④
猜想③正确
【反思评价】小娟认为方案②和方案③中得出的结论都不正确,其理由是.
【得出结论】在高温下,一氧化碳和二氧化碳可生成铁,氧化亚铁,四氧化三铁.请写出只生成氧化亚铁的方程式.

(如:a+b﹣反应 b+c﹣反应 c+d﹣反应)
a | b | c | d | |
① | CO2 | NaOH溶液 | CuSO4溶液 | Fe |
② | 稀盐酸 | Na2CO3溶液 | CaCl2溶液 | CO2 |
③ | AgNO3溶液 | BaCl2溶液 | 稀硫酸 | Fe2O3 |
④ | Zn | 稀盐酸 | NH4NO3溶液 | Ca(OH)2溶液 |

下列说法正确的是( )


【查阅资料】
常温下镁粉能与水发生置换反应,且放热。
【进行实验】
同学们用下图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8 mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:

(实验时的室温为22.8℃)
实验序号 | A | B | C | D | E | F |
固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
乙中现象 | 少量肥皂泡,难以点燃 | ______ | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡,点燃有爆鸣声 |
混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
【解释与结论】
-
(1) 实验B,乙中现象为。
-
(2) 实验A证明了镁粉与水能反应,完成该反应的化学方程式Mg+2H2O=+H2
 。
。
-
(3) 使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入。
-
(4) 【反思改进】
同学们分析实验数据发现,升高的温度没有达到食品加热袋的效果,其可能的原因是。
-
(5) 同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中剩余固体混合物中仍然含有铁粉,检验其铁粉存在的的实验方案为:取少量固体混合物。
-
(6) 从上述实验初步得出“NaCl溶于水没有热量的变化”的结论,依据的两个实验是(填实验序号)。

-
(1) 步骤①中玻璃棒的作用是。
-
(2) 步骤③的名称是。

-
(1) 机身外壳材料的主要成分是铝合金,它属于(填“纯净物”或“混合物”),与单质铝相比,它的硬度更(填“大”或“小”),写出铝离子的结构示意图:。
-
(2) 请用化学方程式表示金属铁、铝的活动性顺序。
-
(3) 根据扫地机器人的制造、使用情况,谈一谈化学与生活的关系。
-
(1) 家用热水瓶内胆壁的银白色金属是(填符号,下同);液体金属是;地壳中含量最高的金属元素是,人体中含量最多的金属元素是。
-
(2) 镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是(任写一个化学方程式)。该合金属于(填“混合物”或“纯净物”),它是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于(填“物理”或“化学”)变化。
-
(3) 合金的很多性能与组成它们的纯金属不同。如图能表示锡铅合金的是(填序号“a”“b”或“c”)。

-
(4) 铝冶炼厂以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,其反应的化学方程式为。
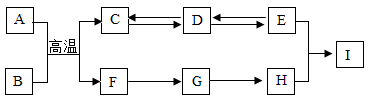
请回答下列问题:
-
(1) C的化学式为。
-
(2) 写出G→H的化学方程式为。
-
(3) D→E属于反应(基本反应类型)。
 ②
②  ③
③  不反应,则下列符合要求的X、Y、Z分别是( )
不反应,则下列符合要求的X、Y、Z分别是( )

-
(1) 反应①的化学方程式为。
-
(2) 反应②的化学方程式为。
-
(3) 反应④的化学方程式为。
 。有关该反应的说法错误的是( )
。有关该反应的说法错误的是( )

-
(1) 写出A点发生的反应化学方程式。
-
(2) 写出B点对应的溶液中含有的金属离子符号。
- “That’sa beautiful table cloth.” “Yes, but it’s not _____
- 《食品安全法》规定:社会团体或其他组织、个人在广告中推荐不符合食品安全标准的食品而使消费者合法权益受到损害的,应与食品生
- 一般人认为,下雪是悄无声息的,但美国某教授经过长期研究发现,“雪落有声”。雪在空中是寂静无声的,可雪一旦落入水中,通过传
- 设定义域,值域为R的单调函数y=f(x)的反函数为y=f-1(x),且f(x)+f(-x)=2则f-1(-1)+f-1(
- (2010年12月浙江省新高考联盟高三联考15题)在第一次工业革命中发挥了重大作用的科学理论是( ) A.生物进化
- 古代文人常常把笔伸向广阔的大自然,请分别写出含有下列自然事物的完整的两句古诗。 山: 水: 春 花: 秋: 月: 风:
- Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸
- 阅读下面的文字,完成各题。 今人对长城最熟悉的印象,莫过于______的长城边墙和敌楼墩台,那如巨龙般的身形正符合中国人
- 用聚苯乙烯泡沫塑料制成的一次性快餐餐具,由于难以降解,造成了对环境的白色污染。最近研制出一种新材料:能替代聚苯乙烯,它是
- 第三部分:阅读理解(共20小题;每小题2分,满分40分) 阅读下列短文,从每题所给的A、B、C、D四个选项中,选出最佳选
- No one can be sure______in a million years. A.what man will
- 下列选项属于内力作用的是 A、变质作用 B、搬运作用 C、风化作用 D、侵蚀作用
- 以下顺口溜属于合理消费的是 ( )A.我去电影院,不买盗版看B.泡吧我不去,买书受教育C.不买“耐克”穿,我
- —There is no need ______,for the clock says we have about te
- 下图表示用云母片(具不透水性)插入燕麦胚芽鞘的尖端部分。用单侧光照射培养一段时间后,胚芽鞘的生长情况是 ( )
- 电磁打点计时器的电源应该是 (填“交流”或“直流”)电源。实验室使用我国民用电时,每隔
- 朱自清曾这样描述一个城市:这是一个别致地方。……大运河穿过这个城市像反写的S,这就是大街;另有小河道四百十八条,这些就是
- 根据你对金属钠性质的了解,完成下列问题。 (1)关于钠的叙述中,正确的是( ) A.钠是银白色金属,硬度很大 B.将金
- 如图为人体内体温与水盐调节的示意图,下列叙述正确的是()①当受到寒冷刺激时,a、b、c、d四种激素的分泌均会增加 ②c、
- 科学家做过如下的试验:①把不含生长素的两小块琼脂放在燕麦胚芽鞘下端(如下图所示);②把含生长素的琼脂小块放在一段燕麦胚芽



