第二节 金属的化学性质 知识点题库
 B . 等质量的Zn和Mg分别与足量等体积等质量分数的稀硫酸反应
B . 等质量的Zn和Mg分别与足量等体积等质量分数的稀硫酸反应 C . 向NaOH溶液中逐滴加入稀盐酸
C . 向NaOH溶液中逐滴加入稀盐酸 D . 等质量CaCO3分别与足量等体积等质量分数的稀盐酸反应
D . 等质量CaCO3分别与足量等体积等质量分数的稀盐酸反应
 B .
B .  C .
C .  D .
D . 

 镁在空气中加热
B .
镁在空气中加热
B .  向盛有少量二氧化锰的烧杯中不断的加入过氧化氢溶液
C .
向盛有少量二氧化锰的烧杯中不断的加入过氧化氢溶液
C .  将等质量的镁片和铁片投入到等体积等溶质质量分数的足量稀硫酸中
D .
将等质量的镁片和铁片投入到等体积等溶质质量分数的足量稀硫酸中
D .  在一定温度下,向饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
在一定温度下,向饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
| 选项 | 实验目的 | 实验方案 |
| A | 获得廉价的新能源 | 电解水制H2 |
| B | 将河水净化为纯水 | 经沉淀、过滤、吸附 |
| C | 验证金属活动性Zn>Cu | 利用Zn片与CuSO4溶液的反应 |
| D | 除去NaCl固体中少量的MgCl2 | 加水溶解,再加入过量NaOH溶液 |
-
(1) 若向所得固体上滴加盐酸有气泡产生,则该固体含有金属为。
-
(2) 写出有关的化学反应方程式(一个即可)。
-
(3) 猜想滤液中溶质为Mg(NO3)2、Zn(NO3)2、AgNO3 , 请分析该猜想不合理的原因。
-
(1) 钢、铝合金、塑料、橡胶等是制造共享单车的材料,上述材料中属金属材料的是。
-
(2) 钢、铁在潮湿的空气中容易锈蚀,共享单车生锈与有关(填名称),为了防止铁制品生锈,可采取的措施是(填一点)。
-
(3) 铜、铁、铝是合金中最常见的金属,要比较铜、铁和铝的金属活动性,如果选用了铝和铜,还需要用到的试剂是(只填一种试剂);铝制品耐用,其原因是铝能与空气中的氧气反应生成一层致密的氧化铝薄膜,因此铝具有良好的性能。
-
(4) 共享单车采用手机扫描二维码来解锁,而手机采用高能锂(Li)电池作为电源。
①锂原子(Li)的原子结构示意图如图所示
 ,则锂离子符号为;
,则锂离子符号为;②锂电池放电时的总反应为Li+MnO2=LiMnO2 , LiMnO2中锰元素的化合价为。
-
(1) 高铁车厢质轻、强度大,是利用制成(填“复合材料”或“无机非金属材料”)。
-
(2) 铝热剂是修筑铁路时常用的焊接材料,其反应原理是,铝在一定的条件下与氧化铁反应,得到熔融的铁和另一种氧化物,该反应的基本类型是。
-
(3) 某品牌的空气净化剂含有过氧化钠(Na2O2),它可以使车厢里的二氧化碳转化为碳酸钠和氧气,写出该反应的化学方程式。
-
(4) 高铁是以电能为动力来源的电动列车,它与以燃煤为动力来源的蒸汽列车相比,其优点是(要求只答一条)。

-
(1) 依此判断下列物质化学式:C,G;组成物质B的元素有。
-
(2) 写出下列各物质间转化的化学方程式:A→J:;E→H+I:;K→L:;
-
(3) 在历史博物馆中,很少有由J制造的较完好的古物,其原因是。
-
(1) 某化学兴趣小组利用图甲所示装置测定空气中氧气的含量,同时用气体压力传感器测出集气瓶中的气压变化,并用数据处理软件以数字、曲线的形式实时显示。集气瓶内气压变化如图乙所示。

①实验前要检查甲装置的气密性,其操作为:按甲图连接好实验仪器,。
②图乙中A点为点燃前集气瓶中的气压,AB段气压显著增加的原因是, t3时刻后瓶内气压又显著增加,t3时进行的实验操作是。
③另一小组同学用甲装置进行该实验,结束时,观察到进入集气瓶内的水大于集气瓶内原空气体积的
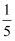 ,可能的原因是 (填写序号)。
,可能的原因是 (填写序号)。A燃烧匙内红磷不足
B将燃烧匙伸入集气瓶的操作过于缓慢
C旋紧橡皮塞后发现橡胶管上未夹弹簧夹
D未等到装置完全冷却就打开弹簧夹
-
(2) 钯(元素符号:Pd)是航空、航天等高科技领域以及汽车制造业不可缺少的关键材料。另一化学兴趣小组通过实验探究“金属钯的金属活动性顺序”,实验操作及对应现象如下:
实验操作
实验现象
向放有少量灰黑色钯粉的试管中加入适量稀盐酸
无明显现象
向放有少量银白色银片的试管中加入适量氯化钯 (PdCl2)溶液
银片表面变黑
向放有少量银白色铂丝 (Pt)的试管中加入适量氯化钯溶液
无明显现象
①Pd在金属活动性顺序中位于。
AH之前 BH和Ag之间 CAg和Pt之间 DPt之后
②钯属于贵重金属,其回收具有重要的现实意义。该兴趣小组利用实验中的氯化钯废液,设计了如下提取金属钯的实验过程:

“过量X”、“过量Y”均为中学化学实验室常见试剂,则X为,Y为。
-
(1) 金属镓与稀硫酸反应,产物中Ga的化合价为+3,反应的化学方程式是。
-
(2) 高纯氧化镓广泛用于生产半导体材料,其一种制备方法如下:
步骤1:向含有硫酸的硫酸镓溶液中通入某种气体,冷却,生成Ga(NH4)(SO4)2固体。
步骤11:在一定条件下灼烧Ga(NH4)(SO4)2固体,制得高纯氧化镓。
①Ga(NH4)(SO4)2中含有的带电的原子团(根)是 (填化学符号)。
②步骤I反应的化学方程式是Ga2(SO4)3 +2X+H2SO4
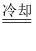 2Ga(NH4)(SO4)2↓,则 x的化学式为。
2Ga(NH4)(SO4)2↓,则 x的化学式为。 -
(3) 氮化镓(GaN)是第三代半导体材料,一般采用GaCl3和NH3在一定条件下制得,同时得到另一种化合物,该反应的化学方程式为。
⑴产生氢气多少克?
⑵这种硫酸溶液中溶质的质量分数为多少?

请回答:
-
(1) 过程I发生的反应之一为:
 。X的化学式为。
。X的化学式为。
-
(2) 过程Ⅱ加入过量锌,反应的化学方程式为。
-
(3) 过程Ⅲ中加入的物质是(填化学式),过程Ⅱ、Ⅲ都要用到的玻璃仪器有玻璃棒、烧杯与。
- 下面是一核反应方程:+→+X,用c表示光速,则( )A.X是质子,核反应放出的能量等于质子质量乘以c2B.X是中子
- “大丈夫生于世间,宁可粗布以御寒,也要保持民族气节,不可为锦衣玉食做无耻的帮凶和奴才。”在民主革命中为中华民族而牺牲的
- 用标准盐酸测定某NaOH溶液的浓度,用甲基橙作指示剂,下列测定结果可能偏低的是( )A.酸式滴定管在装液前未用标准
- 如图是一个几何体的三视图,根据图中数据,可得该几何体的表面积是 ( ) A.9 B.12 C.11
- 如图所示,下列说法正确的是( ▲ )A、若AB//CD,则∠A+∠ABC=180°B、若AD//BC,则∠C+∠ADC=
- to feed monkeys
- 阅读下面两段文字,完成1—5题。 [甲]当余之从师也,负箧曳屣行深山巨谷中。穷冬烈风,大雪深数尺,足肤皲裂而不知。至舍,
- 设,函数的图像可能是( )
- (6分)(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,
- 世界上最大的发展中国家是 ( )A.中国 B.印度 C.印度尼西亚
- 从“天问”探测火星到北斗组网,从“嫦娥”奔月到万米深潜……一项项前沿科技成果引起全球关注。然而,部分关键元器件、原材料依
- 在成熟的神经细胞中,下列几种酶中最不活跃的是 A.ATP合成酶 B.DNA聚合酶 C.呼吸酶
- 下列相关反应的离子方程式书写错误的是 A.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO-+4O
- 学校举行“我最喜欢的一篇高中语文课文”的推荐活动,请您填写下面的表格,推荐一篇课文。要求表述简明连贯,突出课文特点。 课
- 下面句子中加点的虚词,使用正确的一项是( ) A.关于日前出现在报端的那些言论,我虽然又好气又好笑,但也颇有些高兴,因
- 下列各句中加点的成语使用恰当的一句是: A.我们决不能因某一事的成功而沾沾自喜,就此满足。 B.张厂长的一席话起到了抛砖
- 为了解某住宅区的家庭用水量情况,从该住宅区中随机抽样调查了50户家庭去年每个月的用水量,统计得到的数据绘制了下面的两幅统
- 苹果有“智慧果”、“记忆果”的美称,多吃苹果有增进记忆、提高智力的效果,苹果中富含的维生素C(C6H8O6)还具有增强免
- (本小题满分5分)如图,已知,求AB和BC的长.
- 下列化学微粒可以代表一个分子的是 A. B. C.64Cu



