第二节 金属的化学性质 知识点题库

 Fe3O4
B . CaCO3
Fe3O4
B . CaCO3  CaO+CO2↑
C . CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
D . C+2CuO
CaO+CO2↑
C . CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
D . C+2CuO  2Cu+CO2
2Cu+CO2

物质 | 所含杂质 | 除去杂质的方法 | |
A | O2 | CO | 点燃混合气体 |
B | NaOH | NaCl | 适量的稀盐酸溶液 |
C | CuO | Cu | 在纯氢气流中加热 |
D | H2 | 水蒸汽 | 通过盛有浓硫酸的洗气瓶 |
图1 
图2 
(查阅资料)
①锌皮为金属锌  含有少量的铁
含有少量的铁  ;
;
②黑色糊状填充物由炭黑、  、
、  和
和  等组成;
等组成;
③有关数据见表:
| 温度 | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 | | | | | | | |
| | 343 | 395 | 452 | 488 | 541 | 614 | |
-
(1) (实验探究一)小明取适量黑色糊状填充物,按如图2所示实验流程进行探究。
操作I除溶解外,还需进行的操作是,操作Ⅱ中采用冷却热饱和溶液的方法提取N的原理是。
-
(2) 欲从固体M中得到较纯的
 ,操作Ⅲ可采用的简便方法是。
,操作Ⅲ可采用的简便方法是。
-
(3) (实验探究二)小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
取一块锌皮放入盛有适量稀盐酸的烧杯中,有
 生成。写出能生成氯化锌的另一个反应的化学方程式
生成。写出能生成氯化锌的另一个反应的化学方程式  必须与前一个反应有一种相同的反应物,写一个即可
必须与前一个反应有一种相同的反应物,写一个即可  。
。 -
(4) 若将
 锌皮与足量稀硫酸完全反应,则生成氢气的质量
锌皮与足量稀硫酸完全反应,则生成氢气的质量  选填“
选填“ 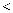 ”、“
”、“  ”或“
”或“  ”
” 
 .下列说法正确的是( )
.下列说法正确的是( )
 2Fe+3CO2
C . 潜艇供氧 2Na2O2+2H2O═4NaOH+O2↑
D . 焊接铁轨 2Al+Fe2O3
2Fe+3CO2
C . 潜艇供氧 2Na2O2+2H2O═4NaOH+O2↑
D . 焊接铁轨 2Al+Fe2O3  2Fe+Al2O3
2Fe+Al2O3
①滤渣中一定有Ag、Cu
②滤渣中一定有Ag,可能有Cu,一定没有Fe、Zn
③滤液中一定有Fe(NO3)2 , 可能有AgNO3、Cu(NO3)2、Zn(NO3)2
④滤液中一定有Fe(NO3)2、Zn(NO3)2 , 可能有AgNO3、Cu(NO3)2
⑤滤液中一定有Fe(NO3)2、Zn(NO3)2 , 一定没有AgNO3 , 可能有Cu(NO3)2
⑥滤液的质量与原混合溶液的质量相比减少了.
-
(1) 镁与热水反应的化学方程式是:, 该反应的基本类型为;
-
(2) 查阅资料:溶液红色褪去的原因是溶液碱性减弱。
(提出问题)
导致溶液碱性减弱的原因是什么?
(假设与分析)
假设1:可能是氢氧化镁与N2或O2发生了反应;
假设2:可能是溶液吸收了空气中的 ;
假设3:可能是氢氧化镁的溶解度随温度的降低而 .由可知,假设1不成立。
-
(3) (实验探究)
实验操作
实验现象
结论
1.取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象
①
假设2成立
2.取上述红色溶液,②,③,观察现象
红色褪去
假设3成立
-
(4) (拓展延伸)
将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。请用化学方程式解释其原因: ① ;②;
-
(5) 除上述金属外,根据金属活动性顺序,预测也能跟硫酸铜溶液反应产生上述现象。(举一例即可)
-
(1) “垃圾分类从干湿分离开始”,这是许多城市在大力推进的简易垃圾分类法。
资料:“湿垃圾” 是指植物类和厨余类垃圾,由于含水量高、易腐坏更适于发酵制沼气和肥料等。除湿垃圾外的其他垃圾为“干垃圾”,经分拣后可分别被再利用。
①下列生活垃圾应投入“干垃圾”桶的是(填字母序号)。
A 菜叶、果皮 B 旧纸箱、玻璃瓶 C 剩菜、剩饭
②由于铁制品易生锈,所以“湿垃圾”桶一般不用铁而是用塑料制成。铁生锈的条件是铁与空气中的 等同时接触。
-
(2) 纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。

①纽扣电池的外壳可以加工得很薄,说明金属具有 性。
②氧化银固体加热分解可以得到两种单质其反应的化学方程式为。
③该电池中涉及铁、锌、银三种金属。它们的金属活动性由强到弱的顺序是(写名称)。
为了验证该结论,甲同学取质量相同的铁片、锌片、银片,分别加入足量的相同浓度的稀盐酸中;乙同学另取铁片放入硝酸锌溶液中。他俩收集到的下列证据,能支持上述结论的是(填字每序号)。
A 甲同学的实验中,银表面没有气泡产生
B 甲同学的实验中,放铁片的试管最终产生气泡的量比放锌片的试管产生的气泡多
C 乙同学的实验中,铁表面没有明显现象产生
-
(1) 三星堆遗址出土了大量的金器和青铜器,其中的黄金面具残片历经三千年依旧金光灿灿,这是因为金的化学性质;大量的青铜面具是用铜、锡等金属制成的合金,现将铜片和锡片分别伸入稀盐酸中,锡片表面有少量气泡生成而铜片没有,说明金属活动性锡(填“>”或“<”)铜。
-
(2) 晋代著名的炼丹家葛洪之妻曾用铁勺盛满曾青(硫酸铜溶液),一段时间后发现铁勺变成了“铜勺”,该过程发生反应的化学方程式为。铝在近一百多年里产量大幅提高。并被广泛使用。请写出铝抗腐蚀性能好的原因。
-
(3) 现代社会。金属更是被广泛使用。如可以将铁粉等物质制成便于携带的取暖物品“暖宝宝”。
①“暖宝宝”发热。其过程首先是铁粉与氧气、水反应生成氢氧化亚铁(Fe(OH)2)。该反应的化学方程式为。
②某兴趣小组利用下图装置。使用“暖宝宝”来测定空气中氧气的含量。实验开始前的装置如图所示,请写出在测定过程中应该在什么时候打开弹簧夹?。

③经过上述过程。实验后量筒中水减少了47mL(假设铁粉与氧气完全反应,暖宝宝体积忽略不计),则测得空气样品中氧气的体积分数为(精确到0.1%)。
-
(4) 该小组同学为探究某“暖宝宝”中铁粉的质重分数,取16g“暖宝宝”样品于烧杯中。向其中逐滴加入稀盐酸(“暖宝宝”中其他成分不与稀盐酸反应),放出气体的总质量与所滴入稀盐酸的质量关系如图所示。请计算该暖宝宝样品中铁粉的质量分数。


-
(1) 混合物中铁粉的质量为。
-
(2) 计算稀硫酸中溶质的质量分数。(写出计算过程)
① 向滤渣中加入稀盐酸,一定有气泡产生。
② 向滤液中加入稀盐酸,一定有沉淀产生。
③ 滤渣中一定含有Ag。
④ 滤液中一定含有Fe(NO3)2 , 一定不含AgNO3 , 可能含有Al(NO3)3
以上说法正确的个数为( )
- 质量为M的框架放在水平地面上,如图所示,一轻弹簧上端固定在框架上,下端固定一个质量为m的小球,小球上下振动时,框架始终未
- 下列注音有误的一项是( ) A.载(zài)歌载舞 弥笃(dǔ) 谙(ān)习箪食(shí) 壶浆 B.睚眦(zì)必报
- 在1980年所作的《目前形势和任务》中指出:“现在特别是在青年当中,有人怀疑社会主义制度,说什么社会主义不如资本主义,这
- 今年是农历猪年,兰兰家有一个放在水平桌面上的金猪宝宝艺术品,如图6所示。猪宝宝是实心的,兰兰很想知道它究竟是由什么物质制
- 加油站必须粘贴的标志是
- CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl·2H2O制备CuCl,并进行相关探究。【实验探究】
- 有人说:“古代西方什么都禁,就是不禁人的本能。中国什么都不禁,独禁本能。”假如你同意上述观点,你可以找到古代社会这一做法
- 下列句中加点的熟语使用恰当的一项是 A.“道理明摆着,不去‘祝贺’一下,把自来水公司给得罪了,以后常给你‘穿小鞋’,经常
- 下列有关生物多样性和进化的叙述中,不正确的是() A. 新物种的形成通常要经过突变和基因重组、自然选择及隔
- 某乡村距城市50,甲骑自行车从乡村出发进城,出发1.5后,乙骑摩托车也从乡村出发进城,比甲先到1,已知乙的速度是甲的速度
- -的相反数是( ) A.3 B.-3 C. D.-
- 女性生殖系统中,产生卵细胞的结构和受精的场所分别是 A.卵巢 子宫 B.卵巢 输卵管 C.子宫输卵管
- 下列物体的长度最接近于6×104μm的是()A.课桌长度 B.物理课本的厚度 C.墨水瓶的高度
- 两个形状完全相同的金属球,带电荷量分别为-2×10-9 C和-6×10-9 C,它们之间的静电力为F.在绝缘条件下,让
- 下列四句话中没有错别字的一句是: A 金融界以15%左右的股市下跌率作预警,而最近美国股市下泄已超过了这个门槛。 B 自
- 氯气在工业上有着重要的用途,某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝( 无水 遇潮湿空气即产生大量白雾) ,可
- 为了参加中考体育测试,甲、乙、丙三位同学进行足球传球训练.球从一个人脚下随机传到另一个人脚下,且每位传球人传球给其余两人
- 如图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图.请回答下列问题: (1)将A、E装置连接时,应将A装置的导
- x取哪些整数值时,不等式5x+2>3(x﹣1)与x≤2﹣都成立?
- 若直线与直线垂直,则 .












