初中 化学
(1)硫在氧气中燃烧 , 反应;
(2)锌与稀硫酸的反应 ;
(3)二氧化碳使澄清石灰水变浑浊 .
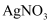 溶液反应
溶液反应  下列说法正确的是
下列说法正确的是 

如图是甲、乙两种固体物质的溶解度曲线.
(1)溶解度随温度升高而减小的物质是 .
(2)t1℃时,甲、乙两种物质的溶解度 .
(3)要使乙的饱和溶液变为不饱和溶液,除加水之外还可采用的方法是 .
(4)要使甲从其饱和溶液中析出,可用的方法.
(5)t2℃时,甲的饱和溶液中溶质的质量分数是 .
 2Hg + O2 ↑
C . CuO + CO
2Hg + O2 ↑
C . CuO + CO Cu +CO2
D . Mg + 2HCl =MgCl2+ H2↑
Cu +CO2
D . Mg + 2HCl =MgCl2+ H2↑


-
(1) NaCl、KNO3、NH4Cl三种固体在水中的溶解度曲线如图所示,请仔细观察曲线,回答下列问题:①三种固体物质的溶解度受温度影响最小的是。
②30℃时三种固体物质饱和水溶液中溶质的质量分数由大到小的顺序是。
③50℃时将20gNH4Cl固体加入到50g水中,充分溶解后,所得溶液是溶液。(填“饱和”或“不饱和”)
④图中A、B点的坐标为:A(10,21)、B(40,64).若将100g40℃的硝酸钾饱和水溶液降温到10℃,析出KNO3固体的质量为g(保留一位小数)。(保留一位小数)
-
(2) 有一包白色固体,可能含有氧化钙、硝酸钾、碳酸钠、碳酸钙中的一种或几种 。为探究其成分进行如下实验

①固体中一定含有。
②固体中一定没有。
③写出产生白色沉淀的化学方程式;反应类型为。

操作X的名称是,在实验室中进行该操作时用到的玻璃仪器有玻璃棒、烧杯、,在该操作中玻璃棒的作用是。
 。
。
-
(1) 锰元素。
-
(2) 2个镁离子。
-
(3) 氧化钙。
-
(4) 4个三氧化硫分子。
 B .
B .  C .
C .  D .
D . 

 水煮蛋
B .
水煮蛋
B .  土豆炖鸡块
C .
土豆炖鸡块
C .  沙糖桔
D .
沙糖桔
D .  清炒西葫芦
清炒西葫芦
回答下列的问题:
(1)金刚石和石墨物理性质存在差异的原因是 ;
(2)黄铜片和纯铜片互相刻划,纯铜片上有痕迹原因是 ;
(3)从微观角度分析,O2和O3化学性质不同的原因是 .
欲证明“CO2与NaOH发生了化学反应”,某化学兴趣小组进行以下探究实验(实验装置中夹持仪器已略去)。
(实验1)配制溶液
(1)用NaOH固体配制20g20%NaOH溶液,无需用到的玻璃仪器有___(填标号)。
A 胶头滴管 B 酒精灯 C 量筒 D 烧杯 E 玻璃棒
(实验2)按如图所示装置进行实验。

实验前U型管两端液面相平,将NaOH溶液滴入试管中,恢复到室温后,U型管中的液面左高右低。据此,甲同学得出“CO2与NaOH发生了化学反应”的结论。
(2)U型管中液面高度发生变化的原因是_______。
(3)上述结论的证据不充足,理由是_____。
(实验3)按如图所示装置进行实验。

查阅资料:i.CaCl2溶液呈中性;ii. ![]()
实验步骤如下:
①检查装置的气密性,往装置中加入药品;
②关闭K1、K2,将注射器中的NaOH溶液缓缓推入A中;
③A中物质充分作用后,打开K1,B中无色溶液倒吸入A中,A中产生沉淀且溶液显红色
④关闭K1,打开K2,将注射器活塞向上拉,C中溶液倒吸入A中。
(4)步骤③“产生沉淀”的现象仍不足以证明CO2与NaOH发生了化学反应,理由是____。
(5)步骤④中,若观察到____(填现象),证明CO2与NaOH发生了化学反应。CO2与NaOH反应的化学方程式为_______。
燃烧分类:
①_______ 燃烧:氧气充足;
②_______ 燃烧:氧气不足。
例如:碳的燃烧
氧气充足,化学方程式: _______ ;
氧气不充足 _______ ;( CO 中毒:与 _______ 结合,失去运氧能力)
A-F和X都是初中化学中的常见物质,其中A、C是无色气体,
B、F是红色固体,它们的转化关系如下图所示(部分生成物已 省略):
省略):
(1)写出反应①的化学方程式 ,工业上用此反应 。
(2)写出反应②的化学方程式 。
(3)含D的生产、生活用品腐蚀的过程,实际上是D与空气中的 发生化学反应的过程。
下列实验基本操作错误的是( )
A.  检查装置气密性
检查装置气密性 ![]() B.
B.  点燃酒精灯
点燃酒精灯
C. ![]() 滴加液体
滴加液体 ![]() D.
D.  过滤
过滤
同学们应用数字化实验探究外界条件对双氧水分解速率的影响.实验装置如图:

【进行实验】
| 序号 | 主要实验步骤 | 装置内压强﹣时间图象 |
| 实 验 1 | ①1号抽滤瓶中不加任何试剂, 2号抽滤瓶中加入0.2gMnO2粉末, 3号抽滤瓶中加入0.2gFeCl3粉末. ②用三支分液漏斗分别加入15mL4%的H2O2溶液. |
|
| 实 验 2 | ①三个抽滤瓶中分别加入0.2g FeCl3粉末. ②分别用1号分液漏斗加入15mL2%的H2O2溶液;用2号分液漏斗加入15mL4%的H2O2溶液;用3号分液漏斗加入15mL6%的H2O2溶液. |
|
| 实 验 3 | ①三个抽滤瓶中分别加入0.2g FeCl3粉末,分别放入装有10℃、20℃、40℃水的水槽中. ②用三支分液漏斗分别加入15mL4%的H2O2溶液. |
|
【解释与结论】
(1)实验1的2号抽滤瓶中反应的化学方程式为 .
(2)某同学得到“不同催化剂的催化效果不同”的结论,他的依据是 .
(3)通过上述实验得到:影响该反应速率的外界因素有 .
【反思与评价】
(4)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是 .
- How is it ______ he has made such rapid progress? A. that
- 由多种饱和链烃组成的不同批号的石油液化气,已知不同批号的每千克液化气在同温同压下汽化得到相同体积的可燃气体,下列叙述中可
- 两火箭A、B沿同一直线相向运动,测得二者相对地球的速度大小分别是vA=0.900c,vB=0.800c,试求二者互测的相
- 从新航路开辟到18世纪中期,海上殖民霸权几度易手,其先后顺序正确的是( ) A.西班牙→荷兰→英国
- 下列关于耳的结构及功能的叙述,正确的是( ) A.外耳道收集声波 B.鼓膜把声波转
- 对任意实数x,y,定义运算,其中为常数,等号右边的运算是通常意义的加乘运算,现已知,,且有一个非零实数m,使得对任意实数
- “a与5的和的2倍”用式子表示为() A.2a+5 B.2(a+5) C.a2+5 D.2(a﹣5)
- 某人现年30岁,身高90cm,最近通过了某科技公司的应聘考试,被聘为计算机软件开发工程师。他身材矮小,主要原因是 (
- 下列变化中,不属于缓慢氧化的是() A.动植物的呼吸 B.木炭燃烧 C.食物的腐烂 D.酒的酿造
- 下列有关细胞中元素和化合物的叙述,正确的是() A.微量元素在生物体内含量很低,但不可缺少,如叶绿素的组成离不开Mg元
- 除去二氧化碳中混有少量一氧化碳的正确方法是( ) A.用燃着的木条点燃 B.通过灼热的木炭 C.通过灼
- 如图,直三棱柱ABC—A1B1C1中,∠ACB=90°,∠BAC=30°,BC=1,AA1=,M为CC1的中点,求证:A
- 阅读下列材料,回答问题。(20分) 材料1:2010年8月31日中国石化集团总经理苏树林介绍说,经过三年的建设,川气东送
- Section B Directions: Read the following four passages. Each
- 钢铁工业是国家工业的基础。2008年我国粗钢产量近5亿吨,居世界首位,某中学社会实践活动小组利用假期对当地钢铁厂进行了调
- 阅读下列材料: 材料一图一 克伦威尔在纳西比战役中 图二克伦威尔就任护国主材料二 几乎所
- 下列各句中,没有语病的一项是 ( ) A 通过“三个代表”的学习,使广大干部进一步认识到加强和改进党的
- (1)多用电表的读数为________________。(2)用游标20分度的游标卡尺测量某工件的内径时,示数如图所示,
- 利用细胞工程方法,以SARS病毒核衣壳蛋白为抗原制备出单克隆抗体。下列相关叙述正确的是( ) A.用纯化的核衣壳蛋白
- 把含有变形虫的池水放入烧杯中,不久变形虫就会聚集在水的上层.这是因为它们需要() A. 充足的氧气 B. 充足的阳光 C






