高考化学试题
A. X、Z的最高价氧化物相互化合,生成的产物可用作防火剂
B. 电解X、Q元素组成的化合物的饱和溶液常被用于工业上制备X单质
C. W、X、Q三种元素都能形成多种氧化物
D. Y、Q形成的化合物是强电解质
EDTA(乙二胺四乙酸)是一种能与Ca2+、Mg2+等结合的螯合剂。某高三研究性学习小组在实验室制备EDTA,并用其测定某地下水的硬度。制备EDTA的实验步骤如下:

步骤1:称取94.5g(1.0mol)ClCH2COOH于1000mL三颈烧瓶中(如图),慢慢加入50%Na2CO3溶液,至不再产生无色气泡;
步骤2:加入15.6g(0.26mol)H2NCH2CH2NH2,摇匀,放置片刻,加入2.0mol·L-1NaOH溶液90mL,加水至总体积为600mL左右,温度计50℃加热2h;
步骤3:冷却后倒入烧杯中,加入活性炭脱色,搅拌、静置、过滤。用盐酸调节滤液至pH=1,有白色沉淀生成,抽滤,干燥,制得EDTA。测地下水硬度:取地下水样品250mL进行预处理后,用EDTA进行检测。实验中涉及的反应有M2+(金属离子)+Y4-(EDTA)=MY2-;M2+(金属离子)+EBT(铬黑T,蓝色)=MEBT(酒红色);MEBT+Y4-(EDTA)=MY2-+EBT(铬黑T)。
回答下列问题:
(1)步骤1中发生反应的离子方程式为_____。
(2)仪器Q的名称是_____,冷却水从_____接口(填“x”或“y”)流出。
(3)用NaOH固体配制上述NaOH溶液,配制时使用的仪器有托盘天平、药匙、烧杯、玻璃棒、_____和_____,需要称量NaOH固体的质量为_____。
(4)将处理后的水样转移到锥形瓶中,加入氨水-氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.0100mol·L-1EDTA标准溶液进行滴定。
①确认达到滴定终点的现象是_____。
②滴定终点时共消耗EDTA溶液15.0mL,则该地下水的硬度=_____度(水硬度的表示方法是将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把1L水中含有10mgCaO称为1度)。
③若实验时装有EDTA标准液的滴定管只用蒸馏水洗涤而未用标准液润洗,则测定结果将_____ (填“偏大“偏小”或“无影响”)。
A. 电解精炼铜时,阳极质量减小64g,转移电子数为2NA
B. 100g质量分数为46%的乙醇溶液中含有氢原子数为12NA
C. 7.8gNa2O2固体中含有离子总数为0.4NA
D. 100mL10mol・L-1浓盐酸与足量MnO2 加热充分反应,生成Cl2 的数目为0.25NA
Ⅰ、实验室制备硫代硫酸钠装置图如下。

(1)仪器B的名称是________。
(2)写出装置B制备Na2S2O3的化学反应方程式____________________________。
(3)NaOH溶液的作用是____________________________________。
Ⅱ、测硫代硫酸钠样品纯度步骤如下
①称取Ⅰ中制得硫代硫酸钠样品8.0g配成250mL溶液
②从①中量取20.00mL溶液于锥形瓶中
③用0.lmol·L-1标准碘液滴定,实验测得数据如下
| 滴定前读数(mL) | 滴定后读数(mL) | 待测液体积(mL) |
实验一 | 1.20 | 21.00 | 20.00 |
实验二 | 0.40 | 19.20 | 20.00 |
实验三 | 0.50 | x | 20.00 |
(4)该滴定时,向锥形瓶中加入1至2滴淀粉液作指示剂,则达到滴定终点的判断标准是______________。
(5)x读数如图所示,则x=________,根据所测的数据计算该硫代硫酸钠样品纯度为_______________。(已知I2+2Na2S2O3=2NaI+Na2S4O6)
(6)若步骤①中量取20.00mL硫代硫酸钠溶液时,未用硫代硫酸钠溶液润洗滴定管,则测得样品的纯度将______________(填“偏大”或“偏小”)。
(资料查阅)磷化锌易水解产生PH3;PH3沸点为-88℃,有剧毒性、强还原性、易自然。

(用量标准]如图:装置A、B、E中盛有的试剂均足量;C中装有100原粮;D中盛有40.00mL6.0×10-5 mol・L-1KMnO4溶液(H2SO4酸化)。
(操作流程)安装仪器并检査气密性→PH、的产生与吸收一转移KMnO4吸收溶液→用Na2SO3标准溶液滴定。
试回答下列问题:
(1)仪器E的名称是______;仪器B、D中进气管下端设计成多孔球泡形状,目的是______。
(2)A装置的作用是______;B装置的作用是吸收空气中的O2,防止______。
(3)下列操作中,不利于精确測定出实验结果的是______(选填序号)。
a.实验前,将C中原粮预先磨碎成粉末
b.将蒸馏水预先煮沸、迅速冷却并注入E中
c.实验过程中,用抽气泵尽可能加快抽气速率
(4)弹化锌发生水解反应时除产生PH3外,还生成______(填化学式)。
(5)D中PH3被氧化成H3PO4,该反应的离子方程式为______。
(6)把D中吸收液转移至容量瓶中,加水稀释至250.00mL,取25.00mL于锥形瓶中,用 5.0×10-5mol・L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液10.00mL.则该原粮中磷化物(以PH3计)的含量为______mg・kg-1,该原粮质量______(填“达标”或“不达标“)。
某离子液体的阴离子的结构如图所示,其中 W 、 X 、 Y 、 Z 、 M 为原子序数依次增大的短周期非金属元素, W 是有机分子的骨架元素。下列说法正确的是

A . Z 元素的最高价态为 +7 B . 基态原子未成对电子数: W>Y
C . 该阴离子中 X 不满足 8 电子稳定结构 D . 最简单氢化物水溶液的 pH : X>M
设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.![]() 金属钠与氧气完全反应生成
金属钠与氧气完全反应生成![]() 与
与![]() 混合物,转移的电子数目为
混合物,转移的电子数目为![]()
B.![]() 和
和![]() 混合气体中所含的分子数目为
混合气体中所含的分子数目为![]()
C.![]() 溶液中
溶液中![]() 的数目为
的数目为![]()
D.标准状况下,![]() 完全溶于水后配成的稀溶液中所含
完全溶于水后配成的稀溶液中所含![]() 的数目为
的数目为![]()
反应 中,氧化产物与还原产物的物质的量之比是( )
中,氧化产物与还原产物的物质的量之比是( )
A. 1:2 B. 1:1 C. 2:1 D. 4:1

A. 分子式为C12H6Cl4O B. 是二氯苯的同系物
C. 其一溴代物有三种 D. 能发生加成反应
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:a>c>b
B.常温下,浓度均为0.1mol/L①醋酸、②盐酸、③醋酸钠溶液,水电离程度的顺序为③>①>②
C.常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为酸性
D.物质的浓度相同的①氯化铵溶液、②硫酸铵溶液、③碳酸氢铵溶液,pH的顺序为:③>①>②
A. 碘水中通入适量的SO2:I2+SO2+2H2O===2I-+SO42-+4H+
B. NH4HCO3溶液与足量NaOH溶液混合后加热:NH4++OH-
C. NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-===BaCO3↓+2H2O+CO32-
D. 向Ca(ClO) 2溶液中通入SO2:Ca2++2ClO-+H2O+SO2===CaSO3↓+2HClO
| 加入的物质 | 结论 |
A | 0.05molCH3COONa固体 |
|
B | 0.05molNaHSO4固体 | c(CH3COO﹣)+c(CH3COOH)=c(Na+)﹣c(SO42﹣) |
C | 0.05molNH4Cl固体 | 水电离程度增大 |
D | 50mLH2O | 由水电离出的c(H+)·c(OH﹣)减小 |
A. A B. B C. C D. D
丹参素是中药丹参的水溶性成分,结构为 F ,具有扩张血管、增加冠脉血流量等作用,某一种合成路线如下图所示:

已知:
(1)丹参素的分子式为____________; D →E 的反应类型是_______________。
(2)试剂X是____________(写化学式);C 中含氧官能团名称为_____________。
(3) A→B 的反应方程式为________________。
(4)G与 E互为同分异构体,请写出满足下列条件的任意两种G的结构简式______________。
①lmolG 能与4molNaOH发生反应;
②能够发生水解反应;
③核磁共振氢谱显示5个吸收峰,且峰面积之比为 1 : 2 : 2 : 2 : 3 。
(5)参考上述流程信息,设计以
(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
(3)

(4)在金属材料中添加

下列实验设计不能达到实验目的的是
| | 实验目的 | 实验设计 |
| A | 检验溶液中 | 取少量待测液,滴加 |
| B | 净化实验室制备的 | 气体依次通过盛有饱和 |
| C | 测定 | 将待测液滴在湿润的 pH 试纸上,与标准比色卡对照 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
A . A B . B C . C D . D

| 气体 | 试剂 | 现象 | 结论 |
A | CH2=CH2 | 溴水 | 溶液褪色 | C2H4能与Br2发生取代反应 |
B | CO2 | BaCl2溶液 | 产生白色沉淀 | CO2能与可溶性钡盐反应 |
C | Cl2 | FeCl2溶液 | 溶液变为棕黄色 | 氧化性Cl2>Fe3+ |
D | SO2 | KMnO4溶液 | 溶液褪色 | SO2有漂白性 |
A. A B. B C. C D. D
A. 原子半径:m>n B. 氢化物的稳定性:n>p
C. q的最高价氧化物的水化物为强酸 D. n在自然界中能以游离态存在
丙烷经催化脱氢可制丙烯 :C 3 H 8 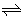

已知:
①C 3 H 8 (g)+5O 2 (g)=3CO 2 (g)+4H 2 O(l) △H=-2220kJ/mol
②C 3 H 6 (g)+9/2O 2 (g)=3CO 2 (g)+3H 2 O(l) △H=-2058kJ/mol
③H 2 (g)+1/2O 2 (g)=H 2 O(l) △H=-286kJ/mol
下列说法不正确的是
A . C 3 H 8 (g)=C 3 H 6 (g)+H 2 (g) △H=+124kJ/mol
B . c(H 2 ) 和 c(C 3 H 6 ) 变化差异的原因: CO 2 +H 2 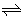
C . 其他条件不变,投料比 c(C 3 H 8 )/c(CO 2 ) 越大, C 3 H 8 转化率越大
D . 若体系只有 C 3 H 6 、 CO 、 H 2 和 H 2 O 生成,则初始物质浓度 c 0 与流出物质浓度 c 之间一定存在: 3c 0 (C 3 H 8 )+c 0 (CO 2 )=c(CO)+c(CO 2 )+3c(C 3 H 8 )+3c(C 3 H 6 )

(1)在上图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由此可得到的结论_______________。
(2)工业上使用下图装置,采用石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为_____。

(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(VI)转化为Cr(III)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O72-的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaC1进行电解,使阳极生成的Fe2+和Cr2O72-发生反应,其离子方程式为___________。阴极上Cr2O72-、H+、Fe3+都可能放电。若Cr2O72-放电,则阴极的电极反应式为_________;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(VI)的废水中加入绿矾,在pH<4时发生反应使Cr(VI)转化为Cr(III),调节溶液pH为6~8,使溶液中的Fe(I)、Fe(Ⅱ)、Cr(III)析出组成相当于Fe(Ⅱ)[Fe(III)x·Cr (III)2-x]O4(铁氧磁体 的沉淀,则铁氧磁体中x=_________。
A. 1mol乙醇完全氧化为乙酸,转移电子数为4NA
B. 标准状况下,22.4L乙烯中含有的共用电子对数目为5NA
C. 3.6gD2O与足量的金属钠反应,生成的D2分子数0.1NA
D. 在1mol/L的NaF溶液中,F—的个数为NA
- 材料一 以十一届三中全会为标志,中国的收入分配制度改革在农村以“家庭联产承包责任制”为突破口,在城市以“奖励和计件工资
- 下图是亚洲东部某区域两个时刻的等压线图(单位:百帕),读图回答5~6题。5.左图中A处等压线的数值可能为 A.1004或
- The prize of the game show is $ 30,000 andan all expenses __
- There is no night-flight to the small town. The service was
- 如图,⊙O的半径OA=3,以A为圆心,OA的长为半径画弧交⊙O于B、C,则BC=.
- 在中国近代史上,北京两次被外国侵略军攻占,两次的侵略者是 ①英美联军 ②英法联军
- 一定量的盐酸跟过量的铁粉反应,为了减缓反应速率且不影响生成H2的总量,可向盐酸中加入适量的( ) A.NaOH(s
- 某企业共有职工150人,其中高级职称15人,中级职称45人,一般职员90人,现采用分层抽样抽取容量为30的样本,则各职称
- 宋代是我国手工业与商业蓬勃发展的时期,历史学家研究发现,宋代民间崇拜的神灵被认为除了具备驱灾治病、报境安民等传统农业社会
- 《汉字英雄》节目制作人马东表示,节目关注青少年对汉字知识与文化传统的认知,体 现汉字之美,而这一切都基于中国人对汉字的感
- 阅读下面的文字,完成1—3题。 林尽水源,便得一山,山有小口,仿佛若有光。便舍船,从口入。初极狭,才通人。复行数十步,豁
- 化简的结果是 .
- 19.补写出下列句子中的空缺部分。 (1)欧阳修在《醉翁亭记》里,“ , ”描绘出了两幅山间
- 每立方厘米的空气质量约为,用小数把它表示为 .
- 下列观点与漫画(右图)中的人所坚持的哲学基本 立场相同的是( ) A. 心中有笼,便有笼;心中无笼,便无笼 B. 未
- The backpack is very . I can’t afford it.A. expensive
- 下列关于实验现象的描述不正确的是 A.把铜
- 给小鼠注射一定剂量的胰岛素后,小白鼠进入休克状态,要使其复苏,可适量注射的物质是
- 我们生活中的很多现象,往往蕴涵了地理知识。下列现象与地球自转有关的是 ( ) A.盐城四季分明,春暖、夏热、秋凉、
- 下列各项中,不属于以为首的中共第一代领导人共同在社会主义改造和建设道路上的有益探索的是
 减小
减小



