高考化学试题
A. 将2mol 二氧化硫和1mol 氧气通入密闭容器中,在一定条件下充分反应,转移电子数为4NA
B. 常温下,44g CO2中含有2NA个碳氧双键
C. 标准状况下,0.1mol Al3+含有的核外电子数为0.3NA
D. 室温下,1LpH=13的氢氧化钡溶液所含氢氧根离子数为0.2NA

下列说法错误的是
A. 放电时,Cl-向X极移动
B. 该电池充电时Y极应该与电源的正极相连
C. 充电时,阴极反应为:NaTi2(PO4)3+xNa++xe-=Na1+ xTi2( PO4)3
D. 该电池可能作为可植入人体的电子医疗设备的电源
A. 绿色化学的核心是在化学合成中将原子充分利用,转化为新的原子
B. 二氧化硅可作为制造宇宙飞船太阳能电池帆板的主要材料
C. 燃煤中添加适量CaO可减少SO2排放量,燃烧中硫元素转化为CaSO4
D. 生活中常见的金属镁、铝、铁、铜等均能通过热还原法冾炼
| A | B | C | D |
c(I2)/mmol•L-1 | 1.00 | 0.22 | 0.44 | 0.11 |
c(H2)/mmol•L-1 | 1.00 | 0.22 | 0.44 | 0.44 |
c(HI)/mmol•L-1 | 1.00 | 1.56 | 4.00 | 1.56 |
A. A B. B C. C D. D
A.
B.
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D.
苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
![]() +KMnO4→
+KMnO4→ + MnO2
+ MnO2 +HCl→
+HCl→ +KCl
+KCl
| 名称 | 相对分 子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL−1) | 溶解性 |
| 甲苯 | 92 | −95 | 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
| 苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | —— | 微溶于冷水,易溶于乙醇、热水 |
实验步骤:
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶液,用0.01000 mol·L−1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为______(填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)在反应装置中应选用______冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,其判断理由是______。
(3)加入适量饱和亚硫酸氢钠溶液的目的是___________;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理__________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是_______。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______。
(6)本实验制备的苯甲酸的纯度为_______;据此估算本实验中苯甲酸的产率最接近于_______(填标号)。
A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中__________的方法提纯。

请回答下列问题:
(1)操作①应包括下列操作中的____________。(填序号)
A.溶解 B.过滤 C.蒸馏 D.分液 E.蒸发结晶
(2)用氨水调节pH至8~9的目的是_________________________________。
(3)若测得滤液C中c(CO32-)=10-3mol/L,则Ca2+____(填“是”或“不”)沉淀完全。[已知c(Ca2+)≤10-5 mol/L时即可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(4)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中c(NH4+) _______c(NO3-)(填“≥”、“≤”、“<”、“>”或“=”)。
(5)操作②是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9~11,才出现大量沉淀。写出该反应的化学方程式_________________________;用简要的文字解释用氢氧化钠调节pH至9~11的原因____________。
(6)已知大理石含CaCO3的质量分数为a,m g大理石可以制得n g CaO2,请计算:CaCO3 转化为CaO2过程中,Ca原子的利用率__________________。
赖氨酸 ![]() 是人体必需氨基酸,其盐酸盐 (H 3 RCl 2 ) 在水溶液中存在如下平衡: H 3 R 2+
是人体必需氨基酸,其盐酸盐 (H 3 RCl 2 ) 在水溶液中存在如下平衡: H 3 R 2+ 

R - 。向一定浓度的 H 3 RCl 2 溶液中滴加 NaOH 溶液,溶液中 H 3 R 2+ 、 H 2 R + 、 HR 和 R - 的分布系数 δ(x) 随 pH 变化如图所示。已知 δ(x)=
,下列表述正确的是

A . 
B . M 点, c (Cl - ) + c (OH - )+ c (R - )=2 c (H 2 R + )+ c (Na + )+ c (H + )
C . O 点, pH=
D . P 点, c (Na + )> c (Cl - )> c (OH - )> c (H + )

A. 加入适量硫酸钠的作用是增加离子浓度,增强溶液的导电能力
B. 电解过程中阳极附近溶液的pH降低
C. 电解过程中,溶液中的Cl-经阳离子交换膜向阳极移动
D. ClO-氧化Ni2+的离子方程式为:ClO-+H2O+2Ni2+=Cl-+2Ni3++2OH-




A. A B. B C. C D. D
A. CuCl2 B. CuSO4 C. Cu2(OH)2CO3 D. Cu(OH)2

已知:

请回答下列问题:
(1)A的名称是_______________,C中含氧官能团名称是______________。
(2)写出反应类型:A→B______________,C→D__________________。
(3)B→C的反应试剂和反应条件是______________________。
(4)D+E→F的反应方程式是_________________。
(5)G的分子式是____________________。
(6)满足下列条件的F的同分异构体共有__________种( 不考虑立体异构)。
a.苯环上有两个取代基,无其他环状结构;b.含碳碳三键,无-C≡COH结构。
(7)多环化合物是有机研究的重要方向,请设计由
 的路线(无机试剂任选)______________
的路线(无机试剂任选)______________

请回答下列问题:
(1)《天工开物》中炼锌的方法中利用了木炭的____ 性。
(2)滤渣1和滤渣3的主要成份分别是______、______(填化学式)。
(3)“溶浸”时,氧化锌参与反应的相关离子方程式是______;“溶浸”时温度不宜过高,其原因是______。
(4)“氧化除杂”的目的是将AsCl52-转化为As2O5胶体,再经吸附聚沉除去,该反应的离子方程式是______。
(5)“电解”含 [Zn(NH3)4]2+的溶液,阴极放电的电极反应式是______。阳极区产生一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是_____(写化学式)。该流程中可以循环使用的物质是_____(写化学式)。

A. BOH属于弱碱
B. BOH的电离常数K=1×10-4.8
C. P点所示的溶液中:c(Cl-)>c(B+)
D. N点所示的溶液中:c(H+)=c(Cl-)+c(OH-)-c(BOH)
废旧太阳能电池 CIGS 具有较高的回收利用价值,其主要组成为 CuIn 0.5 Ga 0.5 Se 2 。某探究小组回收处理流程如图:

回答下列问题:
( 1 ) 硒 (Se) 与硫为同族元素, Se 的最外层电子数为 ___ ;镓 (Ga) 和铟 (In) 位于元素周期表第 IIIA 族, CuIn 0.5 Ga 0.5 Se 2 中 Cu 的化合价为 ___ 。
( 2 ) “ 酸浸氧化 ” 发生的主要氧化还原反应的化学方程式为 ____ 。
( 3 ) 25 ℃时,已知: K b (NH 3 ·H 2 O)≈2.0×10 -5 , ![]() ,
, ![]() ,
, ![]() , “ 浸出液 ” 中 c(Cu 2+ )=0.01mol·L -1 。当金属阳离子浓度小于 1.0×10 -5 mol·L -1 时沉淀完全, In 3+ 恰好完全沉淀时溶液的 pH 约为 ___ ( 保留一位小数 ) ;若继续加入 6.0mol·L -1 氨水至过量,观察到的实验现象是先有蓝色沉淀,然后 ___ ;为探究 Ga(OH) 3 在氨水中能否溶解,计算反应
, “ 浸出液 ” 中 c(Cu 2+ )=0.01mol·L -1 。当金属阳离子浓度小于 1.0×10 -5 mol·L -1 时沉淀完全, In 3+ 恰好完全沉淀时溶液的 pH 约为 ___ ( 保留一位小数 ) ;若继续加入 6.0mol·L -1 氨水至过量,观察到的实验现象是先有蓝色沉淀,然后 ___ ;为探究 Ga(OH) 3 在氨水中能否溶解,计算反应 ![]() 的平衡常数 K= ___ 。
的平衡常数 K= ___ 。
( 已知: ![]()
( 4 ) “ 滤渣 ” 与 SOCl 2 混合前需要洗涤、干燥,检验滤渣中 SO 
( 5 ) “ 高温气相沉积 ” 过程中发生的化学反应方程式为 ___ 。
设 为阿伏加德罗常数的值。下列说法正确的是
A . 
键的数目为
B . 

C . 

D . 

分子数目为
A. 简单离子半径:X>Y>Z
B. 氢化物的沸点:W<X
C. 化合物P中既含有离子键又含有共价键
D. W、X、Y三种元素形成的物质的水溶液显碱性
(1)二氧化碳加氢制甲醇的总反应可表示为:
该反应一般认为通过如下步骤来实现:
①
②
总反应的
A.
 B.
B.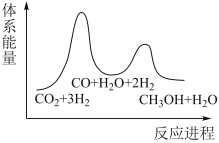 C.
C.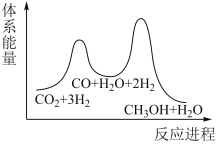 D.
D.
(2)合成总反应在起始物
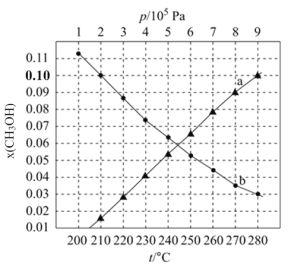
①用各物质的平衡分压表示总反应的平衡常数,表达式
②图中对应等压过程的曲线是_______,判断的理由是_______;
③当
A. 离子半径:E>F>D>C>A
B. 含氧酸的酸性可能为:B>E
C. A、B、F形成的某种化合物可使澄清石灰水变浑浊
D. A与C形成的化合物溶于水显酸性

A. 直线b、d分别对应H+、OH-
B. pH=6时,c(HAc)>c(Ac-)>c(H+)
C. HAc电离常数的数量级为10-5
D. 从曲线a与c的交点可知pKa=pH=4.74
- 下列表示纯合体的基因型是( ) A.AaXHXH B.AABb
- 初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣═H2O.如图,像这种用实际参加反应的离子符号来表示反应的式
- 在5 000多年的历史发展中,中华民族创造了辉煌灿烂的中华文化,其中的许多思想和精神至今仍然熠熠生辉,影响着一代又一代的
- — Would you please pass me something to drink?— What about s
- 阅读下列材料: 启蒙运动在人类历史上产生了深远影响,其天赋人权观、法律与法治观、三权分立的政治学说至今为许多国家所推祟。
- 听觉形成的正常途径是( ) A.声波→鼓膜→听小骨→耳蜗内的听觉感受器→听神经→大脑皮层的听觉中枢 B.声波→鼓室→
- 下列欧洲气候类型中,亚洲缺少的是( )A.地中海气候 B.温带海洋
- 下列都是生活中常见的物质,由物质分类知识可知,属同一类物质的一组是 ( ) A.红
- 中欧光伏贸易争端是中欧贸易史上涉案金额最大的贸易摩擦案,经过中欧双方长达一个多月艰苦、细致的谈判,2013年7月27日,
- 下表为元素周期表前三周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是A.常压下五种元素的单质中Z单质的
- 已知:2Fe2++Br2====2Fe3++2Br-。请按要求写出下列各反应的离子方程式:(1)在FeBr2溶液中通入少
- 根据下面一段材料,概括说明“通货紧缩”产生的原因。(不超过30字) 虽然通货膨胀已经退潮了,但通货紧缩却正向我们逼近,越
- 求不等式组的整数解。
- 下列气体与氧气混合充入密闭容器中,在150 ℃时引爆,再冷却到150 ℃时,容器内气体压强不变的是( ) A.甲烷
- 下列各句中,没有语病的一句是( ) A.市民可凭有效身份证到园博园游客咨询服务中心免费租用一台语言导览器,收听专业
- 用分子的相关知识解释下列生活中的现象,其中错误的是() A.热胀冷缩,说明分子的大小随温度升降而改娈 B.“酒香不怕巷子
- 据史书记载,我国人口从汉代以来大体在五六千万左右,清康熙末年只有两三千万,乾隆五十九年激增至三亿多,道光十四年(1834
- 函数,在定义域上表示的曲线过原点,且在处的切线斜率均为.有以下命题: ①是奇函数;②若内递减,则的最大值为4;③的最大值
- 某同学欲采用下列器材研究一个额定电压约2.5V的小灯泡的伏安特性曲线。A.直流电源(3V,内阻不计); B.电流表(0~
- 在等式中,当时, ( )。 A、23 B、-13 C、-5



