吸热反应和放热反应 知识点题库
下列说法正确的是( )
A . 在化学反应过程中,发生物质变化的同时不一定发生能量变化
B . 硝酸铵溶于水温度降低,这个过程吸热热量
C . 同温同压下,H2和Cl2在光照和点燃条件下的△H不同
D . 自发反应的熵一定增大,非自发反应的熵一定减小
下列属于吸热反应的是( )
①冰雪融化 ②KMnO4分解制O2 ③铝与氧化铁的反应 ④钠与水反应 ⑤二氧化碳与灼热木炭反应 ⑥碘的升华 ⑦Ba(OH)2•8H2O和NH4Cl反应.
A . ②⑥⑦
B . ②⑤⑦
C . ①②⑤⑥⑦
D . ③④
下列反应中属吸热反应的是( )
A . 镁与盐酸反应放出氢气
B . 氢氧化钠与盐酸的反应
C . 硫在空气或氧气中燃烧
D . Ba(OH)2•8H2O与NH4Cl反应
如图所示,把下列物质分别加入装有水的锥形瓶里,立即塞紧带有U形管的塞子,已知U形管内预先装有少量水(为方便观察,预先将水染成红色),结果U形管左边液面升高,则加入的物质可能是( )
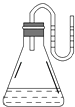
A . NaOH固体
B . 浓硫酸
C . NH4NO3晶体
D . Na2O2固体
下列反应属于吸热反应的是( )
A . Mg与盐酸反应
B . NH4Cl的分解反应
C . Na在Cl2燃烧
D . NaOH溶液与CH3COOH溶液反应
某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图1所示(实验中始终保持V1+V2=50mL).回答下列问题:
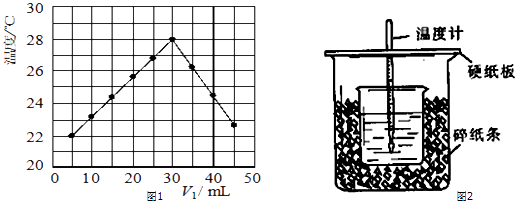
-
(1) 研究小组做该实验时环境温度(填“高于”、“低于”或“等于”)22℃.
-
(2) 由题干及图形可知,V1:V2=时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为mol/L
-
(3) 若通过实验测定及有关计算知此反应共放出Q KJ的热量,请写出此反应的热化学方程式:
-
(4) 请简要说明图2装置的不足之处.
在一定固定容积的密闭容器中,CO2(g)与一定量的C(s)发生进行如下化学反应:CO2(g)+C(s)⇌2CO(g).
①该反应为反应(填“吸热”或“放热”).
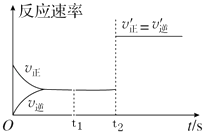
②该反应的反应速率随时间的变化图象如图所示,则下列说法正确的是(填序号).
a.t1时刻该反应已经处于化学平衡状态
b.t2时刻c(CO2)=c(CO)
c.t2时刻该反应仍然处于化学平衡状态
d.t2时刻,改变的条件可能是增大了C的物质的量.
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下:
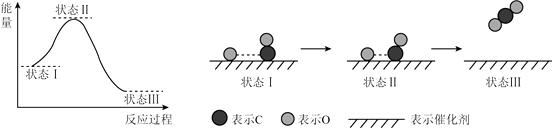
下列说法正确的是( )
A . CO和O生成CO2是吸热反应
B . 在该过程中,CO断键形成C和O
C . CO和O生成了具有极性共价键的CO2
D . 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
下列化学反应的能量变化与下图不符合的是( )
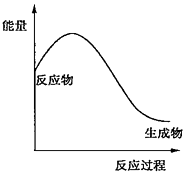
A . 2NH4Cl+Ca(OH)2  2NH3↑+CaCl2+2H2O
B . 2Al+Fe2O3
2NH3↑+CaCl2+2H2O
B . 2Al+Fe2O3  2Fe+Al2O3
C . Mg+2HCl=MgCl2+H2↑
D . C+O2
2Fe+Al2O3
C . Mg+2HCl=MgCl2+H2↑
D . C+O2  CO2
CO2
 2NH3↑+CaCl2+2H2O
B . 2Al+Fe2O3
2NH3↑+CaCl2+2H2O
B . 2Al+Fe2O3  2Fe+Al2O3
C . Mg+2HCl=MgCl2+H2↑
D . C+O2
2Fe+Al2O3
C . Mg+2HCl=MgCl2+H2↑
D . C+O2  CO2
CO2
下列反应一定属于放热反应的是( )
A . 氢氧化钡晶体和氯化铵晶体的反应
B . 反应物能量比生成物能量低的反应
C . 化学键断裂吸收的能量比化学键形成放出的能量少的反应
D . 不需要加热就能发生的反应
下列说法正确的是( )
A . 化学反应中的能量变化都表现为热量的变化
B . 吸热反应在不加热的条件下一定不能发生
C . 需要加热才能发生的反应一定是吸热反应,放热反应在常温下一定很容易发生
D . 反应是吸热还是放热必须看旧键断裂时吸收的能量和新键形成时释放的能量的大小
下列反应中,生成物所储存的化学能比反应物所储存的化学能多的是( )
A . 2Na2O2 + 2H2O = 4NaOH + O2↑
B . NaOH + HCl = NaCl + H2O
C . CH4 + 2O2 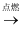 CO2 + 2H2O
D . Ba(OH)2·8H2O + 2NH4Cl = BaCl2 + 2NH3↑ + 10H2O
CO2 + 2H2O
D . Ba(OH)2·8H2O + 2NH4Cl = BaCl2 + 2NH3↑ + 10H2O
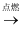 CO2 + 2H2O
D . Ba(OH)2·8H2O + 2NH4Cl = BaCl2 + 2NH3↑ + 10H2O
CO2 + 2H2O
D . Ba(OH)2·8H2O + 2NH4Cl = BaCl2 + 2NH3↑ + 10H2O
下列变化符合图示的是( )
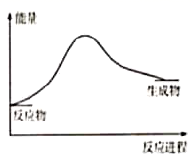
①冰雪融化 ②KMnO4分解制O2 ③铝与氧化铁的反应 ④钠与水反应 ⑤二氧化碳与灼热的木炭反应 ⑥碘的升华 ⑦Ba(OH)2·8H2O和NH4Cl的反应.
A . ②⑥⑦
B . ②⑤⑦
C . ①②⑤⑥⑦
D . ③④
化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化如图所示,则下列说法中正确的是( )
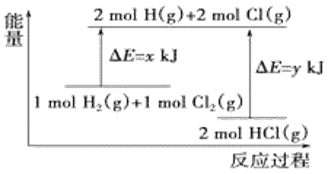
A . 该反应是吸热反应
B . 断裂1molH-H键和1molCl-Cl键时能放出x kJ的能量
C . 断裂2molH-Cl键时需要吸收y kJ的能量
D . 2molHCl(g)的总能量高于1molH2(g)和1molCl2(g)的总能量
我国古代典籍中记载了许多劳动人民对化学知识的认识。下列有关说法正确的是( )
A . “丹砂烧之成水银,积变又还成丹砂”中“烧”的过程有单质硫生成
B . “凡石灰经火焚炼为用。成质之后,入水永劫不坏”中所有反应均为放热反应
C . “胡粉(碱式碳酸铅)投火中,色坏还为铅”中“色坏还为铅”过程为分解反应
D . “以火烧之,紫青烟起,乃真硝石也”中的“硝石”主要成分为NaNO3
下列说法正确的是( )
A . 已知2SO2(g)+O2(g)  2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
C . 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
D . 若1molSO2与0.5molO2反应生成SO3放出的热量为47.8kJ,则该反应的热化学方程式可表示为2SO2(g)+O2(g)
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
C . 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
D . 若1molSO2与0.5molO2反应生成SO3放出的热量为47.8kJ,则该反应的热化学方程式可表示为2SO2(g)+O2(g)  2SO3(g) ΔH=-95.6 kJ∙mol−1
2SO3(g) ΔH=-95.6 kJ∙mol−1
 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
C . 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
D . 若1molSO2与0.5molO2反应生成SO3放出的热量为47.8kJ,则该反应的热化学方程式可表示为2SO2(g)+O2(g)
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
C . 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
D . 若1molSO2与0.5molO2反应生成SO3放出的热量为47.8kJ,则该反应的热化学方程式可表示为2SO2(g)+O2(g)  2SO3(g) ΔH=-95.6 kJ∙mol−1
2SO3(g) ΔH=-95.6 kJ∙mol−1
下列变化中属于吸热的化学反应的是( )
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A . ①②
B . ②③
C . ①④⑤
D . ②④
沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,可用来点火做饭。已知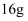 甲烷完全燃烧生成液态水时放出
甲烷完全燃烧生成液态水时放出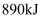 热量。下列说法错误的是( )
热量。下列说法错误的是( )
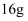 甲烷完全燃烧生成液态水时放出
甲烷完全燃烧生成液态水时放出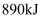 热量。下列说法错误的是( )
热量。下列说法错误的是( )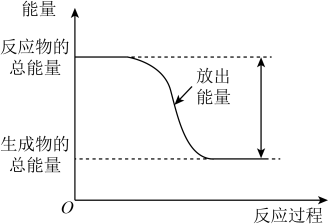
A . 沼气属于可再生能源
B . 沼气的主要成分是 C . 反应生成气态水时放出的热量大于
C . 反应生成气态水时放出的热量大于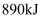 D . 反应过程中能量变化可用图表示
D . 反应过程中能量变化可用图表示
 C . 反应生成气态水时放出的热量大于
C . 反应生成气态水时放出的热量大于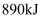 D . 反应过程中能量变化可用图表示
D . 反应过程中能量变化可用图表示
某同学利用如图装置模拟工业生产制备少量硝酸,请结合所学知识完成下列问题。
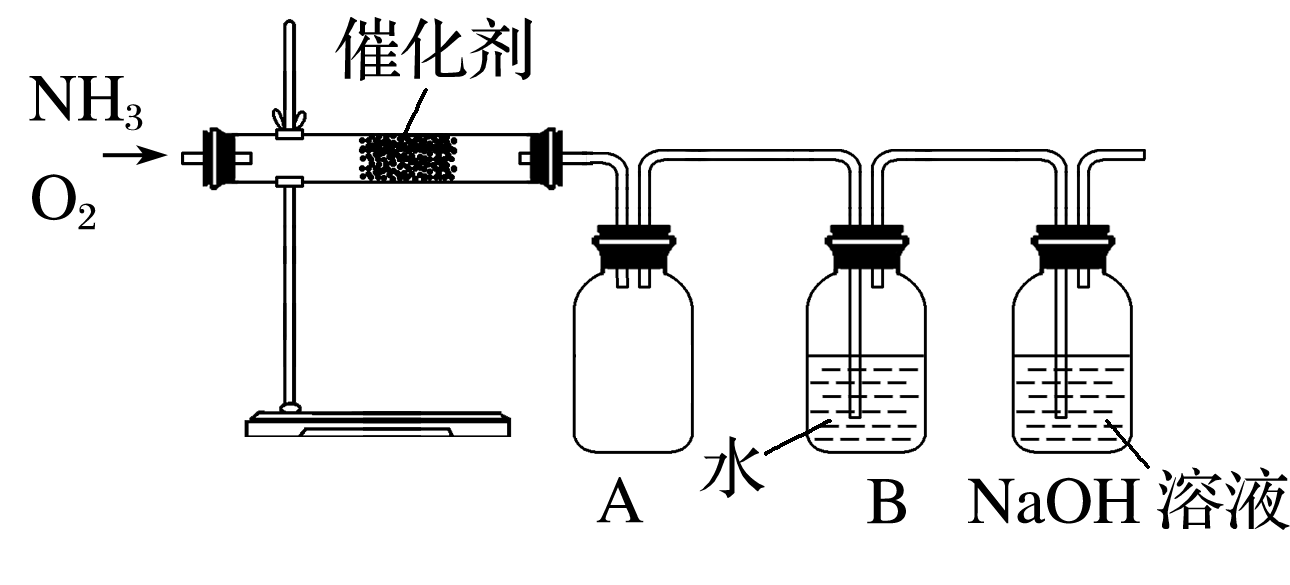
-
(1) 实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是____(填字母)。A .
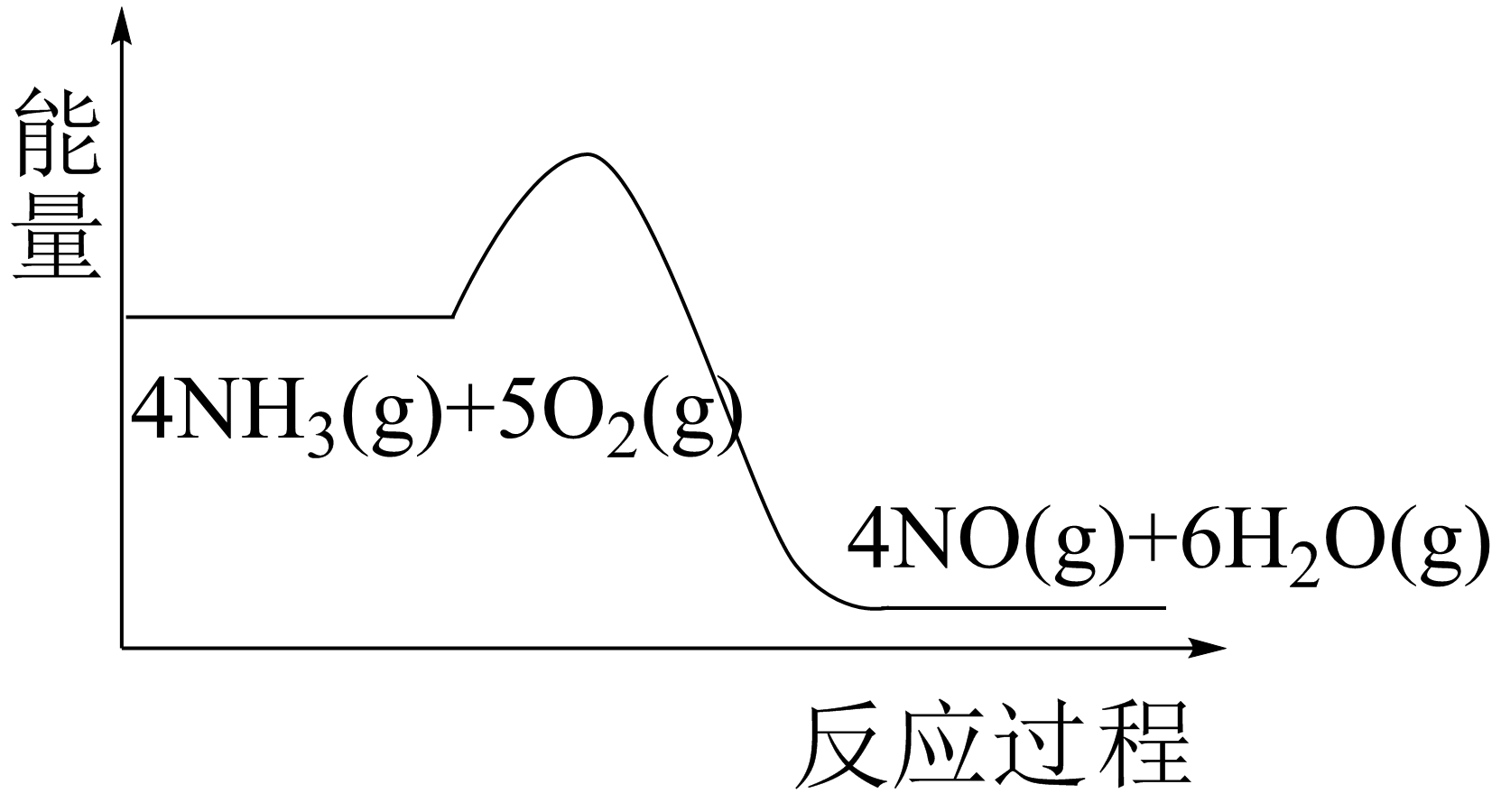 B .
B . 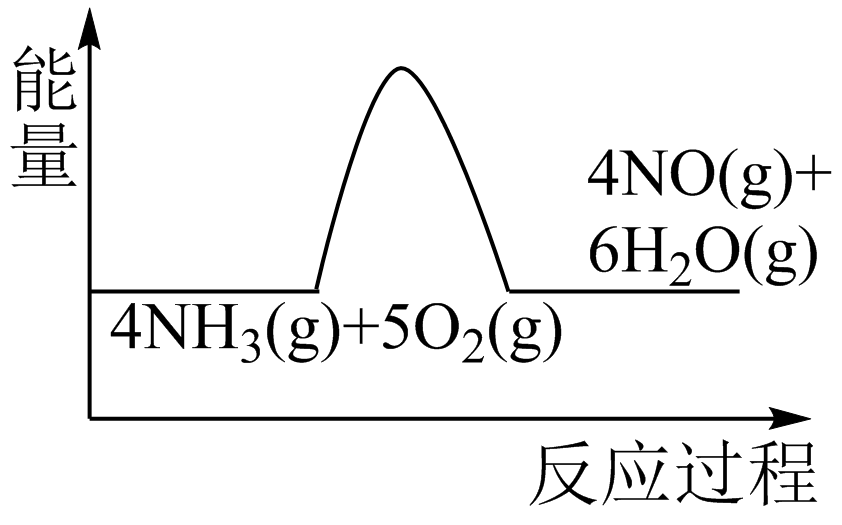 C .
C . 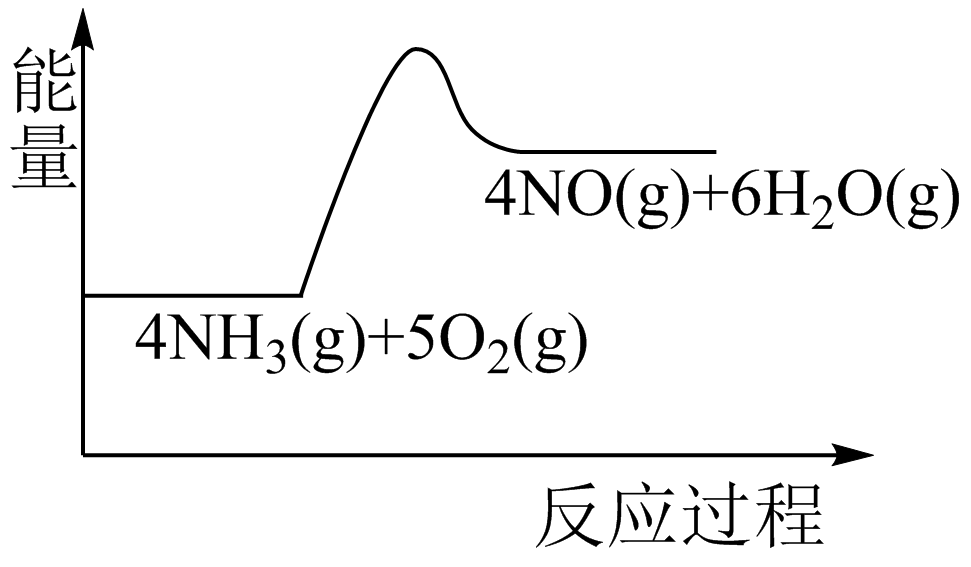
-
(2) 高温时,
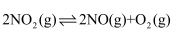 , 因此氨气与氧气反应难以生成
, 因此氨气与氧气反应难以生成 。根据下列1mol物质断键时的能量数据计算,当
。根据下列1mol物质断键时的能量数据计算,当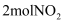 完全分解时,反应会(填“吸收”或“放出”)kJ能量。
完全分解时,反应会(填“吸收”或“放出”)kJ能量。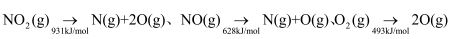
-
(3) 在2L的恒温密闭容器中,发生反应
 , 通入等物质的量的NO和
, 通入等物质的量的NO和 气体,n(NO)随时间的变化如下表:
气体,n(NO)随时间的变化如下表:t/s
0
1
2
3
4
5
n(NO)/mol
0.020
0.012
0.008
0.005
0.004
0.004
①某同学由数据推测,反应在第4s时恰好到达平衡状态。该推测(填“正确”或“错误”)
②在第5s时,
 的转化率为。
的转化率为。③容器中混合气体压强与反应开始时的压强比值为。
在体积为2L的恒容密闭容器中发生反应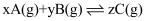 , 图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是( )
, 图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是( )
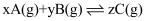 , 图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是( )
, 图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是( )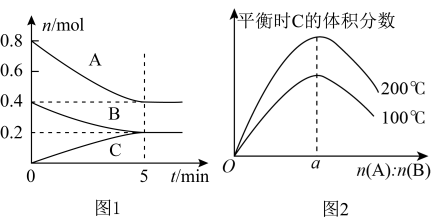
A . 200℃时,反应从开始到平衡的平均速率v(B)=0.04mol·L-1·min-1
B . 由图可知反应的化学方程式为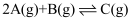 , 且正反应吸热,a=1
C . 若在图1所示的平衡状态下再向体系中充入0.2mol B和0.2mol C,此时v正=v逆
D . 200℃时,向2L恒容密闭容器中充入2mol A和1mol B,达到平衡时A的体积分数小于0.5
, 且正反应吸热,a=1
C . 若在图1所示的平衡状态下再向体系中充入0.2mol B和0.2mol C,此时v正=v逆
D . 200℃时,向2L恒容密闭容器中充入2mol A和1mol B,达到平衡时A的体积分数小于0.5
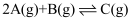 , 且正反应吸热,a=1
C . 若在图1所示的平衡状态下再向体系中充入0.2mol B和0.2mol C,此时v正=v逆
D . 200℃时,向2L恒容密闭容器中充入2mol A和1mol B,达到平衡时A的体积分数小于0.5
, 且正反应吸热,a=1
C . 若在图1所示的平衡状态下再向体系中充入0.2mol B和0.2mol C,此时v正=v逆
D . 200℃时,向2L恒容密闭容器中充入2mol A和1mol B,达到平衡时A的体积分数小于0.5
最近更新
- (本小题满分12分)(改编题) 设数列的各项都是正数, 且对任意都有记为数列的前n项和(1) 求证: ;(2) 求数列的
- 在第十一届全国运动会开幕式上,艺术地再现了山东“一山一水一圣人”的文化特色。其中“圣人”指的是 A.孔子
- 已知f(x)= (x∈R,且x≠-1),g(x)=x2+2(x∈R). (1)求f(2)、g(2)的值; (2)求f[g
- (2014·安徽文综·16)图5是反映新民主主义革命时期重大历史事件的示意图。符合历史发展进程的时序是()①
- Whether dying patients behelped to end their lives is
- 关于文化的叙述,正确的是 ①自然界的阳光、空气、山峰、河流都是文化的一部分 ②山川林木一旦经过人类开发成为景观,就成了文
- 如图6-8-22所示,一根长0.1 m的细线,一端系着一个质量是0.18 kg的小球,拉住线的另一端,使球在光滑的水平桌
- 为防止某突发事件发生,有甲、乙、丙、丁四种相互独立的预防措施可供采用,单独采用甲、乙、丙、丁预防措施后此突发事件不发生的
- 已知函数,若存在实数,当时恒成立,则实数的最大值为 A. B. C
- 已知函数f(x)=-sin(2x+)+6sinxcosx-2cos2x+1,x∈R. (I)求f(x)的最小正周期; (
- 在正三棱柱ABC—A1B1C1中,已知AB=1,D在棱BB1上,且BD=1,则AD与平面AA1C1C所成角的余弦值是
- 已知抛物线. (1)若圆心在抛物线上的动圆,大小随位置而变化,但总是与直线相切,求所有的圆都经过的定点坐标; (2)抛物
- 下列是除去括号内杂质的有关操作,正确的有( )A.苯(苯酚):加浓溴水、振荡、分液B.肥皂液(甘油):加食盐凝聚,
- 化学就在我们身边,它与我们的生活息息相关。 (1)在“石墨、氮气、碳酸氢钠、碳酸钙”中选择适当的物质填空: ①用于填充食
- 关于各元素相对含量说法正确的是 A.地壳中含量最高的元素是氧 B.海洋中含量最高的元素是氯
- 中国近代民族资产阶级不断探索救国之路,他们在从西方思想中寻找武器的同时,又从本民族的文化中寻找可资利用的思想材料。下列属
- 根据行为的发生可分为 行为和 行为.
- (本题满分15分) 设椭圆的左焦点为F,上顶点为A,直线AF的倾斜角为(1)求椭圆的离心率;(2)设过点A且与AF垂直的
- 唐代和宋代都有谏官。唐代谏官由宰相荐举,主要评议皇帝得失;宋代谏官由皇帝选拔,主要评议宰相是非。这说明 A. 唐代君主的
- 在图 所示的电路中,闭合电键 S 灯 L 不亮,电压表 V 有示数。已知电路中各处均接触良好,除灯 L 和电阻 R 外,



