第二节 富集在海水中的元素--氯 知识点题库
-
(1) 利用上述原理所得碳酸氢钠晶体中,可能含有的杂质离子有Cl﹣和NH4+ , 实验室鉴定Cl﹣所选用的试剂是 、 ,鉴定另一种杂质离子的方法是
-
(2) 碳酸氢钠晶体受热分解可得到纯碱,其化学反应方程式为
-
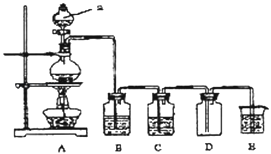
(1) 发生装置A中制取氯气的化学方程式.
-
(2) 利用上图装置制备纯净的氯气,并证明氧化性:Cl2>Fe3+
则装置B中的溶液的作用是;装置D中加的最佳试剂是(填序号):供选试剂:a.浓H2SO4 b.FeCl2溶液 c.无水氯化钙 d.KSCN与FeCl2的混合溶液
-
(3) 在图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的(填溶液名称),E中加入溶液(填化学式).
-
(4) 证明碳元素的非金属性比硅元素的强的现象为;实验2不严谨之处应如何改进.
-
(1) 写出该反应的化学方程式.
-
(2) 若要制取纯净干燥的氯气,应使气体依次通过装有和的洗气瓶.
-
(3) 该小组称取8.7g二氧化锰与足量10mol•L﹣1的浓盐酸反应,理论上可制得氯气的体积(标准状况)V1=L.
-
(4) 若该小组量取了10mol•L﹣1的浓盐酸40mL,与足量的二氧化锰反应,理论上产生氯气的体积为V2(标准状况),则V1V2(填“>”、“=”或“<”)
-
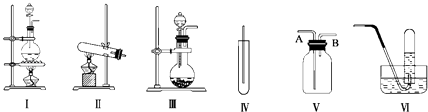
(1) 若用MnO2与浓盐酸反应制取氯气,应选用发生装置,用化学方程式表示制取氯气的反应原理是.
-
(2) 若用KMnO4与浓盐酸反应制取氯气,应选用发生装置,试完成并配平下列离子方程式:MnO4﹣+Cl﹣+H+═Mn2++
Cl2↑+.
-
(3) 若选用MnO2与浓盐酸反应制取的氯气含有杂志气体和.可以选择装置来除杂,装置中盛放的溶液依次为和.
-
(4) 若选用Ⅳ为氯气的收集装置,应该在试管口放置一团棉花,该棉花团应
用溶液浸湿,其作用是.
-
(5) 若选用Ⅴ为氯气收集装置,则氯气应从口通入.用化学方法检验氯气收集满了的方法是
-
(6) 氯气有毒,可选择通过溶液来处理尾气.发生的离子方程式为.
-
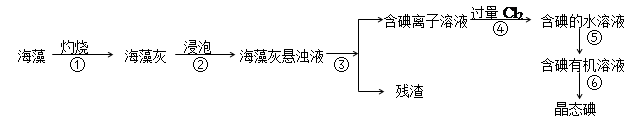
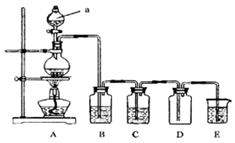
(1) 指出上述提取碘的过程中有关实验操作的名称:
步骤③,步骤⑤。
-
(2) 写出步骤④对应反应的离子方程式:。
-
(3) 步骤④除了加入过量Cl2 , 下列氧化剂最好选用_____________(填代号)。A . 浓硫酸 B . H2O2溶液 C . KMnO4溶液
-
(4) 提取碘的过程中,可供选择的有机试剂是_________________________。(填编号)A . 酒精 B . 醋酸 C . 四氯化碳 D . 苯
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2 , 在碱性溶液中较稳定。
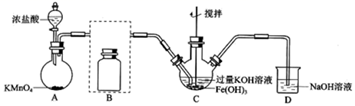
制备K2FeO4(夹持装置略)
-
(1) A为氯气发生装置,A中反应离子方程式是:_。
-
(2) 将除杂装置B补充完整并标明所用试剂。_。
-
(3) C中得到紫色固体和溶液。C中Cl2发生的反应有:3Cl2+2Fe(OH)3+10KOH→2K2FeO4+6KCl+8H2O,另外还有:_。
-
(4) 已知Cl2与KOH在较高温度下反应生成KClO3。为了保证生产KClO,在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是:_、。
探究K2FeO4的性质
-
(5) 高铁酸钾常用于工业废水与城市生活污水的处理,可用作高效水处理剂,表现在水中与污染物作用的过程中,经过一系列反应,由六价降至三价后,能对水产生净化作用的原因是(结合离子方程式回答):。
-
(6) 取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2 , 为证明是否K2FeO4氧化了Cl-而产生Cl2 , 设计以下方案:
方案I
取少量a,滴加KSCN溶液至过量,溶液呈红色
方案II
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生
i.由方案I中溶液变红可知a中含有离子,但该离子的产生不能判断一定K2FeO4将Cl-氧化,还可能由_产生(用离子方程式表示)。
ii.方案II可证明K2FeO4氧化了Cl-。
-
(7) 用KOH溶液洗涤的目的是_。
-
(8) 根据K2FeO4的制备实验得出:氧化性Cl2FeO42-(填“>”或“<”),而方案II实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是_。
-
(9) 资料表明,酸性溶液中的氧化性FeO42->MnO42- , 验证实验如下:
将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO42->MnO42- , 若能,请说明理由;若不能,进一步设计实验方案,理由或方案:。
-
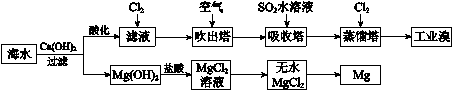
(1) 写出用A制取氯气的化学方程式。
-
(2) 利用上图装置制备纯净的氯气,并证明氧化性:Cl2>Fe3+ , 则装置B中的溶液的作用是;装置D中加的最佳试剂是(填序号)。
供选试剂:
a.浓H2SO4 b.FeCl2溶液 c.KSCN与FeCl2的混合溶液 d.无水氯化钙
-
(3) 在上图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
为了同时完成实验1和实验2,B→E中的试剂分别为:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的(填溶液名称),E中加入溶液(填化学式)。
-
(4) 证明碳元素的非金属性比硅元素的强的现象为。

-
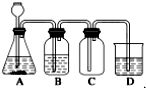
(1) 装置A中反应的离子方程式是。
-
(2) 装置B的作用是。
-
(3) 装置C中盛放的物质是。
-
(4) 装置D用于收集Cl2 , 请将图中装置D的导气管补充完整。
-
(5) 装置E用于吸收尾气,E中反应的离子方程式是。
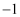 价离子
B . 都只能从海洋中提取
C . 单质熔沸点依次上升
D . 气态氢化物稳定性依次减弱
价离子
B . 都只能从海洋中提取
C . 单质熔沸点依次上升
D . 气态氢化物稳定性依次减弱
|
|
|
|
|
|
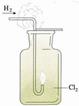
A.纯净的 H2 在 Cl2 中安静地燃烧,发出苍白色火焰,瓶口出现白雾 |
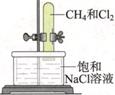
B.光照一段时间,试管内黄绿色变浅, 内壁出现油状液滴,试管内水面上升 |
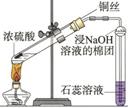
C.将铜丝插入浓硫酸 中,加热试管,产生的气体通入石蕊溶液中,溶液先变红后褪色 |
D.打开弹簧夹,挤压 预先吸入水的胶头滴管,烧杯中的水沿导管进入烧瓶,形成喷泉 |
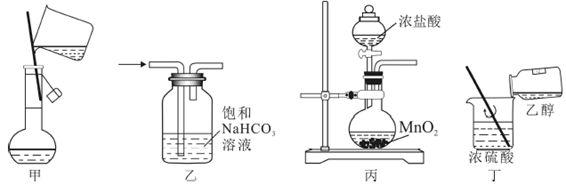
 固体置于100mL甲容器中,加水至刻度,配制
固体置于100mL甲容器中,加水至刻度,配制 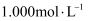
 溶液
B . 用装置乙除去实验室所制
溶液
B . 用装置乙除去实验室所制  中的少量
中的少量  C . 实验室用丙装置制备氯气
D . 丁装置用于混合浓硫酸和乙醇
C . 实验室用丙装置制备氯气
D . 丁装置用于混合浓硫酸和乙醇
- For quite students, their teacher’s advice is more im
- 已知二次函数y1=x2-x-2和一次函数y2=x+1的两个交点分别为A(-1,0),B(3,4),当y1>y1时,自变量
- Frankly, I very much appreciate myself. Yes, I admit I’m in
- 阅读下面的材料,按要求作文。 仰望,从某种意义上说是一种精神上昂的生存姿态,它使生命战栗、贯注、凝神……仰望,就是漫漫黑
- 手握一根水平绳的一端上下抖动,在t时刻绳上呈现的波形如图12-1-3所示.如果绳上C点此时的速度是向下的,则人手握住的是
- 下列各句中,没有语病的一项是( ) A.四川成都一带的乡镇企业之所以发展这么快,是因为抓准了商机,生产的产品适
- 改革开放以来,我国逐渐完善了社会主义初级阶段基本经济制度,经济持续快速发展。如2000年到2012年,国有和集体工业企业
- China is known _________ greatly in terms of its cultural va
- 中国开始走向海洋的重要标志是
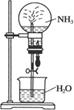
- 如下图所示,在a烧杯中盛有浓氨水,在b烧杯中盛有酚酞溶液,有关现象和解释正确的是
- 设函数f(x)=是奇函数(a,b,c都是整数),且f(1)=2,f(2)<3,f(x)在[1,+∞)上单调递增.(1)求
- 中东地区的原油运输到日本,需要经过哪个海峡? A、直布罗陀海峡 B、马六甲海峡 C、曼德海峡
- The little chick theearthworm,deciding whether to swa
- 过度包装既浪费资源又污染环境.据测算,如果全国每年减少十分之一的包装纸用量,那么能减少3120000吨二氧化碳的排放量.
- 孟德尔两对相对性状的豌豆杂交实验中,F2中能稳定遗传的个体和性状重组型个体所占比例分别是 A.和 B.和
- 20世纪90年代,中共中央为实现我国社会主义现代化而作出的重大部署是()A.作出了改革开放的伟大决策 B.提出实施“科教
- 22.有关生物膜结构与功能的叙述,正确的是 ( ) A.膜载体蛋白的合成不需要ATP
- 李清照在《醉花阴》中写出自己憔悴的句子: , 。
- 具有完善的体温调节能力能在环境温度变化时仍保持恒定温度的动物叫( ) A.变温动物 B.恒温动物
- Dick was a twenty-year-old man. His father was a teacher and