第二节 富集在海水中的元素--氯 知识点题库
某研究性学习小组同学查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为Ca(ClO)2+CaCl2+2H2SO4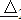 2CaSO4+2Cl2↑+2H2O,他们设计了如图1所示的制取氯气并验证其性质的实验装置:
2CaSO4+2Cl2↑+2H2O,他们设计了如图1所示的制取氯气并验证其性质的实验装置:
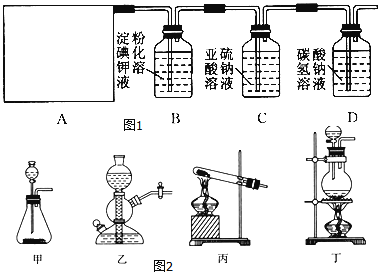
请回答下列问题:
-
(1) 该实验中A部分的装置是图2中的
-
(2) A中发生反应一段时间后,B中的现象是 .
B中发生反应的化学方程式为 .
整套实验装置存在的明显缺陷是
-
(3) 写出D装置中发生反应的离子方程式
-
(4) 请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO3已被氧化为Na2SO4(简述实验步骤):
-
(1) 将Cl2通入NaOH溶液中得到以NaClO为有效成分的漂白液,写出该反应的离子方程式: ;不直接用Cl2作漂白剂的原因是 (写出两条).
-
(2) 使用Cl2为自来水消毒时,会与水中的有机物生成对人体有害的有机氯化物.下列物质中可以替代Cl2为自来水杀菌消毒的是 (填字母序号).
a.臭氧 b.NH3 c.明矾 d.ClO2
-
(3) 生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀.
①NaCl和Cl2中化学键的类型分别是 和 .
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2 . 若生成Cl2 22.4L(标况)时转移电子数为4×6.02×1023 , 该反应的化学方程式是
③已知:
2H2O2(l)═2H2O(l)+O2(g)△H1=﹣196.46kJ•mol﹣1
H2(g)+O2(g)═H2O(l)△H2=﹣285.84kJ•mol﹣1
Cl2(g)+H2(g)═2HCl(g)△H3=﹣184.60kJ•mol﹣1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2 . 依据上述已知反应,写出该反应的热化学方程式:
 ,其中HClO2是漂白剂的有效成分,ClO2是有毒气体.各组分含量随pH变化如图所示,由图可知,使用该漂白剂的最佳pH为( )
,其中HClO2是漂白剂的有效成分,ClO2是有毒气体.各组分含量随pH变化如图所示,由图可知,使用该漂白剂的最佳pH为( ) 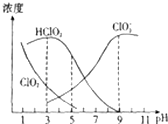
-
(1) 胶体区别于其他分散系的本质特征是.
-
(2) “84”消毒液在日常生活中使用广泛,它的有效成分是(填化学式).
-
(3) 实验室盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞的原因是(用化学方程式说明).
-
(4) 将等物质的量浓度的NaHSO4溶液和Ba(OH)2溶液等体积混合反应,写出该反应的离子方程式是.
-
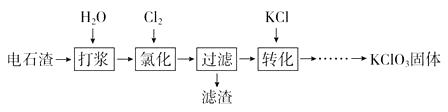
(1) 氯化过程控制电石渣过量、在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①电石与H2O反应的化学方程式为。生成Ca(ClO)2的化学方程式为。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有(填序号)。
A.适当加快通入Cl2速率
B.充分搅拌浆料
C.加水使Ca(OH)2完全溶解
-
(2) 氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:
6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。
75℃时,Ca(ClO)2进一步转化为Ca(ClO3)2的反应方程式为。
滤渣的主要成分为(填化学式)。
-
(3) 向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3的原因是。
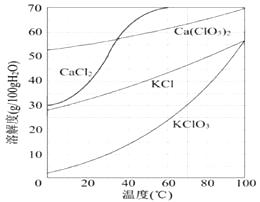
若溶液中KClO3的含量为100 g·L-1 , 从该溶液中尽可能多地析出KClO3固体的方法是。
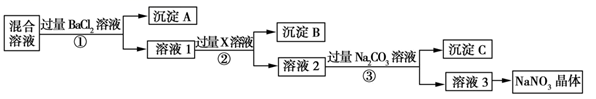
请回答下列问题:
-
(1) 写出实验流程中下列物质的化学式:试剂X,沉淀A。
-
(2) 上述实验流程中①②③步均要进行的实验操作是(填操作名称)。
-
(3) 上述实验流程中加入过量Na2CO3溶液的目的是。
-
(4) 按此实验方案得到的溶液3中肯定含有(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是(填操作名称)。
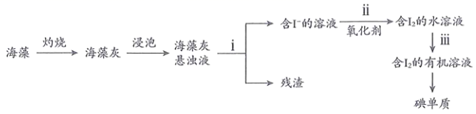
-
(1) 指出上述过程中有关实验操作的名称,步骤i:,步骤iii:。
-
(2) 步骤ii中可使用
 ,从原子结构角度说明理由:。
,从原子结构角度说明理由:。  过量时,可能无法获得
过量时,可能无法获得  ,原因是
,原因是  会被继续氧化为
会被继续氧化为  ,该反应的离子方程式为。
,该反应的离子方程式为。
-
(3) 当使用
 做氧化剂时,
做氧化剂时,  的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。 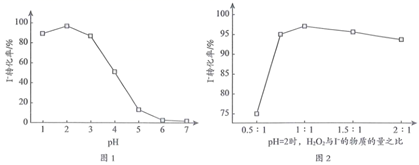
①图1中,
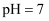 时
时 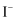 转化率几乎为0,结合离子方程式解释原因:。
转化率几乎为0,结合离子方程式解释原因:。②图2中,
 与
与 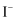 物质的量之比从0.5﹕1提高至1﹕1时,
物质的量之比从0.5﹕1提高至1﹕1时,  的转化率明显增大,可能的原因是(写出2条)。
的转化率明显增大,可能的原因是(写出2条)。
选项 | 实验操作 | 现象 |
A | 将Cl2和H2混合并光照 | 气体安静燃烧,产生苍白色火焰 |
B | 用碘化钾试纸检验Cl2 | 试纸变蓝 |
C | 用酒精萃取碘水中的碘 | 溶液分层,上层是紫红色 |
D | 向FeSO4溶液中滴入NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,最后变为红褐色 |
-
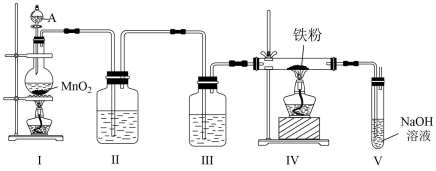
(1) 装置Ⅰ中仪器A的名称是,写出装置Ⅰ中制备氯气的离子方程式。
-
(2) 装置Ⅱ的作用是,装置Ⅲ的溶液是。
-
(3) 写出在装置Ⅳ中发生的反应的化学方程式。
-
(4) 实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到,即可证明滤液中含有
 。
。
-
(5) 另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的装置(填序号)。

 溶液,用湿润的红色石蕊试纸放试管口未变蓝,则原溶液中无
溶液,用湿润的红色石蕊试纸放试管口未变蓝,则原溶液中无 B . 向无色溶液中加入
B . 向无色溶液中加入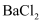 溶液有白色沉淀出现,则溶液中一定含有
溶液有白色沉淀出现,则溶液中一定含有 C . 用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定是钠盐
D . 向某溶液中加入稀盐酸产生使澄清石灰水变浑浊的气体,则溶液中可能含有
C . 用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定是钠盐
D . 向某溶液中加入稀盐酸产生使澄清石灰水变浑浊的气体,则溶液中可能含有
- 用某溶液进行焰色反应实验,透过蓝色钴玻璃可看见紫色火焰,在此溶液中加入AgNO3溶液,生成不溶于稀HNO3的黄色沉淀,此
- 生活中的很多现象与变化有关,下列属于物理变化的是() A.高炉炼铁 B.干冰升华
- 不等式-3x2+6x>2的解集为.
- 某温度时,在2 L容器中X、Y、Z三种物质的变化曲线如下图所示,由图中数据分析,该反应的化学方程式为__________
- 臧霸字宣高,泰山华人也。父戒,为县狱掾,据法不听太守欲所私杀,太守大怒,令收戒诣府,时送者百余人。霸年十八,将客数十人径
- ---_______?---He’s a doctor. A.What is his nameB.What does h
- 2009年12月7日,联合国气候变化大会在哥本哈根开幕。在本次联合国气候变化大会上,三大阵营(欧盟、以美国为首的伞形集团
- 据美国《每日科学》网站2009年7月20日报道,美国两位科学家发现Y染色体比X染色体的演化速度快得多,这将导致Y染色体上
- 《敕勒歌》中“敕勒川,阴山下,天似穹庐,笼盖四野。天苍苍,野茫茫,风吹草低见牛羊”表明:①当时鲜卑人民的游牧生活 当
- 下图为甲、乙、丙、丁四地气温和降水资料统计图。读图完成四地气候类型分布的叙述,正确的是
- 不能用金属和酸直接反应得到的物质是( ) A.FeCl3 B.FeCl2 C.Zn
- 在我国汽车市场上,既有自主品牌的汽车,又有进口汽车和中外合资企业生产的汽车。在以下选项中,可能使我国消费者享受到更低汽车
- 下列哪一项不属于细胞膜的功能? A.控制物质进出细胞B.将胰岛细胞形成的胰岛素,分泌到细胞外 C.提高细胞内化学反应的速
- 下列词语中划线字的读音,全都不相同的一组是( ) A.翌日 翳蔽 风度翩翩 翕然从之
- (5分)下图是实验室制取、收集有关气体的装置图。请按要求回答下列问题: (1)用双氧水制取氧气的化学方程式为
- 小雨在家看电视,发现了一个奇怪的现象:按机上调台键“POB▼”时,频道却在增加(好象按了调台键“POB▲”),而按电视机
- You ________ to leave until you _______ your work. A. won’t
- 计算:= .
- 若动点(x,y)在曲线=1(b>0)上变化,则x2+2y的最大值为( ) A.
- 被日本称为“海上生命线”的海峡是( ) A.白令海峡 B.直布罗陀海峡 C.马六甲海峡



