第二节 富集在海水中的元素--氯 知识点题库
-
(1) 如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 .
-
(2) Na2FeO4溶于水会放出一种无色无味气体,其杀菌消毒、吸附水中的悬浮杂质的原理可用离子方程式表示为
-
(3) 工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2 , 同时产生CO2气体,已知该反应分为两步进行,第一步为2ClO3﹣+2Cl﹣+4H+=2ClO2↑+Cl2↑+2H2O.
①写出第二步反应的离子方程式 .
②工业生产时需在反应物中加少量Cl﹣ , 其作用是 .
③生产中会发生副反应ClO3﹣+Cl﹣+H+﹣Cl2↑+H2O(未配平),若测得反应后的混合气体中Cl2的体积分数为3/73,则起始投料时CH3OH与NaClO3的物质的量之比为
-
(4)
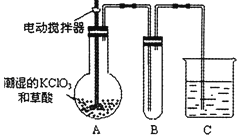
已知二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为﹣59℃,沸点为11.0℃,易溶于水.ClO2也可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸在60℃时反应制得.某学生用如图所示的装置模拟工业制取及收集ClO2 , 其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置.请问:
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置 ;
②C中应装的试剂为 .C中发生反应的化学方程式为:
(1)工业上将氯气通入石灰乳制取漂白粉,反应的化学方程式为: .
(2)漂白粉的有效成分是(填化学式) .
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 .
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号) .
(5)将漂白粉溶于适量水中,呈白色浊状物,静置沉降,取少许上层清液,滴加几滴酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈 性,并可能具有 性.
-
(1) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,漂白粉的有效成分是(填化学式)有关化学反应方程式为.
-
(2) 漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为.
-
(3) O3与Cl2具有相似的性质,均可用于自来水的消毒.已知二者在消毒时均被还原为最低价态,则相同状况下10L O3与L Cl2的消毒能力相当.
①氢氧化亚铁在空气中最终变为灰绿色;
②淀粉溶液遇单质碘变为蓝色;
③向硫酸铁溶液中加入KSCN变为红色
④新制氯水久置后变为无色;
⑤无水硫酸铜吸收水蒸气变成浅绿色;
⑥品红溶液通入过量二氧化硫后褪色.
-
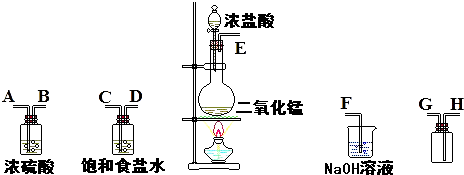
(1) 连接上述仪器的正确顺序(填各接口处的字母):接;接;接;接.
-
(2) 在制备氯气的发生装置中,用到的玻璃仪器除酒精灯外,还有.
-
(3) 写出用如图装置制备氯气的离子方程式:
-
(4) A、B两组同学分别用两种方法制取氯气:A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为AB(填“>”、“<”或“=”)
-
(5) 实验中饱和食盐水的作用是:
-
(6) 写出氯气尾气吸收的化学方程式:.
-
(7) 如何验证氯气已经收集满?
①水玻璃是制备硅胶和木材防火剂的原料;②氢氧化铝可以用做耐火材料;③氢氟酸可以用来刻蚀玻璃;④纯净的二氧化硅是制备光导纤维的原料;⑤利用氯气的毒性可以消灭田鼠;⑥漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂;⑦四氧化三铁常用作红色油漆和涂料⑧晶体硅是良好的半导体材料,可以制成光电池
-
(1) ①写出乙炔的结构式;②写出水玻璃中溶质的化学式。
-
(2) 写出二氧化锰与浓盐酸共热反应的化学方程式:。
 2HCl
B . 制取镁:MgCl2(溶液)
2HCl
B . 制取镁:MgCl2(溶液)  Mg+Cl2
C . 制乙烯:C2H5OH
Mg+Cl2
C . 制乙烯:C2H5OH 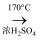 CH2=CH2+H2O
D . 制乙醇:CH2=CH2+H2O
CH2=CH2+H2O
D . 制乙醇:CH2=CH2+H2O 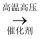 C2H5OH
C2H5OH
-
(1) 25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-分别在三 者中所占分数(α)随pH变化的关系如图1所示:
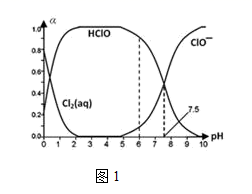
①已知HClO的杀菌能力比ClO-强,由图分析,用氯气处理饮用水时,pH=7.5与 pH=6时杀菌效果强的是。
②氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为。
-
(2) ClO2是一种新的消毒剂,工业上可用Cl2氧化NaClO2溶液制取ClO2 , 写出该反应 的化学方程式。
-
(3) 工业上还可用下列方法制备ClO2 , 在80℃时电解氯化钠溶液得到NaClO3 , 然后与盐酸反应得到ClO2 . 电解时,NaClO3在极(填阴或阳)生成,生成
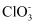 的电极反应式为。
的电极反应式为。
-
(4) 一定条件下,在水溶液中 1mol Cl-、1mol
 (x=1,2,3,4)的能量大小与化合价的关系如图2所示:
(x=1,2,3,4)的能量大小与化合价的关系如图2所示: 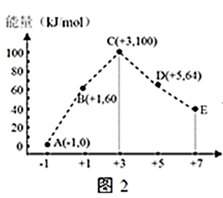
①从能量角度看,C、D、E中最不稳定的离子是(填离子符号)。
②B→A+D反应的热化学方程式为(用离子符号表示)。
-
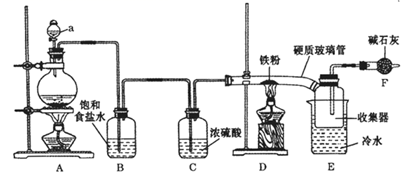
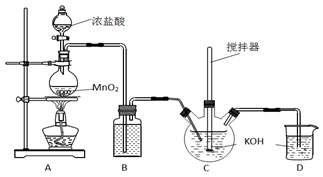
(1) 仪器a的名称是。
-
(2) A中反应的离子方程式是,D中反应的化学方程式是。
-
(3) 反应开始时,先点燃处的酒精灯(填“A”或“D”)。
-
(4) 若无B、C两装置,所得产物中可能含有的杂质是(写化学式)。
-
(5) F中碱石灰的作用是(写2点)。
-
(1) K2FeO4 , 其中铁元素的化合价为。
-
(2) 写出装置A中制备Cl2的化学方程式: 。
-
(3) 装置D中发生的化学反应方程式。
-
(4) 8.7 g MnO2和足量的浓盐酸反应,求生成Cl2的体积为升(标准状况下)
-
(1) 利用下图装置制备“84”消毒液。
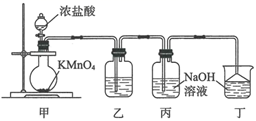
①盛放浓盐酸的仪器名称为,该仪器使用前应先进行的操作为。
②装置甲中制备氯气的离子方程式为。
③装置乙中盛放的药品为,若无此装置造成的后果为。
-
(2) “84”消毒液需要在阴暗处密封保存,否则容易失效,用化学用语解释其原因:
①NaClO+H2O+CO2=NaHCO3+HClO;
②。
-
(3) 某兴趣小组通过实验测定不同pH环境中不同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
NaClO溶液浓度(mg/L)
不同pH下的细菌杀灭率(%)
pH=4.0
pH=6.5
pH=9.0
250
98.90
77.90
53.90
①NaClO溶液呈碱性的原因为(用离子方程式表示)。
②调节NaClO溶液pH时不能选用清厕灵(含HCl)的原因为。
③结合表中数据可推断,相同条件下,HClO的杀菌能力 (填“强于”“弱于”或“相当于”)NaClO的杀菌能力。
-
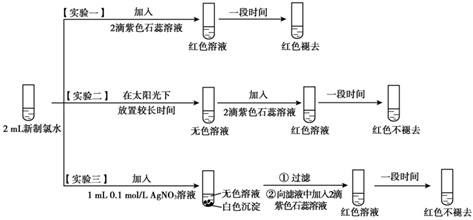
(1) 氯水呈黄绿色,说明其中含有(填化学式)。
-
(2) 实验一的现象表明,氯水具有酸性和性。
-
(3) 氯气与水反应的化学方程式为。
-
(4) 用化学方程式说明实验二中“红色不褪去”的原因。
-
(5) 实验四证明了实验三中“红色不褪去”不是因为氯水被稀释所致,补充所加试剂和现象。、。
-
(6) (实验四)
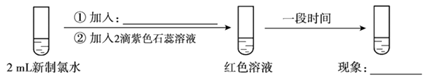
进一步探究实验三中“红色不褪去”的原因。
(实验五)取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
写出氯水和硝酸银溶液反应的化学方程式。
 HClO(aq)
HClO(aq)  Cl2(g)
B . NaCl(aq)
Cl2(g)
B . NaCl(aq) 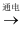 NaOH(aq)
NaOH(aq) 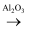 NaAlO2(aq)
C . NaCl(aq)
NaAlO2(aq)
C . NaCl(aq) 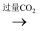 NaHCO3(aq)
NaHCO3(aq) 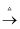 Na2CO3(s)
D . AlCl3(aq)
Na2CO3(s)
D . AlCl3(aq) 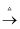 AlCl3(s)
AlCl3(s) 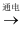 Al(s)
Al(s)
- 他不介意花空余时间为班级做额外的工作。
- Some of you have finished Book One.________, you can go on w
- 音乐会上,演员正在演奏二胡,二胡发声是因为琴弦在,演奏过程中,演员不断调整手指在琴弦上的按压位置是为了改变声音的.
- 关于函数,有下列结论: ①函数的定义域是; ②函数是奇函数; ③函数的最小值为; ④当时,函数是增函数;当时,函数是减函
- 下图分别表示两个自变量对光合速率的影响情况,除各图中所示因素外,其他因素均控制在最适范围。下列分析错误的是:(
- 下列各组比较,不正确的是 A.酸性:HClO4>H2SO4>H3PO4 B.稳定性:HBr>HCl >HF C.原子半径
- (4分)A+,B2+,C-离子都由1~18号中某些元素组成。A+离子中键角为109°28',B2+离子中没有化学键。C-
- 22.阅读下面的材料,根据要求写一篇不少于800字的文章。①衣沾不足惜,但使愿无违。(陶潜) ②致君尧舜上,再使风俗淳。
- 镁是一种活泼的金属,点燃后,既能在氮气中燃烧也能在二氧化碳中继续燃烧。已知镁在氮气中燃烧,生成一种叫氮化镁(氮显-3价)
- 1982年党的十三大上提出了社会主义初级阶段的基本路线,做出了社会主义初级阶段经济发展分三步走的战略部署。
- 下列说法中正确的是 第1组.爆鸣气、纯净的空气、纯碱、玻璃、铝热剂、漂白粉、硫酸 第2组.蔗糖、浓盐酸、铜、医用酒精、食
- 调查发现人群中夫妇双方均表现正常也能生出白化病患儿。研究表明白化病由一对等位基因控制,下列有关白化病遗传的叙述,错误的是
- 鲁迅先生说:“假如我们设立一个‘肚子饿了怎么办’的题目,拖出古人来质问罢,倘说‘肚子饿了应该争食吃’,则即使这人是秦桧,
- 领导了美国历史上第二次资产阶级革命,颁布了《解放黑人奴隶宣言》,维护了国家统一,为美国在19世纪跃居世界头号工业强国开辟
- 甲醇是一种可再生能源,具有广泛的开发和应用前景.下图是用甲醇燃料电池电解饱和食盐水的装置示意图。已知甲池的总反应式为:
- 22.下面是关于“感恩教育”的一段文字。请根据上下文,补写划线处的内容。要求内容贴切,语意连贯,逻辑严密,语句通顺。(5
- 关于氢键,下列说法正确的是 A.某些含氢元素的化合物中一定有氢键 B.氢键比分子间作用力强,所以它属于化学键C
- 用光学显微镜观察植物细胞有丝分裂,下列叙述正确的是() A.一般用洋葱鳞片表皮细胞作为实验材料 B.实验材料
- 椭圆=1上一点到两个焦点的距离的和为()A.26 B.24
- 下图表示某哺乳动物(2n=24)产生生殖细胞的过程,以下说法错误的是 ()。A.在Ⅰ过程中某时期细胞的染色体组最多 B.



