第二节 富集在海水中的元素--氯 知识点题库
下列物质中,不能使干燥、有色布条褪色的是( )
A . “84”消毒液
B . 氯水
C . Cl2
D . 漂粉精溶液
下列物质能使湿润的有色布条褪色的是( )
A . 氯化钙
B . 氯化氢
C . 氯气
D . 氯化钠
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( )
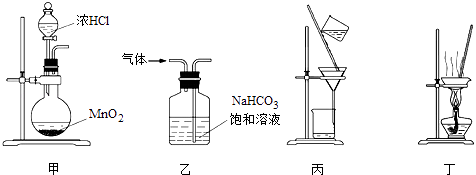
A . 用装置甲制取氯气
B . 用装置乙除去氯气中混有的少量氯化氢
C . 用装置丙分离二氧化锰和氯化锰溶液
D . 用装置丁蒸干氯化锰溶液制MnCl2•4H2O
下列有关物质性质的应用正确的是( )
A . 次氯酸钙有强氧化性,用于饮用水消毒
B . 木炭具有还原性,用于制冰箱除味剂
C . 氧化铝具有两性,用于工业冶炼铝单质
D . 氯化铁溶液呈酸性,用于蚀刻铜电路板
氯气是一种重要的工业原料,在纺织、造纸、化工合成方面都有重要的用途.
-
(1) 工业上电解饱和食盐水制取氯气:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑,理论上每转移1mol电子,生成的氯气在标准状况下的体积为L,工业上将生成的氯气通入石灰乳制取漂白粉,请写出该反应的化学方程式.
2NaOH+H2↑+Cl2↑,理论上每转移1mol电子,生成的氯气在标准状况下的体积为L,工业上将生成的氯气通入石灰乳制取漂白粉,请写出该反应的化学方程式.
-
(2) 实验室用MnO2与浓盐酸共热制氯气,试写出该反应的化学方程式,若用100mL 12mol•L﹣1的浓盐酸与足量的MnO2反应,则生成的氯气在标准状况下的体积6.72L(填“>”、“<”或“=”).
下列有关从海带中提取碘的实验原理和装置能达到实验目的的是( )
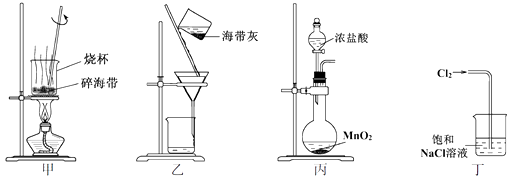
A . 用装置甲灼烧碎海带
B . 用装置乙过滤海带灰的浸泡液
C . 用装置丙制备用于氧化浸泡液中I−的Cl2
D . 用装置丁吸收氧化浸泡液中I−后的Cl2尾气
下列叙述中正确的是( )
A . 工业上以二氧化锰和浓盐酸为原料制取氯气
B . 溴化银可用于人工降雨、氯气可用于制备药物
C . 工业上常用 H2和 Cl2直接化合的方法生产氯化氢以制得盐酸
D . 碘称为“海洋元素”,从海产品中提取碘是工业获取碘的重要途径
在298K、100kPa时,1L水中可溶解0.09molCl2 , 实验测得溶于水的Cl2约有三分之一与水反应。下列说法正确的是( )
A . 氯气与水反应的离子反应方程式为:Cl2 + H2O  2H+ + Cl-+ ClO-
B . 为了增大氯水中HClO的浓度,可以向氯水中加入足量的NaOH固体,使氯气与水反应的平衡向右移动
C . 向该条件下的氯水中加入盐酸,氯气与水反应的平衡移动方向与盐酸的浓度有关
D . 向氯水中通入HCl气体,氯气与水反应的平衡向左移动,氯水的酸性减弱
2H+ + Cl-+ ClO-
B . 为了增大氯水中HClO的浓度,可以向氯水中加入足量的NaOH固体,使氯气与水反应的平衡向右移动
C . 向该条件下的氯水中加入盐酸,氯气与水反应的平衡移动方向与盐酸的浓度有关
D . 向氯水中通入HCl气体,氯气与水反应的平衡向左移动,氯水的酸性减弱
 2H+ + Cl-+ ClO-
B . 为了增大氯水中HClO的浓度,可以向氯水中加入足量的NaOH固体,使氯气与水反应的平衡向右移动
C . 向该条件下的氯水中加入盐酸,氯气与水反应的平衡移动方向与盐酸的浓度有关
D . 向氯水中通入HCl气体,氯气与水反应的平衡向左移动,氯水的酸性减弱
2H+ + Cl-+ ClO-
B . 为了增大氯水中HClO的浓度,可以向氯水中加入足量的NaOH固体,使氯气与水反应的平衡向右移动
C . 向该条件下的氯水中加入盐酸,氯气与水反应的平衡移动方向与盐酸的浓度有关
D . 向氯水中通入HCl气体,氯气与水反应的平衡向左移动,氯水的酸性减弱
从海水中提取溴的工业流程如图:
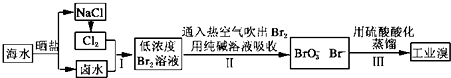
-
(1) 步骤I中将卤水酸化,再通入Cl2 , 是为了防止Cl2与碱反应,写出Cl2与碱反应的离子方程式。
-
(2) 步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是。
-
(3) 实验室保存液溴时,通常在盛液溴的试剂瓶中加少量的水,这与液溴的_____性质有关(填写序号)。A . 氧化性 B . 还原性 C . 挥发性 D . 密度比水大
-
(4) 步骤II中将吹出的溴蒸汽用纯碱溶液吸收时还有CO2生成,写出吸收时发生反应的离子方程式:。
-
(5) 步骤II中通入热空气吹出的Br2用纯碱溶液吸收前先经过NaBr溶液,其目的是。
-
(6) 步骤III中蒸馏出工业溴后残留液的主要溶质是。
-
(7) 步骤III中若使用硝酸酸化,缺点是。
如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是( )
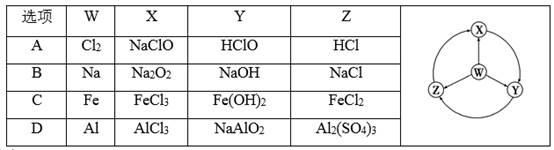
A . A
B . B
C . C
D . D
下列关于氯气的说法正确的是( )
A . 氯气是无色无味气体
B . 铁在氯气中燃烧生成氯化亚铁
C . 氢气在氯气中燃烧,火焰呈淡蓝色
D . 氯气与水反应生成盐酸和次氯酸
有些地方的自来水用氯气消毒,某学生用这种自来水配制下列溶液,不会使药品变质的是( )
A .  溶液
B .
溶液
B . 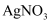 溶液
C .
溶液
C .  溶液
D . 盐酸
溶液
D . 盐酸
 溶液
B .
溶液
B . 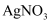 溶液
C .
溶液
C .  溶液
D . 盐酸
溶液
D . 盐酸
-
(1) I. 甲小组的同学用如图装置制备干燥纯净的Cl2 , 并进行性质实验。

装置A中制取氯气,三种玻璃仪器的名称分别是酒精灯、和,反应的化学方程式为。该反应中盐酸体现了(填字母)。
a.氧化性 b.还原性 c. 酸性 d. 碱性
-
(2) 装置B的作用是。
-
(3) 装置C中盛放的是,目的是除去水蒸气。
-
(4) 装置D可以用作不同的用途。
a. 若装置D用于收集Cl2 , 请将图中装置D的导气管补充完整。
b. 若装置D中放入湿润的蓝色石蕊试纸,可以看到的现象是。
-
(5) II. 乙小组的同学用如图所示装置制取氯水并进行相关实验。
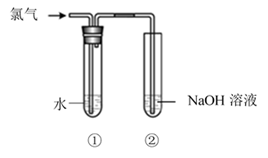
实验进行一段时间后,取少量试管①中的溶液,检验其中有Cl-的方法是。
III. 甲、乙两个小组的同学都用到了NaOH溶液,目的是,反应的离子方程式为。
下列有关实验的操作正确的是( )
| 实验 | 操作 | |
| A | 浓盐酸与MnO2共热制备纯净Cl2 | 将气体产物依次通过浓硫酸、饱和食盐水 |
| B | 除去甲烷中的乙烯 | 将混合气体通过酸性高锰酸钾溶液 |
| C | 配制氯化铁溶液 | 将氯化铁固体溶解在适量的热水中 |
| D | 分离用CCl4萃取碘水中的I2后的混合物 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |
A . A
B . B
C . C
D . D
下列对实验现象的描述正确的是( )
A . 试管中收集到水果香味油状液体 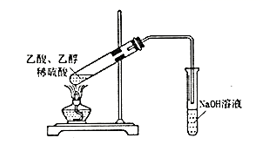 B . 溶液变蓝色
B . 溶液变蓝色 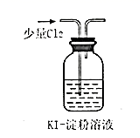 C . 试管中出现黑色沉淀
C . 试管中出现黑色沉淀 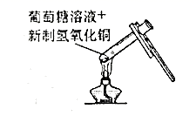 D . 液体最终充满整支试管
D . 液体最终充满整支试管 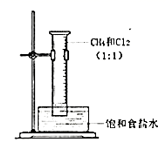
 B . 溶液变蓝色
B . 溶液变蓝色  C . 试管中出现黑色沉淀
C . 试管中出现黑色沉淀  D . 液体最终充满整支试管
D . 液体最终充满整支试管 
向溴水中加入或通入足量下列物质,最终不能得到无色溶液的是( )
A . 二氧化硫
B . 氢氧化钠溶液
C . 碘化钾溶液
D . 热空气
-
(1) ①写出漂白粉有效成分的化学式:;
②写出乙炔的结构式:。
-
(2) 写出实验室用二氧化锰与浓盐酸共热制备氯气的离子方程式:。
-
(3) 写出制备聚丙烯的化学方程式:。
中华传统文化与化学紧密相关,下列有关说法正确的是( )
A . “自古书契多编以竹简,其用缣帛(丝织品)者谓之为纸”,纸的主要成分为蛋白质
B . 李白有诗云“日照香炉生紫烟”,这是描写碘的升华
C . “司南之杓(勺),投之于地,其柢(勺柄)指南”中的“杓”含磁性物质Fe2O3
D . 柴窑烧制出的“明如镜,薄如纸,声如馨”的瓷器,其主要原料为二氧化硅
按要求回答下列问题:
-
(1) 写出
 的电子式;
的电子式;
-
(2) 用电子式表示
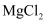 的形成过程;
的形成过程;
-
(3) 写出
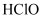 的结构式,它的空间构型为;
的结构式,它的空间构型为;
-
(4) 写出铜和浓硫酸反应的化学方程式;
-
(5) 写出实验室用
 代替
代替  制氯气的离子方程式。
制氯气的离子方程式。
无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡与Cl2反应制备SnCl4 , 装置如图所示。
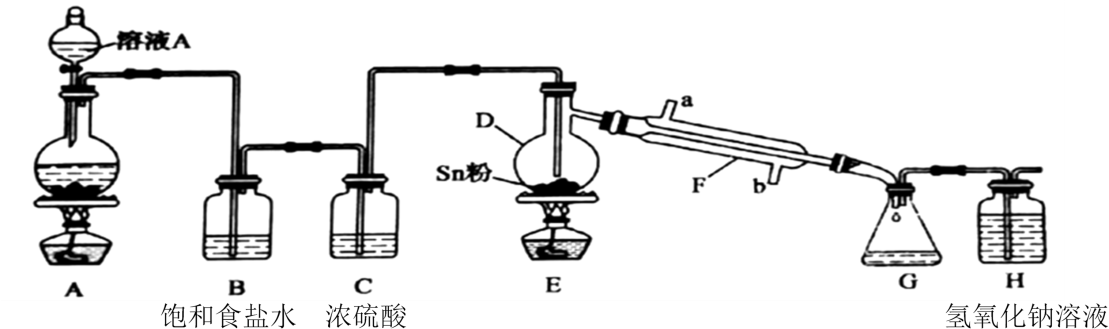
已知:①金属锡熔点为231℃,化学活泼性与铁相似。
②SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解生成SnO2·xH2O,在潮湿的空气中发烟。
③SnCl2中的Sn2+易被氧化为Sn4+。
回答下列问题:
-
(1) 打开分液漏斗上端活塞的作用是,装置A中发生反应的化学方程式为。
-
(2) 实验开始时,正确的操作顺序为(用下列序号排顺序)。
①点燃装置A处酒精灯②点燃装置D处酒精灯③打开分液漏斗活塞
-
(3) 装置B中试剂的作用是,装置F中冷凝水的方向是从端进(填“a”或“b”)。
-
(4) 若没有装置C(其他均相同),则D中发生的主要副反应的化学方程式为:。
-
(5) 该实验装置存在设计缺陷,你的改进措施为。
-
(6) H为尾气处理,请写出反应的离子方程式。
最近更新
- 如图是某几何体的三视图及相关数据,则判断正确的是( )A.a>c B.b>c
- 第二节 完形填空(共20小题;每小题1.5分,满分30分) 阅读下面短文,从短文后各题所给的四个选项A、B、C和
- —______is it? —It's 8:00 in the morning. A.When
- 下图(人民币元/100美元)表明( )①A点到B点表示人民币升值趋势 ②B点到C点表示人民币升值趋势③A点到B点
- “爱国”体现了公民“天下兴亡、匹夫有责”的使命感、责任感,由此,我们会思考自己该以什么样的责任意识和担当精神去践行爱国
- 下列物质不能通过化合反应制得的是:( ) A.FeCl2B.NaHCO3 C.Al(OH)3D.Fe(OH)3
- ------It’s alittle cold today. Would you mind the w
- (4分)液体的表面层里的分子间距离较________。分子间相互作用力表现为________,故液体存在着表面张力。
- 我们有时想说些什么,但似乎又找不着倾诉的对象。这时,你可以尝试跟历史、未来交流,跟爸爸、妈妈交流,跟老师、同学交流;甚至
- 2012年全国两会中,“文化强国”是与会代表们的热门话题。我市某初级中学九年级⑴班同学以“建设文化盐城 你我建言献策”
- 长直木板上表面放一物块,将木板的一端由水平位置缓慢抬起直至竖直,如图1-9-19所示.则铁块受到的摩擦力Ff随角度α的变
- 只用一种试剂就可将AgNO3、KSCN、稀H2SO4、NaOH四种无色溶液区分开,这种试剂是( )A.BaCl2溶
- 题目 依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。
- 俄罗斯大河很多,除伏尔加河外,其它的航运价值不大,最重要的原因是 A.水量小 B.含沙量大
- 古人云:“半部《论语》治天下”。可见《论语》之价值。下列关于此书的叙述正确的是①孔子兴办私学,授徒讲学的主要教材②成为儒
- 选出字形没有错误的一项 (3分) A.接彩 愁怨 哀怨 冷寞 遗篇 沧茫大地 B.忧愁
- 阳光下,微风吹拂的河面,波光粼粼,这里蕴含着光的 现象。
- 下列各种冶炼方法中,可制得相应金属的为 A.高温分解碳酸钙
- ......
- 如图是a、b两种不同物质的熔化曲线,下列说法中正确的是 ()。①a是晶体 ②a是非晶体 ③b是晶体 ④b是非



