第二节 富集在海水中的元素--氯 知识点题库
在硬质玻璃管中的A,B,C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示).向左端导入Cl2 , 在B处加热,可观察到A处棉球呈 色,B处棉球呈 色,C处棉球呈 色.将试管冷却后,在B,C之间的玻璃壁上有 色的 ,这是因为 .
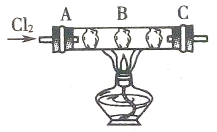
请回答下列问题:
-
(1) 成人如果长期缺碘,会引起的病症是 (填字母).
A.佝偻病 B.甲状腺肿大 C.夜盲症
-
(2) 在瘦肉、胡萝卜、海带中,富含碘元素的是
-
(3) 用盐酸酸化的碘化钾淀粉溶液可检验食盐中是否含有碘酸钾,反应的化学方程式为:5KI+KIO3+6HCl═6KCl+3I2+3H2O则此反应中的氧化剂是 (填化学式),检验加碘盐时可观察到的实验现象是
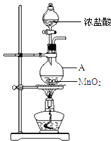
-
(1) 仪器A的名称为;A中反应的离子方程式为;
-
(2) 甲同学将A中产生的气体通入如表溶液:
实验序号
试剂
现象
a
紫色石蕊溶液
b
AgNO3溶液
出现白色沉淀
①实验a中的现象为;
②不能证明产生的气体中含有HCl的实验是(填字母序号);
-
(3) 已知将HCl气体通入饱和食盐水中有白色固体析出.乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因;
-
(4) 已知:2S2O32﹣+I2═S4O62﹣+2I﹣ . 丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl.
I.测定X中溶解的Cl2 . 取25.00mL溶液X,加入过量KI溶液,然后用0.04mol•L﹣1 Na2S2O3溶液滴定生成
的I2 , 达滴定终点时消耗Na2S2O3溶液V mL.
Ⅱ.测定X中Cl元素总量.另取25.00mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl﹣ , 再用0.10mol•L﹣1 AgNO3溶液滴定所得溶液中的Cl﹣ .
①X中的HClO不会影响I的测定结果,原因是;
②由I、Ⅱ中实验数据可证明A中产生的气体中含有HCl,则Ⅱ中消耗0.10mol•L﹣1 AgNO3溶液的体积应大于 mL(用含V的代数式表示).
 CuCl2 所以Cu+I2
CuCl2 所以Cu+I2  CuI2
D . 由钠保存在煤油中,所以钾也可以保存在煤油中
CuI2
D . 由钠保存在煤油中,所以钾也可以保存在煤油中
 5Cl﹣+ClO3﹣+3H2O,请回答下列问题:
5Cl﹣+ClO3﹣+3H2O,请回答下列问题: 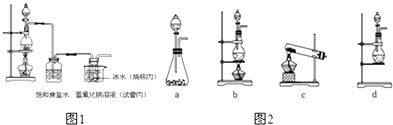
-
(1) 连接好装置,装药品之前,必须进行的一项操作步骤是.
-
(2) 圆底烧瓶内发生反应的化学方程式为;大试管内发生反应的离子方程式为.
-
(3) 饱和食盐水的作用是;冰水的作用是.
-
(4) 在制取Cl2时,实验室中若无MnO2 , 可用KMnO4粉末代替,发生下列反应:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的发生装置是(填序号).
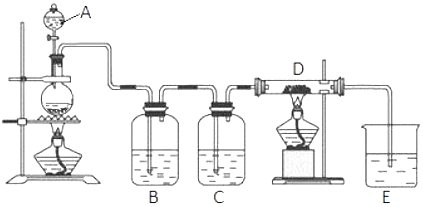
-
(1) 烧瓶中反应的化学方程式是.
-
(2) 装置B中盛放液体是,气体通过装置B的目的是.装置C中盛放的液体是,气体通过装置C的目的是.
-
(3) 烧杯E中盛放的液体是.
-
(4) 资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应.为收集D中产物,在D与E之间,除增加收集装置外,还需要增加装置.
-
(5) 当电子转移的数目为6.02×1023个时生成的氯气的物质的量为mol,生成的氯气用0.5mol/L的NaOH溶液L.
选项 | X | Y | Z | M |
A | FeS2 | SO2 | SO3 | O2 |
B | NaOH | Na2CO3 | NaHCO3 | CO2 |
C | Cl2 | FeCl3 | FeCl2 | Fe |
D | AlO2﹣ | Al(OH)3 | Al3+ | NaOH |
( )
![]()
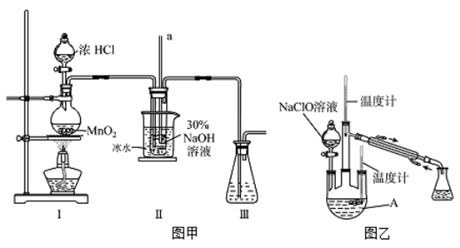
【制备NaClO溶液】实验装置如下图图甲所示(部分夹持装置已省略)
已知:3NaClO  2NaCl+NaClO3
2NaCl+NaClO3
-
(1) 配制30 %NaOH溶液时,所需玻璃仪器除量筒外还有__________(填字母)。A . 容量瓶 B . 烧杯 C . 移液管 D . 玻璃棒
-
(2) 装置I中发生的离子反应方程式是;Ⅱ中玻璃管a的作用为;Ⅱ中用冰水浴控制温度在30℃以下,其主要目的
【制取水合肼】实验装置如上图图乙所示
-
(3) 反应过程中,如果分液漏斗中溶液的滴速过快, 部分N2H4·H2O参与A中反应并产生大量氮气,产品产率因此降低,请写出降低产率的相关化学反应方程式;充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品。
-
(4) 称取馏分0.3000 g,加水配成20.0 mL溶液,一定条件下用0.1500 mol·L-1的I2溶液滴定。已知: N2H4·H2O + 2I2 = N2↑+ 4HI + H2O。
①滴定时,可以选用的指示剂为;
②实验测得消耗I2溶液的平均值为20. 00 mL,馏分中N2H4·H2O的质量分数为。
-
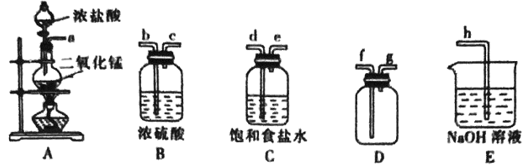
(1) 写出装置中发生反应的程式
-
(2) 连接上述仪器,仪器的正确连接顺序是 a→
-
(3) NaOH溶液的作用是(用化学方程式表示)
-
(4) 将干燥的 Cl2 依次通过干燥的有色布条和湿润的有色布条,可观察到的现象是,得出的结论是
-
(5) 实验结束后,取少量 E 装置中的溶液于烧杯中,加入足量浓盐酸后会产生一种黄绿色气体,试写出生成该气体的离子方程式
 B .
B .  C .
C . 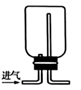 D .
D . 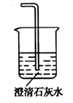
| 操作及现象 | 结论 | |
| A | 向苯中滴入少量浓溴水,振荡,静置分层,上层呈橙红色,下层几乎无色 | 溴水与苯发生取代反应而褪色 |
| B | 向NaI溶液中滴入少量氯水和四氯化碳,振荡静置,下层呈紫色 | I-还原性强于Cl- |
| C | 湿润的淀粉KI试纸伸入某红棕色气体中,试纸变蓝 | 该气体一定为NO2 |
| D | 在无水乙醇中加入金属Na,缓慢生成可以在空气中燃烧的气体 | 乙醇是弱电解质 |
- 储蓄存款并不是越少越好,适度的储蓄( ) ①可以支援现代化建设 ②可以调节货币的流通 ③有利于人们建立文明健康
- 小芳不爱吃蔬菜、水果,刷牙时发现牙龈经常出血,这是由于体内缺少A.维生素D B.维生素C C.维生
- 现有三组混合液:(1)甲酸乙酯和乙酸钠;(2)乙醇和丁醇;(3)溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依此是
- 下列句于中,加点成语使用无误的一项是 A、在“课内比较学”活动中.郭老师的课讲得惟妙惟肖,赢得了全班同学的热烈掌
- 请写出两个既是轴对称图形又是中心对称图形的平面几何图形名称________、_________.
- 关贸总协定发展成为世界贸易组织,是由于() A.多边贸易谈判的决定 B.关贸总协定临时适用性的不足 C.贸易自由化深入发
- 下图是某同学自己设计的装置:用大塑料瓶截去底部,留瓶口一段约10cm,瓶口用一胶塞由里向外塞紧。A、B两极是用镀铬曲别针
- 北京时间2010年8月8 日 20时,梅西率领巴塞罗那队与北京国安队在鸟巢体育场进行友谊赛,下图是与其相符的日照图(阴影
- 人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变成Fe3+,生成高铁血红蛋白而丧失
- 下列现象是描述一定质量的酒精在不同条件蒸发快慢的情况,其中最能说明蒸发快慢跟它的表面积有关的是 A.温度不同的酒精分别装
- 如图,一斜劈放在水平面上,在斜面上的静止释放一物块,物块能以加速度a沿斜面匀加速下滑,若在物块上再放上另一物块,它们在下
- 下列用来表示物质变化的化学用语中,正确的是 A.氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- B.铅蓄电池
- (1)下面A~F是中学化学实验中常见的几种仪器:A.坩埚B.容量瓶C.试管D.托盘天平 E.玻璃棒 ① 其中仪器
- 具有单双键交替长链(如—CH=CH—CH=CH—CH=CH—)的高分子有可能成为导电塑料。下列高分子中可能成为导电塑料的
- all scientists from Asia. A.Were present at the meeti
- 网上购物,因具有“商品多、价格便宜、送货上门”等突出优势,在我国得到迅猛发展。2014年全国网购交易规模达到2.65万亿
- 下列五个命题中: ①函数y=loga(2x﹣1)+2015(a>0且a≠1)的图象过定点(1,2015); ②若定义域为
- --Mike, the telephone is ringing. --I _________ answer it.
- Those farmers who _________ move from place to place with th
- 教师不肯评论考试结果。(comment)



