第二节 富集在海水中的元素--氯 知识点题库
-
(1) 请写出氯气与水反应的化学方程式:.
并据此推断氯水中主要含有的离子是;含有的分子是(均填写化学式).
-
(2) 写出氯气与水反应的产物中发生电离的电离方程式.
;.
-
(3) 写出久置氯水漂白作用会明显减弱的原因的化学方程式:.
-
(4) 向氯水中加入试剂,既能促使氯气与水反应的化学平衡向正反应方向移动又可增加次氯酸的量.
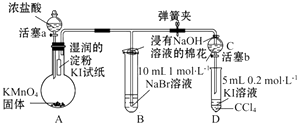
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a.
Ⅳ.…
-
(1) A中产生的是黄绿色气体,其电子式是,在该反应中浓盐酸表现了性和性.
-
(2) 验证氯气的氧化性强于碘的实验现象是.
-
(3) B中溶液发生反应的离子方程式是.
-
(4) 为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是.
-
(5) 过程Ⅲ实验的目的是.
-
(6) 氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,得电子能力逐渐减弱.
选项 | 溶液(或水) | 现象 | 结论 |
A | 蒸馏水 | 溶液呈浅黄绿色 | 氯水中存在Cl2分子 |
B | 品红溶液 | 溶液褪色 | Cl2有漂白性 |
C | AgNO3溶液 | 产生白色沉淀 | 氯水中存在Cl- |
D | Na2S溶液 | 产生淡黄色沉淀 | Cl2有氧化性 |
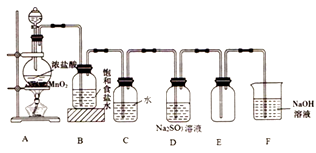
回答下列问题:
-
(1) 装罝A中制取Cl2的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,该反应中体现了HCl的性质。
MnCl2+Cl2↑+2H2O,该反应中体现了HCl的性质。
-
(2) 装罝C中发生反应的离子方程式为,反应后溶液中含有的具有氧化性的含Cl元素的分子有。
-
(3) 实验结束后,测得装罝D溶液中存在大量SO42-。Cl2通过装置D溶液时发生反应的离子方程式为。
-
(4) 装置F的作用是,该装罝中发生反应的离子方程式为。
-
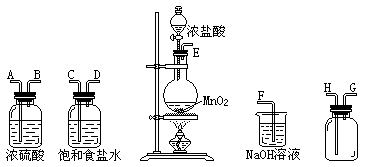
(1) 连接上述仪器的正确顺序是:E接,接,接H,G接F。
-
(2) 气体发生装置中进行的反应化学方程式是 ;当足量的MnO2与2mol浓盐酸充分反应后(不考虑浓盐酸的挥发),得到的氯气的物质的量小于0.5mol的原因是。
-
(3) 在装置中:①饱和食盐水的作用是,②浓硫酸的作用是。
-
(4) 化学实验中检验是否有Cl2产生常用,如果有Cl2产生,可观察到的现象是,写出反应方程式。
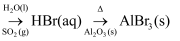 B .
B .  C . Cu(s)
C . Cu(s) 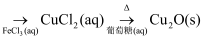 D . SiO2
D . SiO2 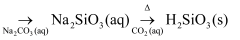
①MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。根据以上两个反应,回答下列有关问题:
-
(1) 反应①的离子方程式为。
-
(2) 浓盐酸在反应①中显示出来的性质是。
A.还原性B.氧化性C.酸性
若有17.4gMnO2参与反应,则被氧化的HCl的质量为g。
-
(3) 用双线桥法表示该反应②中电子转移的方向和数目。
-
(4) 若要制得相同质量的氯气,反应①②中电子转移的数目之比为。
-
(5) 已知反应④:4HCl+O2
 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、KMnO4、O2三种物质氧化性由强到弱的顺序为。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、KMnO4、O2三种物质氧化性由强到弱的顺序为。

已知:①高氯酸:沸点90 ℃,浓度低于60%比较稳定,浓度高于60%遇含碳化合物易爆炸。
② 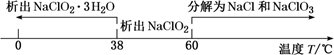
回答下列问题:
-
(1) 仪器a的名称为。实验开始前,胶塞及导管接口必须包锡箔纸,其原因是。
-
(2) 写出装置A制备ClO2同时生成高氯酸的化学方程式:。
-
(3) 关闭止水夹②,打开止水夹①③,通空气一段时间,装置C中生成NaClO2 , 离子方程式为。若关闭止水夹③,打开止水夹②,B中可观察到的现象为。
-
(4) 从装置C反应后的溶液中获得NaClO2晶体,常采用减压蒸发结晶。采用减压蒸发的原因是,减压蒸发时,当有较多晶体析出时,再(填操作方法),洗涤,干燥。即可得NaClO2。
-
(5) 城市饮用水处理新技术用NaClO2、高铁酸钠替代Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,NaClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是。
-
(6) ClO2很不稳定,需随用随制,产物用水吸收可得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样量取V0mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用cmol·L−1Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V1mL。
已知:2ClO2+10I−+8H+=2Cl−+5I2+4H2O,2Na2S2O3+I2=Na2S4O6+2NaI,计算该ClO2的浓度为g/L(用含字母的代数式表示,计算结果化简)。
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2 , 该过程会生成Ca(ClO)2 , Ca(ClO)2会进一步转化为Ca(ClO3)2 , 少量Ca(ClO)2分解为CaCl2和O2 , 过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是( )
 B .
B . 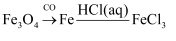 C .
C .  D .
D . 
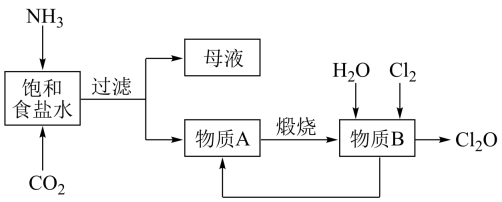
下列说法正确的是( )
 D . 母液经过进一步处理可制得氮肥
D . 母液经过进一步处理可制得氮肥
- 从农业经营方式看A.墨累-达令盆地主要是家庭农场经营B.美国的谷物农业主要由集体农庄经营C.阿根廷的牧牛业主要由国家经营
- When it’s very hot, I ___________swimming in the pool. A.wou
- 洋务运动时期,国内有人反对修筑铁路,“闻泰西诸国专尚机器,如织布、挖河等事,皆明以一器代数百人之工,暗以一器夺数百人之业
- 一块砖平放和竖放在地面时,受力面积之比为4∶1,则平放和竖放时对地面的压强之比为_____,压力之比为_____。
- 2010年6月5日,世界环境日中国主题为“低碳减排,绿色生活”,旨在传递低碳生活理念,提高公众环保意识。该主题倡导减少二
- 11. ____ you may be right , I can’t agree completely. A. Wh
- 如图所示,质量为M的框架放在水平地面上,一轻质弹簧上端固定在框架上,下端固定一个质量为m的小球,小球上下振动时,框架始终
- 某物体从二层楼高处自由下落,则物体下落到地面所用时间大约是 ( ) A.0.01s B.0.8s
- 某点以东是东半球,以西是西半球,以南是南半球,以北是北半球,该点是( ) A.经度0°,纬度0° B
- 如图,塔吊臂上有一可以沿水平方向运动的小车A,小车下装有吊着物体B的吊钩.在小车A与物体B以相同的水平速度沿吊臂方向匀速
- 某C、H、O化合物0.05 mol在0.2 mol O2中燃烧。反应完毕,此有机物已全部变成气态无机化合物(110 ℃)
- 本题对应于“物质结构与性质”选修模块的内容。 下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。 Z M
- 补写下列句中的空缺部分。(8分)(1) 汉乐府民歌《______》是我国最早的也是最长的一首叙事诗,它与南朝的《木兰辞》
- 对于股份制,下列认识正确的有() ①股份制是社会化大生产发展的产物 ②股份制的实质是私有制 ③股份有限公司最基本的特征
- 全国政协在北京举行座谈会,众多政协委员汇聚一堂,就金融业如何服务于战略性新兴产业进行了探讨并提出了建议。以下关于人民政协
- In a typhoon, winds _____ a speed greater than 120 kilometer
- -- __________ ? --The more.the better. A.How often shall I f
- 有一在空气中暴露过的KOH固体,含H2O 2.8%(质量分数,下同),含K2CO3 7.2%。取1 g该样品投入到25
- 航天员专用的小分子团水具有饮用量少、在人体内储留时间长、排放量少等特点。航天员一次饮用125mL小分子团水,可维持人体6
- 10.某外伤病人,不能说话但能听懂别人讲话,能写字,也能看书看报,那么受损的是( ) A.运动性语言中枢S区



