第二节 富集在海水中的元素--氯 知识点题库
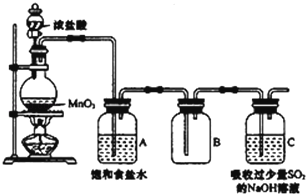
某科研小组用MnO2的浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对尾气进行吸收处理,如图所示:
(1)装置连接好后,应先检查装置气密性,方法是 .
(2)盛浓盐酸的仪器名称是 ;圆底烧瓶中发生反应的离子方程式是 ;饱和食盐水的作用是 .
(3)吸收Cl2时首先发生的反应时Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O.吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl﹣、SO42﹣和OH﹣ . 请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响).
①提出合理假设:
假设1: ;
假设2:只存在ClO﹣;
假设3:既不存在SO32﹣ , 也不存在ClO﹣;
②吸收液中可能存在ClO﹣的原因是 (用离子方程式表示).
③设计实验方案,进行实验.请在表中补充实验步骤以及预期现象和结论.限选实验试剂:3mol/L H2SO4溶液,1mol/L NaOH溶液、0.01mol/L KMnO4溶液、品红溶液、淀粉KI溶液.
实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液于试管中,滴加3mol/L H2SO4溶液至溶液呈酸性,然后将所得溶液分别置于A、B试管中 | / |
步骤2: | Ⅰ: ,则假设1成立; Ⅱ: , |
步骤3: | Ⅰ: ,则假设1成立; Ⅱ: , |
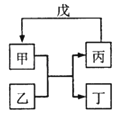
下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)
甲 | 乙 | 丙 | 戊 | |
A | NH3 | Cl2 | N2 | H2 |
B | C | SiO2 | CO | CuO |
C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | CO2 |
D | 乙醇乙酯 | NaOH溶液 | 乙醇 | 乙酸 |
( )
-
(1) 上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH﹣=H2O,该反应的化学方程式为.
-
(2) 实验室制备试剂⑦的方法是:.
-
(3) 可用于治疗胃酸过多的试剂是(填序号)
-
(4) 若某溶液中同时存在Fe3+和Fe2+ , 则可用于验证其中含Fe2+的试剂是(填序号);若某溶液中存在Na+、K+、SO42﹣、Cl﹣四种离子,若检验Cl﹣的存在可选用的试剂是(填序号),具体操作方法是.
-
(5) 用98%的浓H2SO4(ρ=1.84g/cm3)配制500ml0.5mol/L的稀H2SO4 , 所需浓H2SO4的体积为 ml(小数点后保留一位有效数字)
| 选项 | 实验 | 现象 | 结论 |
| A | 将氯气通入品红溶液 | 溶液红色褪去 | 氯气具有漂白性 |
| B | 将铜粉加入1.0mol•L﹣1 的Fe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属Fe比Cu活泼 |
| C | 用坩埚钳夹住用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点比较低 |
| D | 向盛有少量浓硝酸、稀硝酸的两支试管中分别加入一片大小相同的铜片 | 浓硝酸中铜片很快开始溶解,并放出红棕色气体;稀硝酸中过一会铜片表面才出现无色气体,气体遇空气变红棕色 | 浓硝酸氧化性强于稀硝酸 |
| 选项 | 实验 | 检验方法 |
| A | 向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,得Fe(OH)3胶体 | 用激光笔照射烧杯中的液体 |
| B | 证明溶液中存在NH4+ | 滴加浓NaOH溶液,加热,将湿润的红色石蕊试纸置于试管口,试纸变蓝 |
| C | 区分AgNO3溶液和Al2(SO4)3溶液 | 分别取少量溶液,滴加BaCl2溶液 |
| D | 证明氯水中起漂白作用的不是Cl2 | 用CCl4充分萃取,将红纸条分别浸入分层后的溶液中 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向少量未知溶液中加入稀盐酸 | 产生能使澄清石灰水变浑浊的气体 | 未知溶液中含有 |
| B | 在空气中点燃氢气,将导管伸入盛有氯气的集气瓶 | 集气瓶中产生白烟 | 生成 |
| C | 向 | 溶液中出现凝胶 | 非金属性: |
| D | 向 | 电导率减小 | 溶液中的离子浓度减小 |
 B . 向氯水中滴加硝酸酸化的
B . 向氯水中滴加硝酸酸化的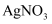 溶液,产生白色沉淀,说明氯水中含有
溶液,产生白色沉淀,说明氯水中含有 C . 向氯水中加入
C . 向氯水中加入 粉末,有气泡产生,说明氯水中含有
粉末,有气泡产生,说明氯水中含有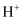 D . 向
D . 向 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
-
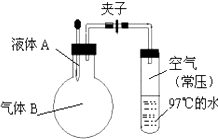
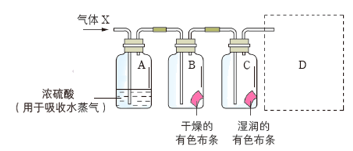
(1) C中的现象是;结合化学方程式说明B、C中现象不同的原因。
-
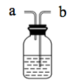
(2) 需要在D处连接如图所示装置,气体应该由(填“a”或“b”)管通入。该装置的作用是,用离子方程式表示其原理。
- 有下列应用或实验现象:①在玻璃生产车间里,利用有真空吸盘的吊车吊运平板玻璃;②将两个表面光滑的铅块相互压紧后,能悬挂若干
- (2015届湖北黄冈中考)阅读下面的文字,完成后面题目。 【甲】庆历四年春,滕子京谪守巴陵郡。越明年,政通人和,百废具兴
- 下图海底地形中,表示大陆架的是( )A、① B、② C、③ D、④
- 不能判定四边形ABCD是平行四边形的条件是( )A.AB=CD,AD=BC B.A
- Na、Al、Fe都是重要的金属元素。下列说法正确的是() A.三者的氧化物都是碱性氧化物 B.三者的氢氧化物都是白色固体
- 选出下列各项中成语运用不恰当的一项: ( ) A研究生导师配备互选,既加深了导师和学员之间的相互了解,避免了“乱点鸳鸯谱
- Low-carbon lifestyle is of great benefit to improve the worl
- 下列各句中,没有语病的一句是 A.我国约近百分之六十左右的青年认为“诚实可信”、“助人为乐”是优秀的传统美德,是做人的基
- 工业革命后,西欧各国普遍认识到科学技术的重要性,大力鼓励科学理论研究,取得了一系列重大突破。19世纪因而被称作“科学的世
- Itwas in 1969 ______ two Americans went to the moon by spac
- -How is Emmy? -I have no idea. She hasn’t written to me ____
- Although the working mother is very busy, she still ___ a lo
- Everyone’s at it, even my neighbors. I thought I might be th
- 下列词语中,没有错别字的一组是() A.装订 节骨眼 见危授命 叨陪鲤对 B.亲睐 照相机 声名雀起 涣然冰释 C.国粹
- 股票和国债的相同点在于() ①都是有价证券 ②都是能带来一定收益的金融资产③受益权相同 ④都是集资的手段 A.①②③
- 在平面直角坐标系中,圆:,圆:.若圆上存在一点,使得过点可作一条射线与圆依次交于点,,满足,则半径r的取值范围是
- 过双曲线左焦点,倾斜角为的直线交双曲线右支于点,若线段的中点在轴上,则此双曲线的离心率为( ▲ ) A.
- 人们总是希望有一个“好皇帝”,依靠他拯救众生。因此,在中国封建社会中,皇帝及皇权的长期统治便凝聚成人们对皇帝敬畏的世俗宗
- 神舟八号飞船已于2011年11月1日发射升空,升空后“神八”与此前发射的“天宫一号”实现了两次交会对接,“神八”与“天宫
- 20、仔细观察下面这幅漫画,用一句话概括其寓意。(6分)
 或
或 

 溶液中滴入稀盐酸
溶液中滴入稀盐酸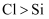
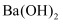 溶液中滴加少量稀硫酸,测电导率变化
溶液中滴加少量稀硫酸,测电导率变化


