第二节 富集在海水中的元素--氯 知识点题库
-
(1) 向FeCl2溶液中加入氯水,氯水中起作用的主要微粒是,反应的离子方程式是。
-
(2) 向AgNO3溶液中加入氯水,氯水中起作用的主要微粒是,反应的离子方程式是。
-
(3) 向氯水中滴加石蕊试液,溶液变红,起作用的微粒是;然后又褪色,起作用的微粒是。
-
(1) 该消毒液可用NaOH溶液吸收 Cl2制备,化学方程式为.
-
(2) 向 FeSO4 溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为:.
-
(3) 该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险.若将二者混合,每产生 1mol Cl2 , 转移电子个数约为
-
(1) C3O3N3Cl2Na由种元素组成.
-
(2) HClO中氧元素的化合价为.
-
(3) 净化水除了上述方法外.请你另举一例:.
-
(4) 除去余氯的反应之一为:Na2SO3+HClO=Na2SO4+X,X的化学式为.
-
(5) 使用净水丸时.能否先破碎后使用? (填”能”或“不能”)
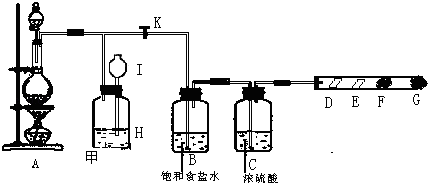
其中D处放有干燥的紫色石蕊试纸,E处放有湿润的紫色石蕊试纸,F、G处依次放有喷上少量淀粉KI溶液、浓NaOH溶液的棉球.回答下列问题:
-
(1) 在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,请写出A处反应的化学方程式:;
-
(2) B处饱和食盐水是为了除去.
-
(3) 在E处,紫色石蕊纸的颜色由紫色变为红色,再变为无色,其原因是.
-
(4) 当F处棉球变色,立即关闭活塞K,可看到I瓶中液面上升,H瓶中充满黄绿色气体.则甲装置的作用为.
-
(5) G处可能发生反应的化学方程式.
-
(1) I. 某同学设计检验食盐是否为加碘盐的定性实验方法:
①取待检食盐溶于水,加入稀硫酸酸化,再加入过量的KI溶液,振荡。
②为验证①中有I2生成,向上述混合液中加入少量CCl4充分振荡后,静置。
若为加碘盐,则①中发生反应的离子方程式为。
-
(2) ②中的实验操作名称是。
-
(3) 实验过程中能证明食盐含KIO3的现象是。
-
(4) Ⅱ. 碘摄入过多或者过少都会增加患甲状腺疾病的风险。目前国家标准(GB/T13025.7)所用的食盐中碘含量测定方法:
①用饱和溴水将碘盐中少量的I-氧化成IO3-。
②再加入甲酸发生反应:Br2+HCOOH=CO2↑+2HBr。
③在酸性条件下,加入过量KI,使之与IO3-完全反应。
④以淀粉作指示剂,用Na2S2O3标准溶液进行滴定,测定碘元素的含量。
I2+2Na2S2O3=2NaI+Na2S4O6
①中反应的离子方程式为。
-
(5) 测定食盐碘含量过程中,Na2S2O3 , 与IO3-的物质的量之比为。
-
(6) 有人提出为简化操作将①、②省略,但这样会造成测定结果偏低。请分析偏低的原因:。
-
(1) 工业上制取漂白粉的化学方程式为。
-
(2) 漂白粉的有效成分是(填化学式)。
-
(3) 漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸。化学反应方程式为 。
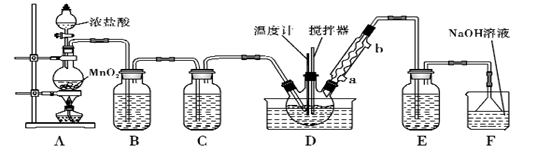
 CCl4+S2Cl2),其装置如下:
CCl4+S2Cl2),其装置如下:
-
(1) A装置中的离子反应方程式为。
-
(2) 一氯化硫(S2Cl2)常温下较为稳定,受热易分解,易被氧化,且遇水即歧化,歧化产物中不仅有淡黄色固体,而且还有两种气体,用NaOH溶液吸收该气体可得两种盐Na2SO3和NaCl。 写出一氯化硫与水反应的化学反应方程式。
-
(3) B装置的作用是。
-
(4) D中冷凝管的冷水进水口为(填“a”或“b”);实验过程中,需要先点燃A处酒精灯,通入氯气一段时间后方可向D中水槽里面加入热水加热,这样做的目的是。
-
(5) F装置是用来处理尾气氯气的,已知该吸收反应的氧化产物不仅有NaClO还有NaClO3 , 且n(NaClO)/n(NaClO3)=3/1,则该反应被还原的氯原子与被氧化的氯原子物质的量之比为。
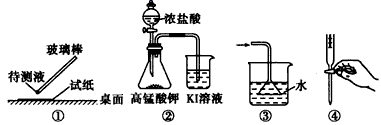
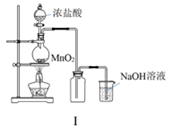 图I:若MnO2过量,则浓盐酸就可全部消耗
B .
图I:若MnO2过量,则浓盐酸就可全部消耗
B . 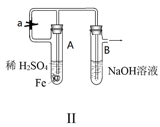 图Ⅱ:可利用该装置制备Fe(OH)2并较长时间保持颜色不变
C .
图Ⅱ:可利用该装置制备Fe(OH)2并较长时间保持颜色不变
C . 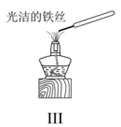 图Ⅲ:可利用该实验直接观察纯碱中钠元素的焰色反应
D .
图Ⅲ:可利用该实验直接观察纯碱中钠元素的焰色反应
D . 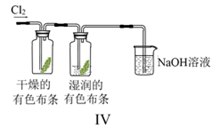 图Ⅳ:利用该实验装置可证明起漂白作用的不是Cl2
图Ⅳ:利用该实验装置可证明起漂白作用的不是Cl2
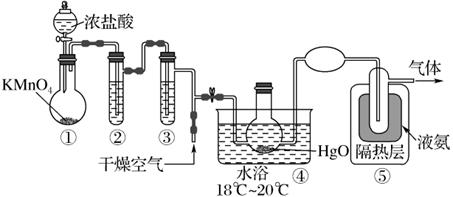
已知:Cl2O 的熔点为-116℃,沸点为3.8℃;NH3的沸点为-33.5 ℃;Cl2 的沸点为-34.6 ℃;HgO+2Cl2=HgCl2+Cl2O。下列说法中错误的是( )
| 实验 | 装置 | 试剂X | 现象 |
| ① | | 滴有酚酞的NaOH溶液 | 溶液红色褪色 |
| ② | NaHCO3溶液 | 产生气泡 | |
| ③ | HNO3酸化的AgNO3溶液 | 产生白色沉淀 | |
| ④ | FeCl2溶液、KSCN溶液 | 溶液变红 |
 +HClO=ClO-+CO2↑+H2O
C . 实验③:ClO-+Ag++H2O=AgCl↓+2OH-
D . 实验④:Cl2+2Fe2+=2Fe3++2Cl-
+HClO=ClO-+CO2↑+H2O
C . 实验③:ClO-+Ag++H2O=AgCl↓+2OH-
D . 实验④:Cl2+2Fe2+=2Fe3++2Cl-
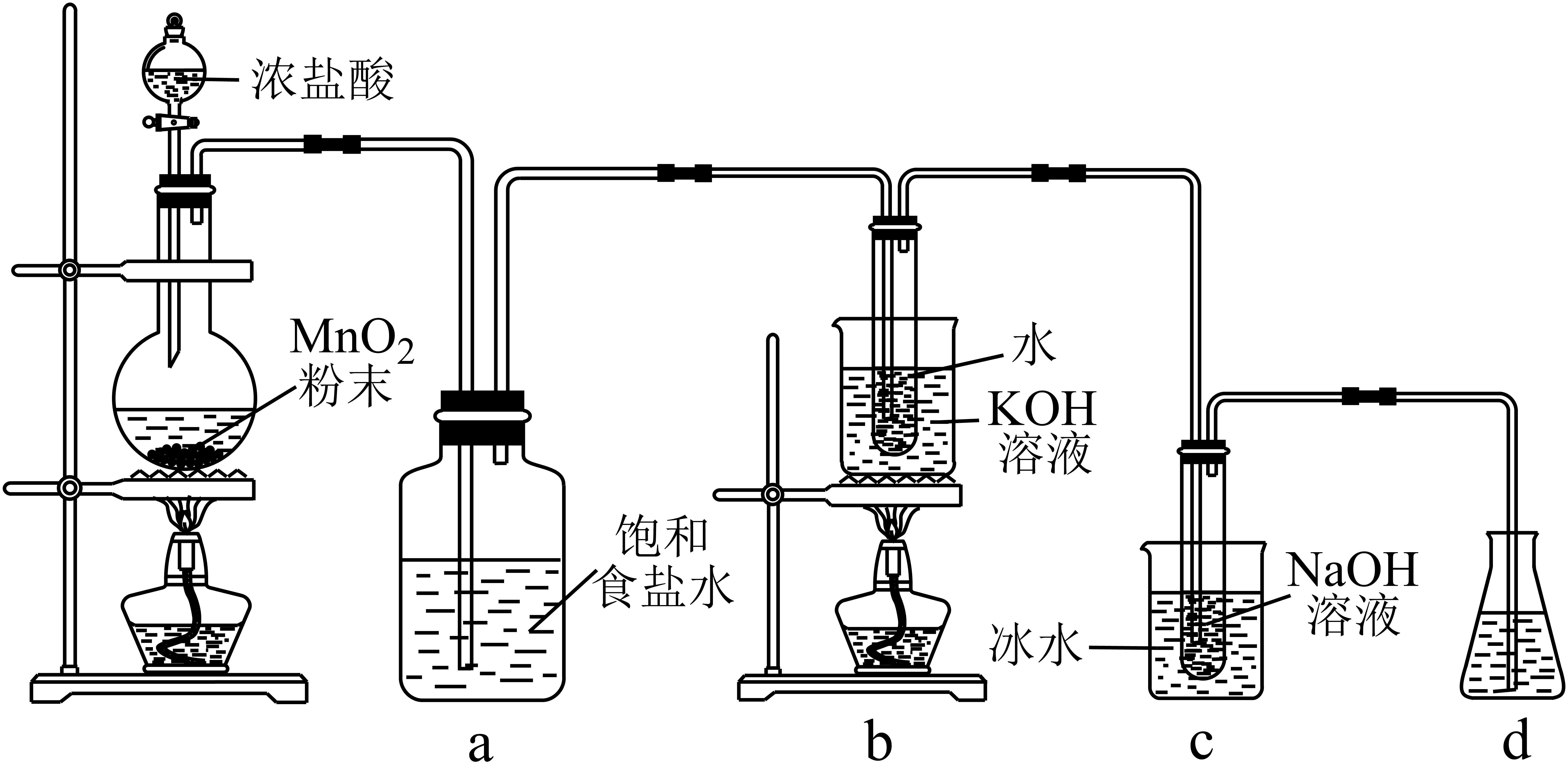
回答下列问题:
-
(1) 盛放浓盐酸的仪器名称是。
-
(2) a的作用是。
-
(3) b中采用的加热方式是,c中发生反应的离子方程式是。
-
(4) d中可选用试剂____(填标号)。A . Na2SO3溶液 B . NaCl溶液 C . NaOH溶液 D . 稀H2SO4
-
(5) 反应结束后,取出b中试管,经冷却、结晶、、及干燥,得到KClO3晶体。
-
(6) 取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变,2号试管溶液变为棕色,可知该条件下NaClO的氧化能力KClO3(填“大于”或“小于”)。
-
(7) 已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常用水稀释100倍(体积之比)后使用。用水稀释后的溶液中c(Na+)=mol/L。(保留到小数点后两位)
84消毒液
有效成分:NaClO
规格:100mL
质量分数:25%
密度:1.19g/cm3
选项 | 实验 | 现象 | 结论 |
A | 向 | 产生白色沉淀,且有无色气体生成 | 溶液中 |
B | 检验某无色溶液中是否含有 | 溶液变黄色且试管上部产生红棕色气体 | 该溶液中含有 |
C | 将铜粉放入稀硫酸溶液中并不断通入 | 铜粉快速溶解,溶液变为蓝色 | 形成 |
D | 向某钾盐中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为 |
- 已知小麦抗病对感病为显性,无芒对有芒为显性,两对性状独立遗传。用纯合的抗病无芒与感病有芒杂交,F1自交,播种所有的F2,
- 根据下列实验操作,预测的实验现象和实验结论或解释正确的是 实验操作 预测的实验现象 实验结论或解释 A 向饱和Na2CO
- —I will buy you a new bike if you learnhow to swim this summ
- 2009年7月30日,商务部、国家发改委等九部委在京联合召开电视电话会议,决定从今年8月至2010年2月,在全国范围内开
- 下图表示的是身边一些物质在常温下的近似pH,有关这些物质的比较和判断正确的是()A.柠檬的酸性比橘子弱 B.橘子汁显
- (1)属于芳香族化合物的是________(填序号,下同)。 (2)属于芳香烃的是__________。 (3)属于苯的
- 阅读下列短文,从各题所给的A、B、C和D项中选出最佳选项,Robots aren’t only in the movie
- 函数的值域是
- 不等式组的解集在数轴上表示为( )
- (08四川攀枝花)已知:R1<R2,图中的四种不同接法,其总电阻最小的是( )
- 如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,A池中混合液的体积为
- 2014 年 2 月 23 日召开的济南市民族宗教工作会议指出,要以创新宣传教育机制为重点,以加强宗教团体建设为突破口,
- 把方程去分母,正确的是( )A.B.C.D.
- Michael Jordan hasfailed over and over again in his life.And
- 设P是△ABC内任意一点,S△ABC表示△ABC的面积,λ1=, λ2=,λ3=,定义f(P)=(λ1, λ, λ3),
- 下列说法不正确的是() A.氢氧化钡晶体与氯化铵固体的反应是吸热反应 B.氢氧化钾与硝酸的反应是放热反应 C.共价化合物
- . 某机关现有工作人员120名,现在的人数比三年前减少了40%,求原有人数x,根据题意,相等关系为_______,列方程
- 下列说法正确的是
- 1919年五四运动取得了初步胜利,其表现不包括( ) A、北洋军阀政府被迫释放被捕学生 B
- 右图为细胞间信息传递的几种模式示意图,下列分析错误的是( ) A.若细胞1产生的激素

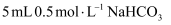 溶液中滴入
溶液中滴入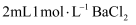 溶液
溶液 部分电离出
部分电离出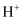 和
和 ,
,  与
与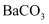 沉淀,促进了
沉淀,促进了 的电离,使
的电离,使
 , 取少量该溶液于试管中,加稀盐酸酸化,再加入
, 取少量该溶液于试管中,加稀盐酸酸化,再加入 溶液
溶液 , 再在溶液中滴加少量
, 再在溶液中滴加少量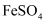 溶液
溶液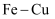 原电池,加快反应速率
原电池,加快反应速率 或
或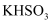 或者二者混合物
或者二者混合物


