高考化学试题
(1)基态镍原子的价电子排布式___________________________
(2)镍和苯基硼酸共催化剂实现了丙烯醇(CH2=CH—CH2OH)的绿色高效合成.丙烯醇中碳原子的杂化类型有______________________;丙醛(CH3CH2CHO)与丙烯醇(CH2=CH—CH2OH)分子量相等,但丙醛比丙烯醇的沸点低的多,其主要原因是________________________。
(3)羰基镍[Ni(CO)4]用于制备高纯度镍粉.羰基镍[Ni(CO)4]中Ni、C、O 的电负性由大到小的顺序为______。
(4)Ni2+ 能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]- 等。NH3 的空间构型为:_______;与SCN- 互为等电子体的分子有:__________________(填分子式)
(5)“NiO”晶胞如图:

①氧化镍晶胞中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为_____________
②已知氧化镍晶胞密度dg/cm3,NA 代表阿伏加德罗常数的值,则Ni2+ 半径为________nm(用代数式表示)
①水玻璃、碱石灰、漂白粉、福尔马林、淀粉均为混合物
②进行中和热的测定实验时,必须用到两个量筒和两个温度计
③由不同种原子间形成的共价键一定是极性共价键
④有单质参加的反应或有单质产生的反应一定是氧化还原反应
⑤碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
⑥蒸馏在天然香料,药物提取及核燃料处理等技术中得到了广泛的应用
⑦Ca(HCO3)2、Fe(OH)3可由化合反应制得,Fe3O4可以由置换反应制得
A. ①③⑤ B. ①⑤⑦ C. ②③⑤⑦ D. ①②④⑥
四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿 ( 主要含 




回答下列问题:
( 1 ) “ 焙烧 ” 产生的气体用 _______ 吸收后可制取氮肥。
( 2 ) “ 浸出 ” 时, 




( 3 ) “ 净化 ” 时,浸出液中残留的 、








( 4 ) “ 净化 ” 后,溶液中若有低价钼 ( 以 


( 5 ) “ 沉淀 ” 时,加入 
( 6 ) 高温下用 


A. 用装置甲进行中和热的测定
B. 用装置乙制取CO2气体
C. 用装置丙蒸发CH3COONa溶液得CH3COONa晶体
D. 用装置丁模拟工业制氨气并检验产物


回答下列问题:
(1)A的名称是______________。
(2)B→C的反应试剂是_______ ,反应类型是_______;E→F的反应类型是_______。
(3)C→D反应的化学方程式为________________。
(4)E中含氧官能团的名称为______。
(5)1molG与足量NaOH溶液反应,可以消耗_____molNaOH。
(6)H是G的同系物,满足下列条件的H的同分异构体有_______种(不考虑立体异构)。
① H相对分子质量比G大14 ② 苯环上含两个取代基
其中核磁共振氢谱为六组峰,峰面积之比为1:2:2:2:2:1的结构简式为_____________。
(7)结合以上合成路线及相关信息,设计由苯制备苯酚的合成路线________________。
A.
 配制0.1mol·L-1NaCl溶液
配制0.1mol·L-1NaCl溶液B.
 检验石蜡油分解产生了不饱和烃
检验石蜡油分解产生了不饱和烃C.
 用渗析法分离葡萄糖与氯化钠的混合液
用渗析法分离葡萄糖与氯化钠的混合液D.
 用陶瓷蒸发皿加热NaOH溶液获得纯净的NaOH固体
用陶瓷蒸发皿加热NaOH溶液获得纯净的NaOH固体
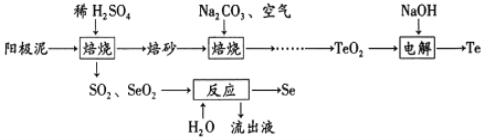
下列叙述错误的是( )
A. 合理处理阳极泥有利于保护环境和资源再利用
B. 流出液是H2SO4溶液
C. 电解过程中阴极上析出单质Te
D. “焙砂”与碳酸钠充分混合后,可在瓷坩锅中焙烧
I.I-的定性检测
(1)取少量碘盐样品于试管中,加水溶解。滴加硫酸酸化,再滴加数滴5%NaNO2和淀粉的混合溶液。若溶液变________色,则存在I-,同时有无色气体产生并遇空气变红棕色。试写出该反应的离子方程式为 ___________________________________。
Ⅱ.硫代硫酸钠的制备
工业制备硫代硫酸钠的反应原理为2Na2S + Na2CO3 +4SO2 =3Na2S2O3 +CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠如下图。

先关闭K1打开K2,打开分液漏斗,缓缓滴浓硫酸,控制好反应速率。
(2)y仪器名称___________ 。此时B装置的作用是___________________________。
(3)反应开始后,C中先有淡黄色浑浊,后又变为澄清,此浑浊物为____________。(填化学式)装置D的作用是____________________________________。
(4)实验结束后,关闭K2打开K1。玻璃液封管x中所盛液体最好为________(填序号)
A.NaOH溶液 B.浓硫酸 C.饱和NaHSO3溶液
Ⅲ.碘含量的测定
巳知:①称取10.00g样品,置于250mL锥形瓶中,加水100mL溶解,加2mL磷酸,摇匀。
②滴加饱和溴水至溶液呈现浅黄色,边滴加边摇,至黄色不褪去为止(约1mL)。
③加热煮沸,除去过量的溴,再继续煮沸5min,立即冷却,加入足量15%碘化钾溶液,摇匀。
④加入少量淀粉溶液作指示剂,再用0.002mol/L的Na2S2O3标准溶液滴定至终点。
⑤重复两次,平均消耗Na2S2O3溶液9.00mL
相关反应为:I-+3Br2+3H2O = IO3-+6H++6Br-
IO3-+5I-+6H+ = 3I2+3H2O
I2+2S2O32-= 2I-+S4O62-
(5)请根据上述数据计算该碘盐含碘量为_______ mg·kg—1。

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12

已知:铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
氢氧化物 | Fe(OH)2 | Fe(OH)3 | Cd(OH)2 | Mn(OH)2 |
开始沉淀的pH | 6.5 | 1.5 | 7.2 | 8.2 |
沉淀完全的pH | 9.9 | 3.3 | 9.5 | 10.6 |
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③_____等。已知浸出的金属离子均为二价,写出浸出钴的化学方程式_____________
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3、Co2+的溶液形成微电池并产生合金CoSb。该微电池的正极反应式为______________
(3)除铁的过程分两步进行:
①先加入适量KMnO4,发生反应的离子方程式为_____________
②再加入ZnO控制反应液的pH范围为_____________
(4)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):Ksp(CdCO3)=5.2×10-12, Ksp(CdS)=3.6×10-29,Ksp(Cd(OH)2)=2.0×10-16,根据上述信息:沉淀Cd2+效果最佳的试剂是____________。
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳pH为11,此时溶液中c(Cd2+)=________________
选项 | 实验操作和现象 | 结论 |
A | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | Na2O2没有变质 |
B | 取少许CH3CH2Br与NaOH溶液共热,冷却后滴加AgNO3溶液,最终无淡黄色沉淀 | CH3CH2Br没有水解 |
C | 室温下,用pH试纸测得:0.1 mol·L-1 Na2SO3溶液的pH约为10,0.1 mol·L-1 NaHSO3溶液的pH约为5 | HSO |
D | 向少量碘水中加入过量浓FeCl2溶液,分成两等份,向一份中滴加KSCN溶液显红色;向另一份中滴加淀粉溶液显蓝色 | Fe3+与I-的反应为可逆反应 |
A. A B. B C. C D. D

(1)碘在元素周期表的位置:______________________,其中一种人工放射性核素131I常用于甲亢的治疗,该核素含有的中子数为___________。
(2)结合元素周期律分析Cl-、I-的还原性强弱:同主族元素的原子,从上到下,____________。
(3)水体中的I-的非酸性条件下不易被空气中的
(4)大气中的部分碘源于
已知:每
序号 | 试剂 | 反应前溶液 | 反应后溶液 |
|
|
A |
|
|
| 约 | —— |
B |
|
|
| —— | 少量 |
C |
|
|
| 约 | 大量 |
① a=__________。
② 用离子方程式解释A中pH增大的原因_______________________________________。
③ 写出B中产生![]() 的离子方程式_________________________________________。
的离子方程式_________________________________________。
④ C中实验进行20s后,发现溶液中![]() 浓度开始下降。导致下降的直接原因有_______。
浓度开始下降。导致下降的直接原因有_______。
A ![]() 减小 B
减小 B ![]() 减小 C
减小 C ![]() 不断生成
不断生成
编号 | 操作和现象 | 结论 |
A | 向某待测液中滴加少量新制氯水,再加入几滴KSCN溶液,若溶液变为血红色 | 待测液中存在Fe2+ |
B | 向Na2CO3溶液中加入足量稀盐酸,将产生的气体通入Na2SiO3溶液中,若产生白色沉淀 | 非金属性:Cl>C>Si |
C | 向浓度均为0.1 mol/LNaCl和KI混合溶液中逐滴加入0.1mol/ LAgNO3溶液,若先产生黄色沉淀 | KSP(AgCl)>KSP(AgI) |
D | 向1ml20%的蔗糖溶液中,加几滴稀硫酸。水浴加热5mm后,再加入少量新制备的Cu(OH)2悬浊液,煮沸,若无砖红色沉淀产生 | 蔗糖未水解 |
A. A B. B C. C D. D

(1)向含碘废液中加入稍过量的
(2)操作
(3)氧化时,在三颈瓶中将含

(4)已知:
①取适量含碘废水用
②__________________;
③另从水层中取少量溶液,加入
(5)二氧化氯(
①完成
②若处理含
下列根据实验操作、现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将废铁屑溶于过量盐酸,滴入KSCN溶液 | 溶液未变红 | 废铁屑中不含三价铁的化合物 |
| B | 室温下,测定CH3COONa溶液和NaNO2溶液的pH | 前者pH大 | HNO2电离出H+的能力比CH3COOH的强 |
| C | 向苯酚浊夜中滴入Na2S溶液 | 浊液变清 | 结合H+能力:C6H5O-<S2- |
| D | 向BaSO4固体中加入饱和Na2CO3溶液,过滤,沉淀洗净后加入足量稀盐酸 | 沉淀 部分溶解,且产生气泡 | Ksp(BaSO4)>Ksp(BaCO3) |
A.A B.B C.C D.D
(1)通过以下反应制备金属铝。
反应1:Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g);ΔH1=akJ·mol-1
反应2:Al2O3(s)+3C(s)===2Al(l)+3CO(g);ΔH2=bkJ·mol-1
反应3:3AlCl(g)===2Al(l)+AlCl3(g);ΔH3
①反应3的ΔH3=_______kJ·mol-1。
②950℃时,铝土矿与足量的焦炭和Cl2反应可制得AlCl3。该反应的化学方程式是_______。
(2)在高温条件下进行反应:2Al(l)+AlCl3(g)
①向图1所示的等容积A、B密闭容器中加入足量的Al粉,再分别充入1 mol AlCl3(g),在相同的高温下进行反应。图2表示A容器内的AlCl3(g)体积分数随时间的变化图,在图2中画出B容器内AlCl3(g)体积分数随时间的变化曲线。__________

②1100℃时,向2 L密闭容器中通入3 mol AlCl(g),发生反应:3AlCl(g)=2Al(l)+AlCl3(g)。已知该温度下AlCl(g)的平衡转化率为80%,则该反应的平衡常数K=________。
③加入3molAlCl(g),在不同压强下发生反应,温度对产率的影响如图3所示。此反应选择温度为900℃的原因是_______________。

(3)用铝制作的快速放电铝离子二次电池的原理如图4所示。
①该电池充电时,阴极的电极反应式为_____。
②AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl4-和Al2Cl7-两种离子在电极上相互转化,其他离子不参与电极反应。NaCl的作用是_____。
四硼酸钠的阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示。下列说法不正确的是( )

A. 阴离子中三种元素的第一电离能:O>B>H
B. 在Xm-中,硼原子轨道的杂化类型有sp2和sp3
C. 配位键存在于4、5原子之间和4、6原子之间
D. m=2,NamX的化学式为Na2B4O5(OH)4
北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是
A. 胆矾的化学式为CuSO4
B. 胆矾可作为湿法冶铜的原料
C. “熬之则成胆矾”是浓缩结晶过程
D. “熬胆矾铁釜,久之亦化为铜”是发生了置换反应
A. 配制一定物质的量浓度溶液时,容量瓶中有少量的水会导致溶液浓度偏低
B. 用盐酸标准溶液滴定未知浓度氨水,选用酚酞做指示剂的结果比甲基橙更准确
C. 测定硫酸铜晶体中结晶水含量时,加热后的坩埚应直接放置在石棉网上冷却
D. 测定中和热时,应迅速将酸、碱稀溶液在有保温措施的容器内混合、搅拌,记录最高温度

(1)下列说法正确的是__________。
A.反应后,将试管Ⅰ中的白色固体加入水中,溶液呈蓝色
B.取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO4
C.试管Ⅳ中KMnO4溶液褪色,说明SO2具有氧化性
D.试管V中的NaOH溶液可用Na2CO3溶液代替
(2)取下试管Ⅱ,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因______________。
- 已知,,试判断,所在象限.
- (2011年11月苏州市期中4题)《民本的极限——黄宗羲政治思想新论》的作者张帅伟认为,黄宗羲是传统社会一心一意专事“补
- 华罗庚在古稀之年时说:“树老易空,人老易松,科学之道,诫之以空,诫之以松。我愿一辈子从实以终。”根据课文所提供的材料,谈
- 为保证加酶洗衣粉洗涤效果,应注意( )A.使用沸水先冲泡洗衣粉 B.用含氯较高的自来
- 石墨是一种具有片层结构的晶体,层与层之间的相互作用是范德华力,每一层为碳原子通过共价键形成的六元环并置形成的平面,图3-
- 16.下列各句中,没有语病的一项是( ) A.法国尼斯的恐袭事件备受关注,事件发生几小时后,各个网络媒体关于这一
- 辛亥革命之所以失败主要是因为 A.帝国主义支持反革命势力 B.帝国主义的武装干涉
- 法国人克雷夫克在18世纪70年代写到:“我可以给你指出一个家庭……他的妻子是荷兰人,儿和法国人结婚,生了四个孩子。都娶
- 下列词语中加点的字,每对的读音完全相同的一组是 () A.勾当/勾搭 吐露/露马脚 勒索/
- 电动机的内电阻r=2Ω,与R=8Ω的电阻串连接在线圈上,如图所示.已知线圈面积为m2,共100匝,线圈的电阻为2Ω,线圈
- 完成下列各小题中的化学反应方程式。⑴碱金属与O2反应生成氧化物较复杂,有普通氧化物(如Na2O)过氧化物(如Na2O2)
- 补写出下列名篇名句中的上句或下句 (1)_________ ,景行行止。(《诗经》) (2)_________ ,从恶如
- 下列有关德国影响欧洲局势的表述,符合历史实际的是 A.一战中德国的盟国包括奥匈帝国、罗马尼亚和保加利亚 B.德国在希特勒
- 仿写句子。 彩虹,经过与雷电激战之后才出现; 理想,经过与困难搏斗之后才诞生; 成功,_________________
- 如图所示的电路中,R1=10 Ω,R2=20 Ω。闭合开关S后,电压表V1与V2示数之比为()A.3∶1
- 设集合,则 ( ) A.{1,3} B.{2,4} C.{1,2,3,5} D.{2,5}
- —Do you know the tall man ______ to Mr King overthere? —Sor
- “战士双脚走天下,四渡赤水出奇兵。乌江天险重飞渡,兵临贵阳逼昆明……”歌曲《四渡赤水出奇兵》描绘了红军长征的壮美画卷。
- 第二节:书面表达(满分25分)你的朋友李华是高中毕业生。他对填报志愿时是首先考虑专业还是学校拿不定主意。他想了解你们学校
- 随着经济的发展,文化越来越渗透进人们的日常生活中。如吃饭讲求“饮食文化”,穿衣讲求“服饰文化”,住房讲求“建筑文化”,上



