高一化学试题
某溶液中含有等物质的量的 K+、Na+、Fe3+、Fe2+、SO42-、SO32-、I-、NO3-中的几种离子,为了确定其组成,某同学取两份该溶液进行了如下实验(不考虑盐类的水解及水的电离):
(1)一份滴入酸性高锰酸钾溶液,发现高锰酸钾溶液褪色;
(2)另一份加入氯化钡固体,产生不溶于水的沉淀。
下列说法不正确的是
A. 溶液中可能含有K+ B. 溶液中可能含有SO42-
C. 溶液中可能含有Fe3+ D. 溶液中可能含有SO32-
将15 g CH4和C2H4的混合气体通入盛有足量溴水的容器中,溴水的质量增加了7 g,则混合气体中CH4和C2H4的体积之比为( )
A.1∶2 B.2∶1 C.3∶2 D.2∶3
以下是元素周期表的一部分,回答下列有关问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 4 |
|
|
(1)与水反应最剧烈的金属元素是_____;元素构成的最稳定气态氢化物的化学式是_________;③、④、⑧元素原子半径由大到小是_____________(用元素符号表示).
(2)写出元素⑦的单质与⑥最高价氧化物的水化物反应的离子方程式______________.
(3)②、④两种元素形成某气体化合物是导致温室效应的主要原因,该化合物的电子式为_____________;元素⑥可形成一种碱性氧化物,用电子式表示该碱性氧化物的形成过程______________________.
(4)②的单质与⑨的最高价氧化物的水化物的浓溶液反应化学方程式____________________.
在反应H2S+H2SO4===S↓+SO2↑+2H2O中,若有32 g硫生成则转移电子为( )
A.6 mol B.2 mol C.3 mol D.4 mol
下列化学用语使用正确的是:
A.HCN分子的结构式:H—C≡N B.水分子的球棍模型:![]()
C.中子数为10的氧原子:![]() D..二氧化碳的电子式:
D..二氧化碳的电子式:![]()
将某溶液逐滴加入Fe(OH)3溶胶内,开始产生沉淀,继续滴加时沉淀又溶解,该溶液是
A. FeCl3溶液 B. 2mol·L−1 NaOH的溶液
C. 2mol·L−1 MgSO4的溶液 D. 2mol·L−1 H2SO4的溶液
镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤, 滤液中存在的离子有 ( )
A.AlO2— B.Cu2+ C.Al3+ D.Mg2+
下列离子方程式书写正确的是( )
A.铝粉投入到NaOH溶液中:2Al+2OH-= 2AlO2-+H2
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- = Al(OH)3↓
C.三氯化铁溶液中加入铁粉:![]()
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
20℃时,NaCl的溶解度是35.1g,此时NaCl饱和溶液的密度为1.12g/cm3,在此温度下NaCl饱和溶液中NaCl的物质的量浓度为 ( )
A.0.15mol/L B.1.35mol/L C.4.97mol/L D.6.0mol/L
 (1)如右图所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气。过一段时间后可观察到的现象__________________,发生反应的化学方程式为 。
(1)如右图所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气。过一段时间后可观察到的现象__________________,发生反应的化学方程式为 。
(2)某班同学用如图所示装置测定空气中氧气的含量。先用弹簧夹夹住橡胶管。点燃钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广口瓶内水面的变化情况。

上述实验过程中发生反应的化学方程为 。
苏轼的《格物粗淡》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A.甲烷 B.脱落酸 C.乙烯 D.生长素
区别下列各组中的两种物质的方法错误的是
A. 甲烷和乙烯:分别通入酸性KMnO4溶液
B. 苯和四氯化碳:分别与溴水混合、振荡、静置
C. 乙醇和乙酸:分别滴加NaOH溶液
D. 棉花织品和羊毛织品:分别燃烧闻气味
下列变化属于氮的固定的是
A. 工业上用氨气和硝酸合成硝酸铵
B. 氯化铵受热分解生成氨气和氯化氢
C. 氨气与氯气反应生成氮气
D. 氮气和氧气在放电条件下生成NO
铝是重要的金属材料,铝土矿(主要成分A12O3另含少量的SiO2、Fe2O3等)是工业上制铝的原料。实验室模拟工业上以铝土矿为原料制取铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如下图所示:
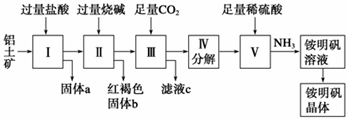
请回答下列问题:
(1)固体a的主要成分为__________________(写化学式)。
(2)II中烧碱过量的原因是________________________________________。
(3)写出III中主要反应的离子方程式__________________________________________。
(4)制取铵明矾溶液的化学方程式为_________________________________________;由铵明矾溶液制取铵明矾晶体的实验操作依次为(填操作名称)______________________、____________、过滤、洗涤。
(5)设计实验证明铵明矾溶液中含有NH4+_______________________________________。
下列的化合物中所有原子周围都满足8电子稳定结构的是 ( )
A.N2 B.PCl5
C.CS2 D.BF3
下列化合物中,不能通过化合反应制取的是:
A.FeCl3 B.H2SiO3 C.CuCl2 D.FeCl2
根据热化学反应方程式:N2(g) + O2(g)→2NO(g)-180.58kJ,若在标准状况下反应生成11.2LNO,则此过程中共( )
A.放出45.145kJ的热量 B.放出180.58kJ的热量
C.吸收45.145kJ的热量 D.吸收90.29kJ的热量
14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法不正确的是( )
①1 mol 14CH4分子中所含中子数为8NA
②7 g 14C原子形成的石墨中所含质子数为3NA
③17 g 甲基(-14CH3)所含电子数为8NA
④常温常压下22![]() .4 L 14CO2的分子数为NA
.4 L 14CO2的分子数为NA
A.①② B.①③ C.①②③ D.③④
相同温度下,关于氨水和氢氧化钠溶液的比较,下列说法正确的是
A.pH相等的两溶液中:c(Na+)>c(![]() )
)
B.物质的量浓度相同的两溶液,分别与HCl气体反应至中性时(忽略溶液体积变化)c(Na+)<c(![]() )
)
C.物质的量浓度相同的两溶液,进行导电性实验,灯泡的亮度相同
D.分别中和pH和体积均相等的两溶液,所需HCl的物质的量不同
硅元素在周期表中的位置是
A. 第二周期ⅣA族 B. 第三周期ⅣA族 C. 第三周期ⅥA族 D. 第二周期ⅥA族
- 图5中的巴尔喀什湖,以湖水东部咸西部淡著称于世。读图回答9~10题。 9.不属于巴尔喀什湖对该地区起的作用是(
- 把足量的铁粉投入到硫酸和硫酸铜的混合溶液中,充分反应后,剩余金属粉末的质量与原加入铁粉的质量相等,则原溶液中H+与的物质
- 某溶液除水电离出的H+、OH-之外仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种,这4种
- 如图所示,间距为d的光滑平行金属导轨,水平放置在竖直向下的、磁感应强度为B的匀强磁场中,一端接有阻值为R的电阻,一质量为
- 函数的定义域为( ) A. B. (0,1] C. D. (,1]
- 化石燃料是不可再生的,因此在农村可将秸杆、杂草等废弃物在密闭环境中发酵得到_____________;汽车可使用含乙醇1
- 2010年8月26日,中国石窟艺术(云冈)金银纪念币发行庆祝仪式在云冈石窟大景区隆重举行。该套金银纪念币共5枚,分别为1
- 如图7所示中,通过定滑轮匀速提起重物G时,向三个方向拉动的力分别为F1、F2、F3,则三个力大小关系是 【】 A
- 下列生产、生活中的变化,属于物理变化的是() A. 冬季雾凇
- 1901年《辛丑条约》签订以后,清政府完全成为帝国主义统治中国的工具,你认为最主要的原因是清政府 A.赔偿白银4.5亿两
- 进入秋冬季,我们很少能看见蛇、青蛙等动物,它们都进入了昏睡状态,这种现象叫冬 眠,这体现了生物对环境的 。
- (11·漳州)(满分10分)如图,AB是⊙O的直径,,∠COD=60°.(1)△AOC是等边三角形吗?请说明理由;(2)
- 一个静止的放射性原子核处于垂直纸面向里的匀强磁场中,由于发生了衰变而形成了如图所示的两个圆形径迹,两圆半径之比为1:16
- 以下各项中,属于明朝大儒王阳明提出的思想主张的是( ) A.“已所不欲,勿施于人” B.“天者,理也” C.“饮食
- 如图,已知长方体 ABCD-A1B1C1D1中,AB=AA1=2,BC=3,M为AC1与CA1的交点,则M点的坐标为__
- (09年雅礼中学月考理)底面边长为,侧棱长为2的正三棱锥ABCD内接于球O,则球O的表面积为 .
- 用如图所示实验装置进行物质性质的探究实验。下列说法不合理的是 ( )A.若品红溶液①
- 简答题 ⑴《欧也妮·葛朗台》是巴尔扎克最得意的长篇小说之一。作品中葛朗台这一形象被刻画得极为生动,成为世界文学史上四大吝
- 按要求写出下列反应的表达式,并注明基本反应类型. (1)氯酸钾和二氧化锰混合物制取氧气;; (2)加热氧化汞粉末;; (
- 下列关于浮力的有关说法中,正确的是( )A.只要液体的密度越大,物体所受的浮力就一定越大 B.只要物体的体积越大,物体



