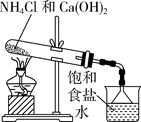
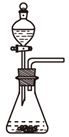
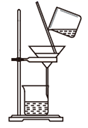
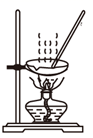
气体发生装置 知识点题库
下图装置可用于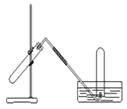
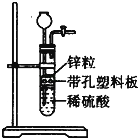
某一兴趣小组准备在实验室中制H2 , 装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaNO3溶液②酒精③四氯化碳 ④苯⑤Na2CO3溶液⑥KCl溶液.( )
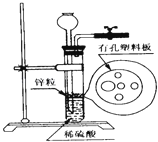
如图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
①食盐水;②KNO3溶液;③适量稀硫酸铜溶液;④Na2CO3溶液;⑤CCl4;⑥浓氨水.
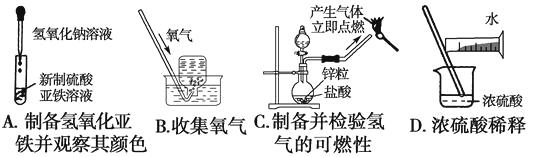
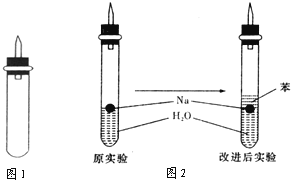
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液.为点燃上述三个反应生成的H2 , 他们设计了如图所示的装置图:
请回答下列问题:
(1)在点燃H2之前必须先进行 .
(2)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了.
他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少.于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是
(3)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97g/mL、0.88g/mL、1.00g/mL,并据此对实验进行了改进.
在改进后的实验中H2的生成速率 .(填减慢或加快)
(4)2.3g钠投入20mL水中完全反应所得溶液的物质的量浓度是 .(不计溶液体积的变化)
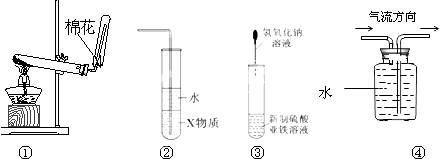
装置① 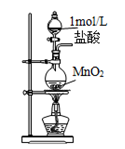 装置②
装置② 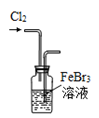 装置③
装置③ 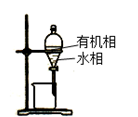
装置④ 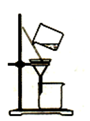 装置⑤
装置⑤ 
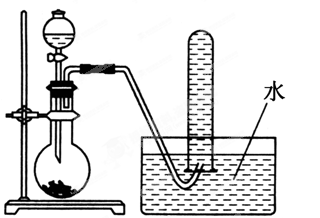
 CH2═CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。
CH2═CH2↑+H2O,某化学学习小组通过该原理制取乙烯并对其性质进行验证。
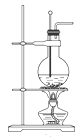
-
(1) 在制取时,常常需要在烧瓶中加入碎瓷片,目的是。
-
(2) 要检验生成的物质,应该首先检验,常选用的药品为。
-
(3) 制取时,关键要控制好温度。
①温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。为了除去除水蒸气外的杂质气体,常用装有下列试剂的洗气瓶进行洗气,则应选用的试剂是。
A.酸性KMnO4溶液
B.浓硫酸
C.NaOH溶液
D.溴水
②制取时温度过低,在140℃时主要发生分子间取代反应生成乙醚(CH3CH2OCH2CH3),试写出其反应方程式。
-
(4) 将净化后的气体先通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,并有新的无色无味气体产生,该气体可参与大气循环,发生反应的离子方程式为。然后将气体通入溴水,溴水褪色,并有油状物质生成。
-
(5) 乙烯的某种同系物的相对分子质量为乙烯的3倍,其同分异构体总数为。将其与氢气加成,得到的烷烃再与氯气发生取代反应,其一氯取代产物为三种的烷烃的结构简式为。
-
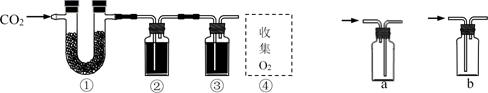
(1) 甲组的同学拟制备原料气NO和Cl2 , 制备装置如下图所示:
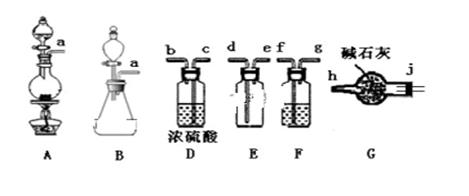
①制备NO发生装置可以选用(填写字母代号),请写出发生反应的离子方程式:。
②欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→ (按气流方向,用小写字母表示)。
-
(2) 乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①实验室也可用X装置制备NO,X装置的优点为。
②检验装置气密性并装入药品,打开K2 , 然后再打开 ,通入一段时间气体,其目的为,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中NOCl可能发生反应的化学方程式为。
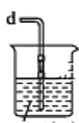
④若尾气处理装置连接上图烧杯中导管d,则烧杯中可加入 溶液。
-
(3) 取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(NOCl)的质量分数为(用代数式表示)。
[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10 , Ksp(Ag2CrO4)=1×10-12]
 B .
B . 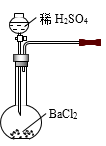 C .
C . 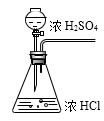 D .
D . 
下列说法错误的是( )
 制取氯气并探究氯气性质,设计了如图所示的实验装置:
制取氯气并探究氯气性质,设计了如图所示的实验装置: 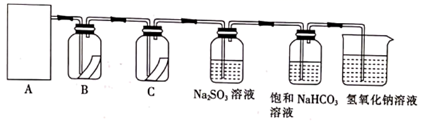
-
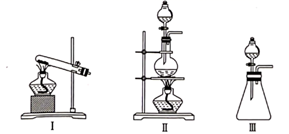
(1) 从装置I、Ⅱ、Ⅲ中选择合适的制氯气的装置( A处):( 填标号)。
-
(2) 装置B、C中依次放的是干燥的红色布条和湿润的红色布条实验过程中该同学发现装置B中的布条也褪色,其原因可能是;说明该装置存在明显的缺陷,请提出合理的改进方法。
-
(3) 验证氯气的氧化性:将氯气通入
 溶液中,氯气可将
溶液中,氯气可将  氧化成
氧化成  。写出该反应的化学方程式:。
。写出该反应的化学方程式:。
-
(4) 氯气通入饱和
 溶液中能产生无色气体已知酸性:盐酸>碳酸>次氯酸。( 强酸可以制弱酸)该实验证明氯气与水反应的生成物中含有( 填“盐酸”或“次氯酸”)。
溶液中能产生无色气体已知酸性:盐酸>碳酸>次氯酸。( 强酸可以制弱酸)该实验证明氯气与水反应的生成物中含有( 填“盐酸”或“次氯酸”)。
-
(5) 实验装置中烧杯内氢氧化钠溶液的作用是。
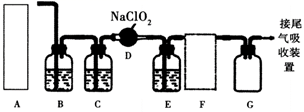
-
(1) A为氯气的发生装置,若用高锰酸钾代替MnO2 , 和浓盐酸可在常温下反应制取Cl2 , 从①、②、③中选择合适的装置(如图,填序号),仪器P的名称是。
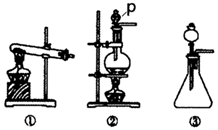
-
(2) 写出装置A中瓶内发生反应的离子方程式:。
-
(3) C装置所盛试剂的作用是,G的作用是。
-
(4) F为ClO2收集装置应选用的装置是(如图,填序号),其中与E装置导管相连的导管口是(填接口字母)。
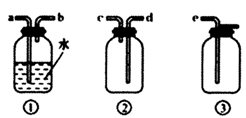
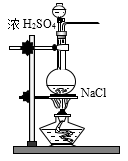
 B . 实验室制备NO
B . 实验室制备NO 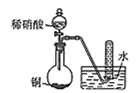 C . 制备氢氧化亚铁
C . 制备氢氧化亚铁 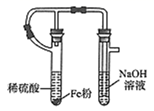 D . 收集SO2 , 并吸收多余的SO2
D . 收集SO2 , 并吸收多余的SO2 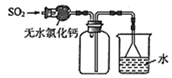
| 选项 | A. | B. | C. | D. |
| 实验操作 | | | | |
| 实验目的 | 制取氨气将其溶于饱和食盐水 | 用碳酸钠与稀硫酸制二氧化碳 | 过滤获得碳酸钠晶体 | 蒸发浓缩氯化铵溶液 |
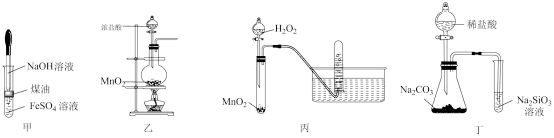
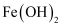 B . 用乙制备少量
B . 用乙制备少量 C . 用丙制备并收集
C . 用丙制备并收集 D . 用丁比较Cl、C、Si的非金属性强弱
D . 用丁比较Cl、C、Si的非金属性强弱
 B . 用装置乙制备
B . 用装置乙制备 气体
C . 用装置丙干燥
气体
C . 用装置丙干燥 D . 用装置丁分离甲醇和水
D . 用装置丁分离甲醇和水
气体 | 方法 | |
A | Cl2 | 将浓盐酸滴入高锰酸钾固体中,用排饱和食盐水法收集 |
B | NH3 | 将浓氨水滴入NaOH固体中,用向下排空气法收集 |
C | NO2 | 将铜片加入浓硝酸中,用排水法收集 |
D | SO2 | 铜与浓硫酸混合加热,用排饱和亚硫酸氢钠溶液法收集 |

- 定义:,若已知函数(且)满足. (1)解不等式:; (2)若对于任意正实数恒成立,求实数的取值范围.
- 补写出下列名句名篇中的空缺部分。(8分)(1)今南方已定,兵甲已足,当奖率三军,北定中原, ,攘除奸凶
- 从Na、C、S、H、O、N六种元素写出符合下列要求的物质(或主要成分)的化学式。(1)常用于食品防腐的一种单质气体
- 造纸技术的改革是在宫廷官员领导下进行的,其成果经皇帝下令推广……司天蓝(古代观测、研究天文等方面的机构)由高级官吏太史令
- 当前,网吧接纳未成年人,黑网吧和非法网络游戏等现象普遍存在,这些现象的存在反映了 A.发展文化不能追求经济利益
- 下列各句中,标点符号使用正确的一句是: A、中国跳水队领队在出征雅典世界杯赛前表示,“这次奥运会前的热身赛预定完成三项任
- 据中国人民银行统计,2009年1~12月份,我国居民户存款余额的同比增幅在29%以上。经济学家把中国居民在银行的存款形象
- (09江苏卷18)原生态文化资源的开发和利用,在丰富人们文化消费的同时,也促进了当地旅游经济的发展。由此可见 A.文化对
- 下列词语中没有错别字的一项是: ( )(2分)A.狼藉彷徨肃然起敬张慌失措B.酝酿懊悔不容置疑目不暇接C
- 下列各组词语中加点字的读音,与所给注音全都相同的一组是 A. 差(chā) 差错 误差 差强人意
- 下列关于Cl﹣和Cl两种粒子的说法不正确的是() A.
- 细菌的特殊结构是( ) A 细胞核 B细胞质 C杆状、球状、螺旋状 D荚膜、鞭毛、芽孢
- 一次函数y=mx-n的图象如图所示,则下面结论正确的是( ) A.m<0,n<0 B.m&
- 由NaHS、MgSO4、NaHSO3组成的混合物中,已知硫元素的质量分数ω(S)=a%,则氧元素的质量分数ω(O)为()
- 生活中的下列物品,用合成材料制作的是 A.铝合金门窗 B.不锈钢餐具 C.塑料洗衣盆 D.景德镇瓷器
- 下列各组有机物不互为同分异构体的是( ) A.氨基乙酸与硝基乙烷
- (07年辽宁卷)(12分)如图,在直三棱柱中,,,分别为棱的中点,为棱上的点,二面角为.(I)证明:;(II)求的长,并
- 悟成长之美:读《音乐学院的坐位》完成后面的答题。(12分)音乐学院的座位(节选)意大利摩德纳市音乐学院有一件有意思的现象
- 国务院总理温家宝通过各种形式问政于民、问计于民表时 间内容2009年2月13日与13位邀请来的基层群众代表围坐在椭圆形桌
- 设 满足约束条件 ,则的最大值为 。