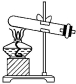
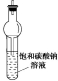
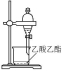
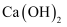气体发生装置 知识点题库
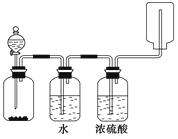
下列有关实验装置进行的相应实验,能达到实验目的是( )
-
(1) 写出利用上述仪器和药品,用化学方程式表示制取该气体的化学反应原理,在制取该气体的整个实验过程中需要用到的仪器有(填仪器序号);
-
(2) 如果下图用氯酸钾制氧气,请同学们将图补充完整;
-
(3) 上图中用此方法收集气体时.证明该气体已经收集满的现象是;
-
(4) 实验结束后要先后。
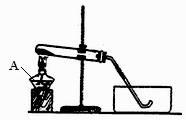
-
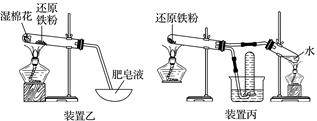
(1) 若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验中观察到C溶液中出现白色沉淀。则A中液体的是(填名称),C中发生反应的离子方程式为。
-
(2) 若要制O2 , B为黑色固体,A中的试剂是(填化学式),C中盛有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为血红色,同时生成红褐色沉淀。写出C中发生氧化还原反应的离子方程式。
-
(3) 已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4 , C中盛有KI淀粉溶液,C中的现象是,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为。
下列说法错误的是( )
 B . 净化Cl2
B . 净化Cl2 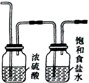 C . 收集Cl2
C . 收集Cl2 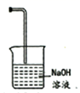
| 气体 | 试剂 | 制备装置 | 收集方法 | |
| A | | | b | e |
| B | | Cu和稀硫酸 | b | c |
| C | NO | Cu和稀硝酸 | b | c |
| D | | | a | d |
 +2H2O=2MnO
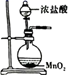
+2H2O=2MnO +MnO2↓+4OH-。下列用Cl2氧化K2MnO4制备KMnO4的实验原理和装置不能达到实验目的的是( )
+MnO2↓+4OH-。下列用Cl2氧化K2MnO4制备KMnO4的实验原理和装置不能达到实验目的的是( )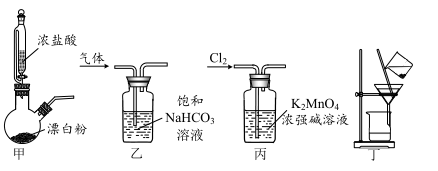
-
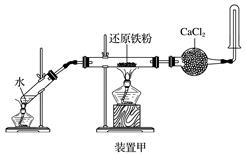
(1) Ⅰ.制备Na2S2O3•5H2O反应原理:Na2SO3(aq)+S(s)
 Na2S2O3(aq)
Na2S2O3(aq)实验步骤:
①称取15gNa2SO3加入圆底烧瓶中,再加入80mL蒸馏水。另取5g研细的硫粉,用3mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60min。回答下列问题:
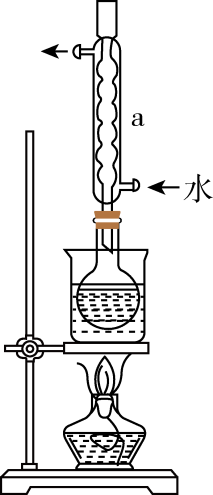
硫粉在反应前用乙醇润湿的目的是。
-
(2) 仪器a的作用是。
-
(3) 产品中除了有未反应的Na2SO3外,是可能存在的无机杂质是,检验是否存在该杂质的方法是。
-
(4) Ⅱ.分离Na2S2O3•5H2O。已知:Na2S2O3•5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。
分离Na2S2O3•5H2O晶体的流程如图所示:





回答下列问题:
为减少产品的损失,操作①要(填操作),其目的是;操作②的包括的过程是快速过滤、洗涤、干燥,其中洗涤操作是用(填试剂)作洗涤剂。
-
(5) 蒸发浓缩滤液直至溶液为止,蒸发时要控制温度不宜过高原因。
-
(6) Ⅲ.研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为10mL):
实验编号
实验温度/℃
c(Na2S2O3)/mol·L-1
c(H2SO4)/mol·L-1
⑴
25
0.1
0.1
⑵
25
0.1
0.2
⑶
50
0.2
0.1
⑷
50
0.1
0.1
探究浓度对化学反应速率的影响,应选择(填实验编号)。
-
(7) 探究温度对化学反应速率的影响,应选择(填实验编号)。
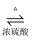 CH3COOC2H5 +H2O。下列操作或装置能达到实验目的的是( )
CH3COOC2H5 +H2O。下列操作或装置能达到实验目的的是( )A | B | C | D |
|
|
|
|
混合反应物 | 生成乙酸乙酯 | 收集乙酸乙酯 | 分离乙酸乙酯 |
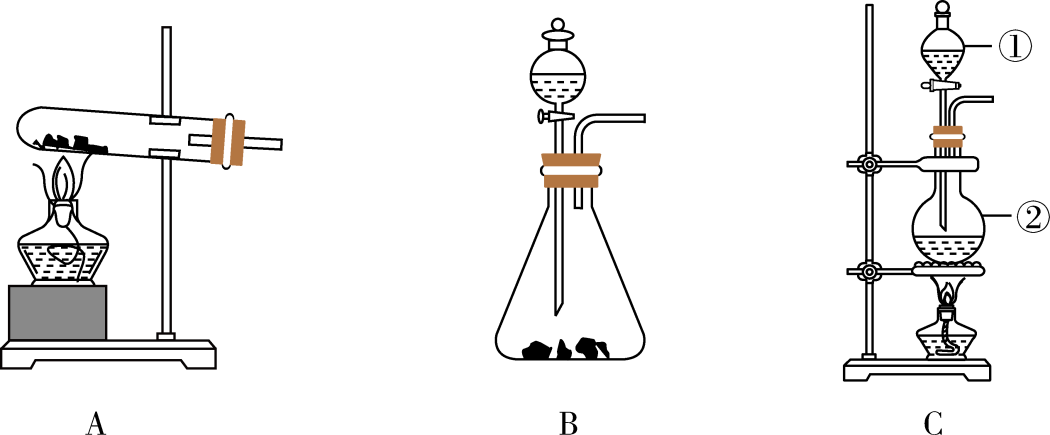
-
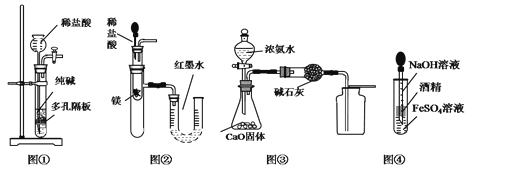
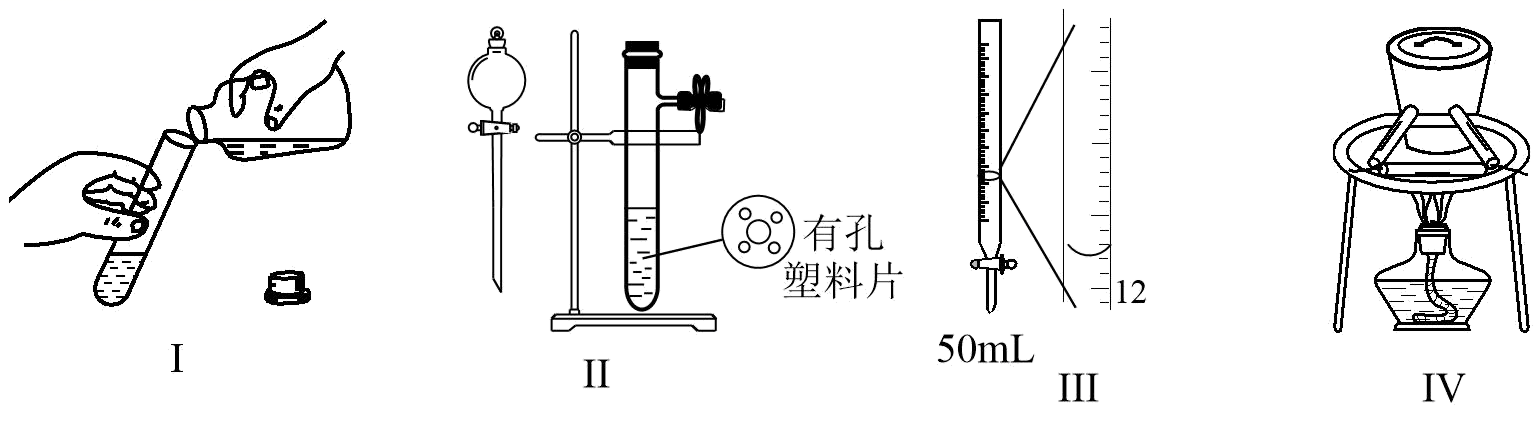
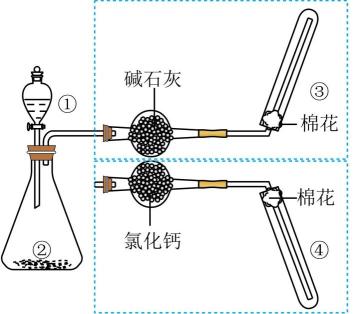
(1) 仪器②的名称是。
-
(2) 根据题目所提供药品,可利用装置B制备的气体是。
-
(3) 用C装置制备的气体离子方程式。
-
(4) 实验室也可利用装置B将浓氨水滴入生石灰制备NH3 , 写出该反应的化学方程式。
-
(5) 下列说法正确的是____。A . 四种气体均可以用无水CaCl2干燥 B . 在制备H2时,可滴加几滴CuSO4溶液以加快反应速率 C . 制备CO2时,稀盐酸可用稀硫酸代替 D . 足量二氧化锰与0.4L10.0mol/L浓盐酸反应,可生成标准状况下22.4L的Cl2 E . 若试剂任选,实验室制备O2可用装置A也可用装置B
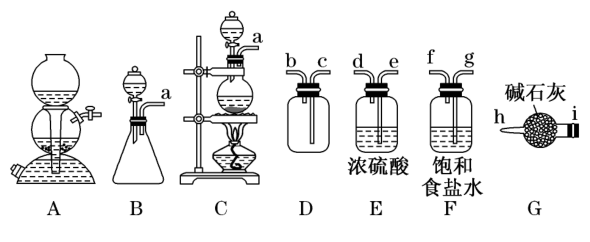
查阅资料:
①亚硝酰氯的熔点为-64.5° C、沸点为-5.5 ℃,气态时呈黄色,液态时呈红褐色。
②亚硝酰氯遇水易反应生成一种氯化物 和两种氮的常见氧化物,其中一种呈红棕色。
请回答下列问题:
-
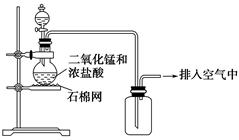
(1) I .Cl2的制备:舍勒制备氯气的方法至今还是实验室制取氯气的主要方法之一。
该反应中被还原与被氧化的物质的物质的量之比为。
-
(2) 欲收集一瓶纯净干燥的氯气,选择图中的装置,其导管连接顺序为a→ →i →h(按气流方向填小写字母标号)。
-
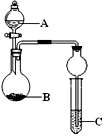
(3) II.亚硝酰氯的制备。实验室可用如图装置制备亚硝酰氯(冰盐水的温度一般在-20~ -10 ℃):
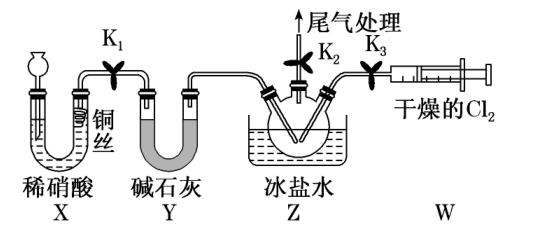
组装好实验装置后应先检查装置气密性,然后装入药品。一段时间后,两种气体在装置Z中反应的现象为。
-
(4) III.亚硝酰氯纯度的测定:将所得亚硝酰氯产品13.10g 溶于水,配制成250 mL溶液;取出25.00 mL,以K2CrO4溶液为指示剂,用0.8 mol·L-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50 mL。(已知: Ag2CrO4 为砖红色固体)
配制溶液时除使用烧杯、玻璃棒、胶头滴管、量筒外,还需用到的玻璃仪器是;当滴入最后半滴AgNO3标准溶液后,出现且半分钟内不消失,即达到滴定终点。
-
(5) 亚硝酰氯(NOCl)与水反应的离子方程式为,亚硝酰氯的质量分数为。
-
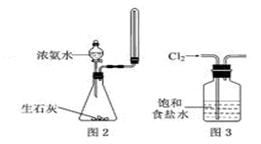
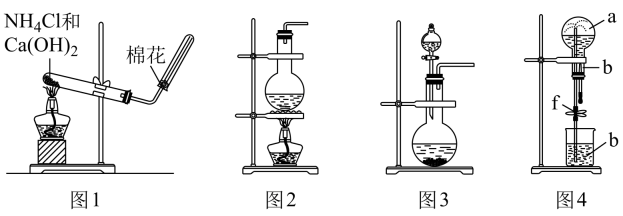
(1) 请写出图1实验室制取氨气的化学方程式。
-
(2) 用图1的装置为什么不能直接加热分解
 制取氨气?
制取氨气?
-
(3) 实验室若采用浓氨水和
 作用制取氨气,则选择的装置是(选填"图2"或"图3")。
作用制取氨气,则选择的装置是(选填"图2"或"图3")。
-
(4) 图4为探究气体溶解性的喷泉实验,圆底烧瓶收集满某易溶于水的气体A进行喷泉实验,若气体A全部被吸收,则所得溶液物质的量浓度为mol/L(可以分数表示或保留两位有效数字)。
-
(5) 现有
 完全溶于适量的浓硝酸中,生成氮的氧化物的混合物(含
完全溶于适量的浓硝酸中,生成氮的氧化物的混合物(含 )共
)共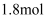 , 这些气体恰好能被
, 这些气体恰好能被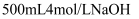 溶液完全吸收,生成只含
溶液完全吸收,生成只含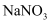 和
和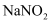 的盐溶液,其中
的盐溶液,其中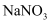 的物质的量为。
的物质的量为。
选项 | 制取气体 | 所选药品 | 收集装置 | |
① | ② | |||
A | NH3 | 浓氨水 | 氧化钙 | ④ |
B | SO2 | 浓硫酸 | 亚硫酸钠 | ④ |
C | CO2 | 醋酸溶液 | 石灰石 | ③ |
D | Cl2 | 浓盐酸 | 二氧化锰 | ③ |
- we arein a stage _________it is still too early to say who
- 为了除去ZnCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,使溶液的pH升高,过滤后再向滤液中加入适量盐酸
- Hesighed again and the failure in physics seemed to have co
- 阅读《螳螂捕蝉》完成11—14题。(16分) 园中有树,其上有蝉,蝉高居悲鸣,饮露,不知螳螂在其后;螳螂委身①曲附②,欲
- 关于物体内能的变化,以下说法中正确的是( ) A.物体吸收热量,内能一定增大 B.物体对外做功,内能一定减小 C.
- 随着经济的发展,科技的进步与综合国力的提升,我国近些年来在两级地区先后建成多个科学考察站.下列考察站位于北极地区的是()
- 孟子主张“民贵君轻”、董仲舒认为“君权神授”、黄宗羲则认为君主专制是“天下之大害”。以下对此解释正确的是 A、儒学思
- 某制鞋公司成立初期,收集了300多件上至先秦下迄民国、不同时期不同民族的具有代表性的鞋,认真研究“张良跪履”、“谢公履”
- 日全食是指在地球上的部分地点,太阳光被月球全部遮住的天文现象。北京时间2015年3月20日15时41分,挪威朗伊尔城(7
- A.褶皱 B.背斜 C.向斜 D.断层
- 在密闭容器中进行可逆反应,A跟B反应生成C,反应速率v(A)、v (B)、v (C)之间存在以下关系:v (B)=3 v
- 下图是等高线地形图上过P点的两幅剖面图,两剖面线垂直相交于P点,则P点所在的地形部位是( )A.山峰 B.盆地
- 若,则的值为( )A. B. C. D.
- 如图,∠MON=30°,A在OM上,OA=2,D在ON上,OD=4,C是OM上任意一点,B是ON上任意一点,则折线ABC
- 近几年,中国铝业有限公司连年巨亏,而国内几大民营铝企却“形势大好”。某民营企业老总分析国企亏损的原因时说:“一是管理不行
- 已知为球的半径,过的中点且垂直于的平面截球面得到圆,若圆的面积为,则球的体积等于______.
- 选出与“项伯杀人,臣活之”中“活”的用法不相同的一项是( ) A、外连横而斗诸侯 B、沛公旦日从百余骑。 C、因利乘便,
- 下列工业上制备物质的过程中,无氧化还原反应发生的是A.合成氨 B.从铝土矿中获得铝 C.玻璃制备
- 社会主义精神文明建设对社会主义物质文明的发展有巨大的反作用,它为物质文明建设提供 ①强大的精神动力 ②重要的智力支持 ③
- 一快艇要从岸边某处到达河中离岸100 m远的浮标处,已知快艇在静水中的速度图象如图甲所示,流水的速度图象如图乙所示,假设

 和浓盐酸
和浓盐酸

 和
和