有关反应热的计算 知识点题库

-
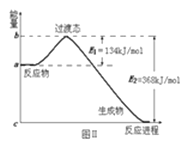
(1) 图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是(选填“A”、“B”或“C”);
-
(2) 20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.
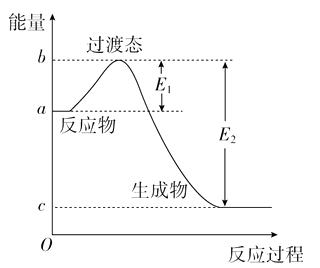
图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:;
-
(3) 过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化.请在图Ⅱ中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图;
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ•mol﹣1;
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ•mol﹣1 .
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
①SiO2(s)+2C(s)═Si(s)+2CO(g)△H=+682.44kJ•mol﹣1 ,
(石英砂) (粗硅)
②Si(s)+2Cl2(g)═SiCl4(g)△H=﹣657.01kJ•mol﹣1
③SiCl4(g)+2Mg(s)═2MgCl2(s)+Si(s)△H=﹣625.63kJ•mol﹣1
(纯硅)
用石英砂生产1.00kg纯硅的总放热为( )
-
(1) 已知20.0gNaOH稀溶液跟足量稀盐酸反应,放出28.68kJ热量,那么此反应数据表明:如果NaOH稀溶液跟稀盐酸中和生成18g水时,该反应放出热量kJ,由此测得的中和热为kJ/mol.
-
(2) 已知断开1molH﹣H键、1mol Br﹣Br键、1mol H﹣Br键分别需要吸收的能量为436kJ、193kJ、366kJ. 计算H2和Br2反应生成1mol HBr需(填“吸收”或“放出”)能量kJ.
①H2(g)+  O2(g)=H2O(g)△H=﹣242kJ/mol;
O2(g)=H2O(g)△H=﹣242kJ/mol;
②2H2(g)+O2(g)=2H2O(l)△H=﹣572kJ/mol;
③C(s)+  O2(g)=CO(g)△H=﹣110.5kJ/moL;
O2(g)=CO(g)△H=﹣110.5kJ/moL;
④C(s)+O2(g)=CO2(g)△H=﹣393.5kJ/moL;
⑤CO2(g)+2H2O(g)=CH4(g)+2O2(g)△H=+802kJ/moL
化学键 | O=O | C﹣C | H﹣H | O﹣O | C﹣O | O﹣H | C﹣H |
键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 |
回答下列问题
-
(1) 写出能表示H2燃烧热的热化学方程式:
-
(2) 计算C(s)+H2O(g)⇌H2(g)+CO(g)△H=kJ/moL;
-
(3) 估算出C=O键能为 kJ/moL.
-
(4) CH4的燃烧热△H=﹣ kJ/moL.
-
(5) 25℃、101kPa下,某燃具中CH4的燃烧效率是90%(注:相当于10%的CH4未燃烧),水壶的热量利用率是70%,则用此燃具和水壶,烧开1L水所需要的CH4的物质的量为 mol[保留到小数点后2位;c (H2O)=4.2J/(g•℃)].
-
(1) 写出过氧化氢的结构式.
-
(2) 写出该反应的化学方程式:.
-
(3) 16g液态肼与足量液态过氧化氢反应生成氮气和水蒸气时,放出的热量为 kJ.
-
(4) 上述反应用于火箭推进剂,除释放大量热和快速产生大量气体外,还有一个很突出的优点是:.
 CH3OH(g)+H2O(g)。下图中是按
CH3OH(g)+H2O(g)。下图中是按  分别为①1:4和②1:6两种投料比时,CO2的平衡转化率随温度变化的曲线。
分别为①1:4和②1:6两种投料比时,CO2的平衡转化率随温度变化的曲线。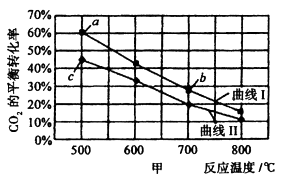
下列有关说法正确的是( )
 的数值,a点比c点小
的数值,a点比c点小
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)  Si(s)+4HCl(g),该反应的反应热△H为 ( )
Si(s)+4HCl(g),该反应的反应热△H为 ( )
 2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是( )
2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是( )
| 化学键 | H-H | O=O | H-O |
| 键能(kJ/mol) | 436 | 496 | 463 |
 CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol; ②N2(g)+O2(g)
CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol; ②N2(g)+O2(g)  2NO(g) ΔH=+180 kJ/mol。则CH4(g)+4NO(g)
2NO(g) ΔH=+180 kJ/mol。则CH4(g)+4NO(g)  CO2(g)+2N2(g)+ 2H2O(l)的 ΔH为( )
CO2(g)+2N2(g)+ 2H2O(l)的 ΔH为( )
主反应Ⅰ:2CH2=CH2(g)+O2(g) 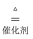 2
2 ![]() (g)
(g) 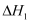 =-210kJ·mol-1
=-210kJ·mol-1
副反应Ⅱ:CH2=CH2(g)+3O2(g) 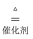 2CO2(g)+2H2O)(l)
2CO2(g)+2H2O)(l) 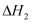 =-1324kJ·mol-1
=-1324kJ·mol-1
Ⅲ.2 ![]() (g)+5O2(g)
(g)+5O2(g) 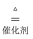 4CO2(g)+4H2O(g)
4CO2(g)+4H2O(g) 
已知:环氧乙烷选择性是指乙烯进行反应Ⅰ生成环氧乙烷的优势。
-
(1)
 =kJ·mol-1。
=kJ·mol-1。
-
(2) ①图1是乙烯转化率、环氧乙烷选择性与流速关系的图象,图中随进料气的流速加快,乙烯的转化率下降,其可能原因是。
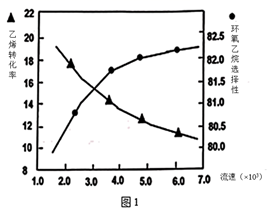
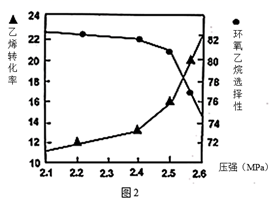
②图2是乙烯转化率、环氧乙烷选择性与压强关系的图象,图中当反应体系的压强高于2.4MPa,环氧乙烷选择性下降,其可能原因是。
-
(3) 实验测得反应Ⅰ中,v正=K正·x2(CH2=CH2)·x(O2),v逆=K逆·x2(
 ),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。 ①若在1L的密闭容器中充2molCH2=CH2(g)和1molO2(g),在一定温度下只发生反应,达到平衡时CH2=CH2的转化率为75%,则该反应平衡常数的值为。
②若平衡后仅升高温度,则下列说法正确的是。
a.x(CH2=CH2)增大,x(
 )减小
)减小b.K正与K逆的比值增大
c.v正减小,v逆增大
d.K正与K逆的比值减小
-
(4) 将乙烯与饱和食盐水的电解产物反应,转化为氯乙醇[CH2(OH)CH2C],氯乙醇进一步反应生成环氧乙烷,其电解简易装置如右图所示。
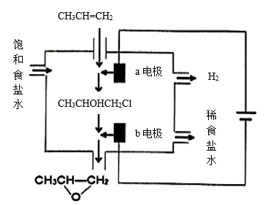
已知:CH2=CH2+H2O+Cl2→CH2(OH)CH2Cl+HCl
①a电极为(选填“阴极”或“阳极”)。
②b电极区域生成环氧乙烷的化学方程式为。
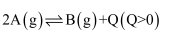 ,下列能量变化示意图正确的是( )
,下列能量变化示意图正确的是( )
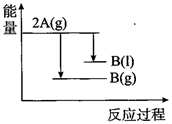 B .
B . 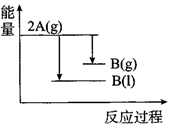 C .
C . 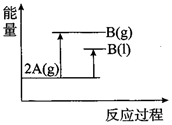 D .
D . 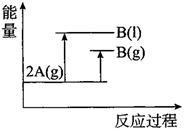
 2NH3(g) ΔH=-akJ·mol-1。一定条件下,将1molN2和3molH2通入2L的恒容密闭容器,反应10min,测得H2的物质的量为2.4mol。下列说法正确的是( )
2NH3(g) ΔH=-akJ·mol-1。一定条件下,将1molN2和3molH2通入2L的恒容密闭容器,反应10min,测得H2的物质的量为2.4mol。下列说法正确的是( )
-
(1) 已知:S(s)+O2(g)=SO2(g) ∆H=-297.2kJ·mol-1 , CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) ∆H=-295.9kJ·mol-1 , 若CH4(g)+2O2(g)=CO2(g)+2H2O(l)反应物的能量为E1 , 则生成物的能量E2是
-
(2) 利用反应:C(s)+SO2(g)
 CO2(g)+S(g),可减少SO2在大气中的排放,在密闭容器中投入足量的反应物,不同实验条件下达到平衡,测得T=600℃下的x(SO2)—p和p=105Pa下—1gKc—t如图所示[x(SO2)表示SO2平衡时含量,Kc表示平衡常数]。该反应的正反应是反应(填“放热”、“吸热”),理由是。
CO2(g)+S(g),可减少SO2在大气中的排放,在密闭容器中投入足量的反应物,不同实验条件下达到平衡,测得T=600℃下的x(SO2)—p和p=105Pa下—1gKc—t如图所示[x(SO2)表示SO2平衡时含量,Kc表示平衡常数]。该反应的正反应是反应(填“放热”、“吸热”),理由是。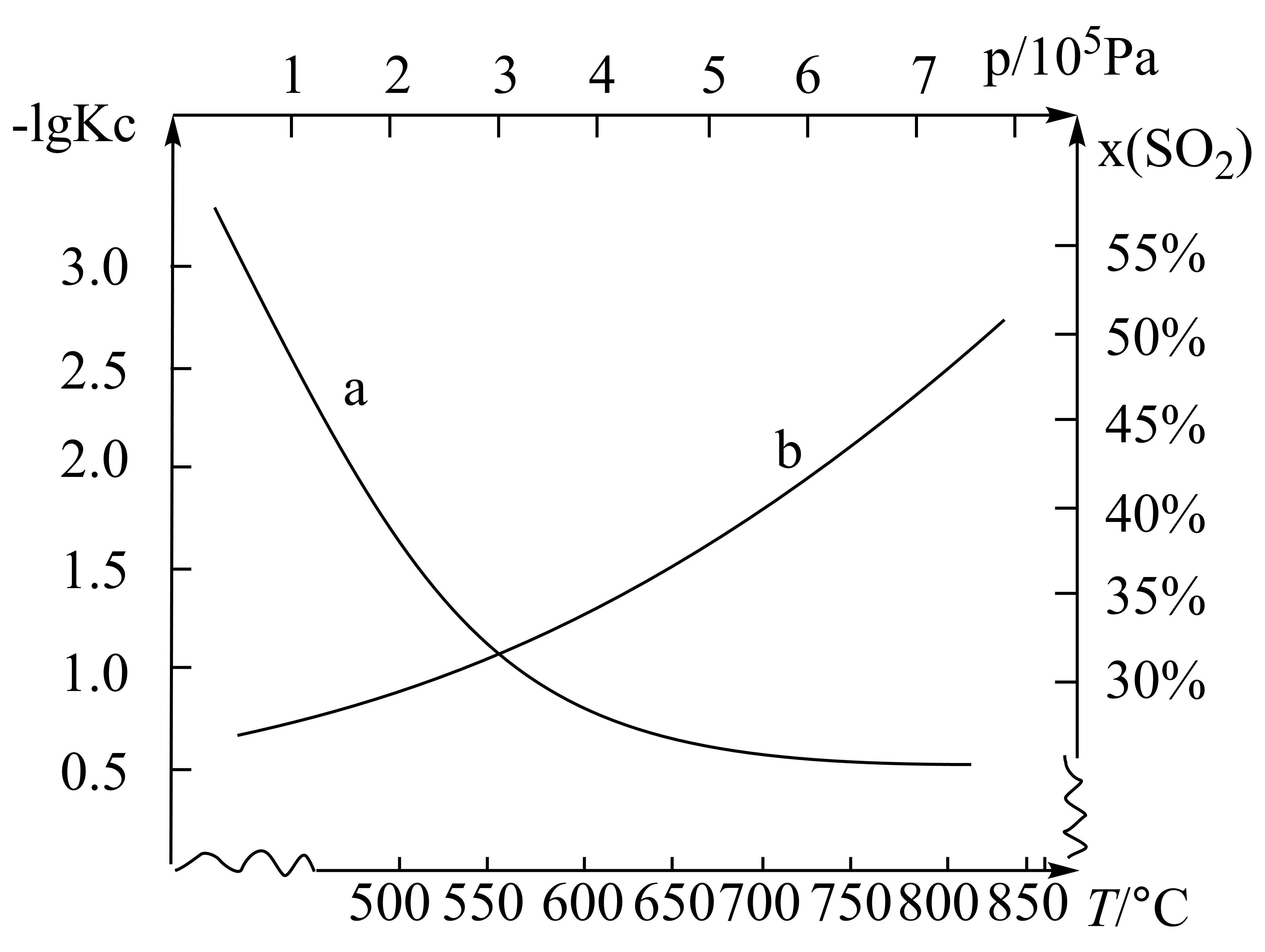
-
(3) 恒温恒容条件下,下列事实不能说明反应C(s)+SO2(g)
 CO2(g)+S(g)达到平衡状态的是____(填字母)
A .
CO2(g)+S(g)达到平衡状态的是____(填字母)
A . 不变
B . v(CO2)正=v(SO2)逆
C . 混合气体的总压强不再改变
D . 混合气体的密度不再改变
不变
B . v(CO2)正=v(SO2)逆
C . 混合气体的总压强不再改变
D . 混合气体的密度不再改变
-
(4) 800℃,在1.0L的恒容密闭容器中投入1.0molSO2和120gC,容器中压强为p0kPa,发生反应C(s)+SO2(g)
 CO2(g)+S(g),5min时容器中CO2的体积分数为20%,10min时达平衡,容器中压强为pkPa时。0~5minv(SO2)kPa·min-1 , 800℃的化学平衡常数Kc=mol/L。
CO2(g)+S(g),5min时容器中CO2的体积分数为20%,10min时达平衡,容器中压强为pkPa时。0~5minv(SO2)kPa·min-1 , 800℃的化学平衡常数Kc=mol/L。
-
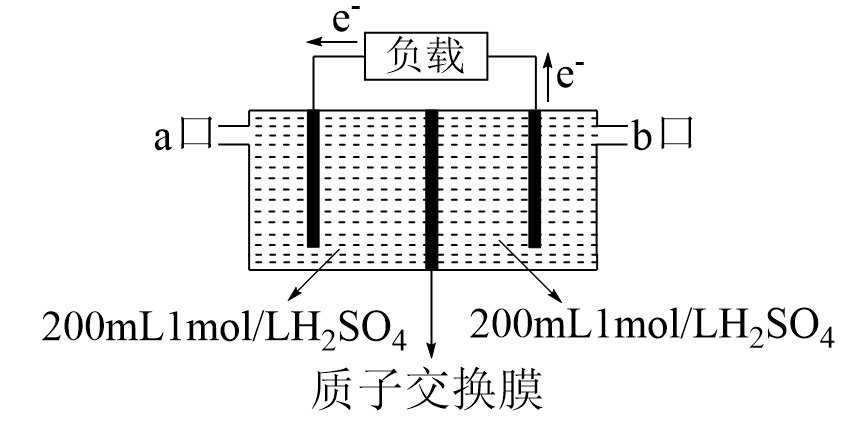
(5) 用电化学原理吸收烟道气中SO2以减少其排放,其装置示意图。H2O2从口进入,电路中通过1mol电子时,正极区溶液的c(H+)将,负极区n(H2SO4)=。
-
(1) 制作有降温、保鲜和镇痛的冷敷袋可以利用(填“放热”或“吸热”)的化学变化或物理变化。
-
(2) “即热饭盒”可利用下面____(填字母序号)反应释放的热量加热食物。A . 生石灰和水 B . 浓硫酸和水 C . 钠和水
-
(3) CH3OH是优质液体燃料,在
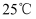 、101 kPa下,充分燃烧1 g CH3OH并恢复到原状态,会释放22.7 kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:。
、101 kPa下,充分燃烧1 g CH3OH并恢复到原状态,会释放22.7 kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:。
-
(4) 已知常温下红磷比白磷稳定,在下列反应中:
①
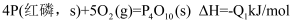
②

若Q1、Q2均大于零,则Q1和Q2的关系为____(填字母序号)。
A .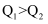 B .
B . 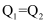 C .
C . 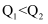 D . 无法确定
D . 无法确定
-
(5) 火箭和导弹表面的薄层是耐高温物质。制得该物质的热化学方程式为
 。该反应中每转移1 mol电子放出的热量为
。该反应中每转移1 mol电子放出的热量为
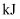 。
。
-
(6) 工业合成氨是人类科学技术的一项重大突破,其反应如下:
 , 若断裂1 mol H-H和1 mol N-H需要吸收的能量分别为436 kJ和391 kJ,则断裂1 mol N≡N需要吸收的能量为
, 若断裂1 mol H-H和1 mol N-H需要吸收的能量分别为436 kJ和391 kJ,则断裂1 mol N≡N需要吸收的能量为
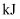 。
。
- 已知函数,若二次函数满足:①与的图象在点处有公共切线;②是上的单调函数.则= .
- 如图,已知抛物线与直线的两个交点分别为A、B,点P在抛物线上从A向B运动(点P不同于点A、B),(Ⅰ)求由抛物线与直线所
- 某农场预算用5600元购买单价为50元(每吨)的钾肥和20元(每吨)的氮肥,希望使两种肥料的总数量(吨)尽可能的多,但氮
- 2007年10月24日,我国第一颗探月卫星“ ”在西昌发射中心成功升空,并于11月26日传回第一张月面图片,
- 一个具有人文主义精神的老师,他对学生的教育态度可能是( ) A.要求学生努力提高考试分数,否则给予惩罚 B.重视体
- 下图是“以极点为中心的半球图”,箭头表示洋流的流向。读图完成12~13题。12.下列叙述正确的是 A.①洋流
- “欲天下之治安,莫若众建诸侯而少其力。”下列举措实践了贾谊这一主张的是 A.秦始皇推行郡县制 B.汉景帝
- 函数的单调增区间为 A., B. C., D.
- The government is now trying to provide _______ health benef
- 如图2-1-1所示,将左边的铜导线和右边的铝导线连接起来,已知截面面积S铝=2S铜,在铜导线上取一截面A,在铝导线上取一
- 若,,,则的大小关系为 ( ) A. B. C. D.
- Everymorning, Mrs. Smith listens to the latest news _______
- 如图,四棱锥P-ABCD中,AD⊥平面PAB,AP⊥AB. (1)求证:CD⊥AP; (2)若CD⊥PD,求证:CD∥平
- 如果等差数列的前 5 个偶数项的和等于 15,前三项的和等于 -3,则 a1 = ,d =
- 关于温度、热量和内能,下列说法错误的是 ( )A.温度高的物体内能一定
- Laptop computers are popular all over the world.People use t
- 选出下列成语运用正确无误的一项:( ) A.他们疼爱孩子,孩子也孝敬他们,一家人相敬如宾,生活美满幸福。 B.台湾前领
- 课文的两个部分之间,是如何过渡的?把这些话找出来,说说是怎样起过渡作用的。 答:____________________
- 在图示期间,与美国相比,我国()A. 城市人口数较少 B. 城市人口数增长率较低 C. 城市人口比重较低 D. 城市人口
- -- My cat’s really fat. --- You ______ have given her so



