化学反应原理 知识点题库
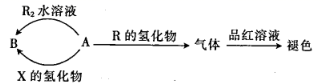
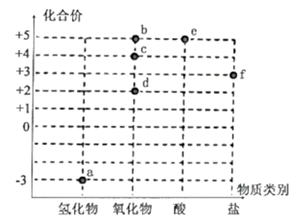
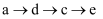 的转化过程中,必须向每个步骤中提供氧化剂
C . c、d同时通入
的转化过程中,必须向每个步骤中提供氧化剂
C . c、d同时通入  溶液中仅生成f一种盐,反应的离子方程式为
溶液中仅生成f一种盐,反应的离子方程式为 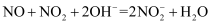 D . a与c在一定条件下反应生成无污染的物质,该反应中氧化剂与还原剂的物质的量之比为3:4
D . a与c在一定条件下反应生成无污染的物质,该反应中氧化剂与还原剂的物质的量之比为3:4
 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以  为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用  人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将  转化为甲醇。
转化为甲醇。 已知:① 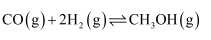
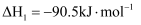
② 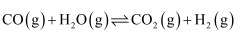
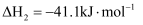
③ 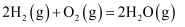
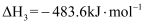
下列说法错误的是( )
 时,放出的热量大于90.5kJ
B .
时,放出的热量大于90.5kJ
B .  与
与  合成甲醇的热化学方程式为:
合成甲醇的热化学方程式为: 
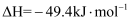 C . 通过电解制
C . 通过电解制  和选用高效催化剂,可降低
和选用高效催化剂,可降低  与
与  合成甲醇的反应的焓变
D . 以
合成甲醇的反应的焓变
D . 以  和
和  为原料合成甲醇,同时生成
为原料合成甲醇,同时生成  ,该反应需要吸收能量
,该反应需要吸收能量
-
(1) 工业上以煤和水为原料通过一系列转化可获得清洁能源氢气。
已知:① C(s) + O2(g) = CO 2 (g) △H 1 = -393.5kJ·mol −1
②
 ΔH2=-571kJ mol−1
ΔH2=-571kJ mol−1③H2O(l) = H2O(g) △H1 = +44kJ·mol−1
则碳与水蒸气反应 C(s) +2H2O(g)
 CO2(g)+2H2(g)的 ΔH = 。
CO2(g)+2H2(g)的 ΔH = 。 -
(2) 工业上也可以仅利用上述反应得到的 CO2 和H2 进一步合成甲醇:
CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) △H<0
CH3OH(g) + H2O(g) △H<0①在某 1L 恒温恒容密闭容器中充入 1mol CO2和 3molH2发生反应,测得 CO2(g)和 CH3OH (g)浓度随时间变化如下图 1 所示。则平衡时H2 (g)的转化率为,该温度下的平衡常数表达式为 K=。

②该反应在催化剂 Cu—ZnO—ZrO 2 表面进行,主反应历程如图 2 所示(催化剂表面吸附的物种用*标注),下列说法不正确的是。
A.该反应的原子利用率为 100%
B.催化剂可以降低反应活化能
C.反应②中,断裂和形成的共价键至少有 2种
D.使用催化剂可以提高反应的转化率
-
(3) 将合成的甲醇进行水蒸气重整是电动汽车氢氧燃料电池理想的氢源。该制氢(SRM)系统简单,产物中2H 含量高、CO 含量低(CO会损坏燃料电池的交换膜),反应如下:
反应Ⅰ(主):CH3OH(g) + H2O(g)
 CO2(g) +3H2(g) △H 1 >0
CO2(g) +3H2(g) △H 1 >0反应Ⅱ(副):CO2(g) + H 2 (g)
 CO(g) + H2O(g) △H 2 >0
CO(g) + H2O(g) △H 2 >0温度高于 300℃会同时发生反应Ⅲ:CH3OH(g)
 CO(g) + 2H 2 (g)
CO(g) + 2H 2 (g)①反应 1能够自发进行的条件是。
②升温有利于提高 CH 3 OH 转化率,但也存在一个明显的缺点是。
③写出一条能提高 CH3OH 转化率而降低 CO生成率的措施。
 B . 氨水
C . 冰醋酸
D . 氯气
B . 氨水
C . 冰醋酸
D . 氯气

已知:整个工艺流程,溶液中的铬元素均为+3价。
-
(1) 写出酸浸时的离子方程式(至少写2个)。
-
(2) 硫化铬属于难溶电解质,FeS和NiS的溶度积如表所示,试剂a为。将NiS固体加入0.1mol/LFeSO4溶液中,分析是否有FeS生成(简述计算过程,
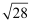 ≈5.3)。
≈5.3)。硫化物
Ksp
FeS
6.3×10-18
NiS
2.8×10-21
-
(3) 加入草酸(H2C2O4)生成草酸亚铁的化学方程式。
-
(4) 为满足冶金及颜料级铬绿的要求,氧化铬产品中铁的质量分数应低于0.03%。一种测定氧化铬中铁含量的操作如下:
ⅰ.称取mg氧化铬产品,用酸溶解;
ⅱ.多步操作分离铁和铬;
ⅲ.取含有Fe3+的溶液,调pH,加入指示剂,用cmol/L的无色EDTA—2Na溶液滴定,共消耗EDTA—2Na标准液VmL。
资料:EDTA—2Na和Fe3+按物质的量1:1反应,低浓度时产物无明显颜色。
①指示剂是,滴定终点的现象为。
②氧化铬产品中铁的质量分数是。
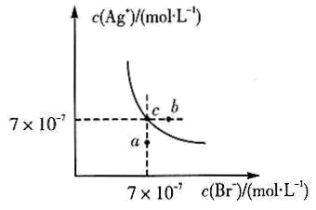
 H++HS-和HS-
H++HS-和HS- H++S2-。对H2S溶液进行如下操作,有关描述正确的是( )
H++S2-。对H2S溶液进行如下操作,有关描述正确的是( )
-
(1) C在元素周期表中的位置为,G的原子结构示意图是。
-
(2) D与E按原子个数比1:1形成化合物甲,其电子式为,其与水反应的化学方程式为。
-
(3) D,E,F,G形成的简单离子,半径由大到小的顺序是。(用离子符号表示)
-
(4) B,C,F,G最高价氧化物对应水化物,酸性最强的是。(填化学式)
-
(5) 写出一种由A、B、C、D四种元素组成的正盐的化学式。
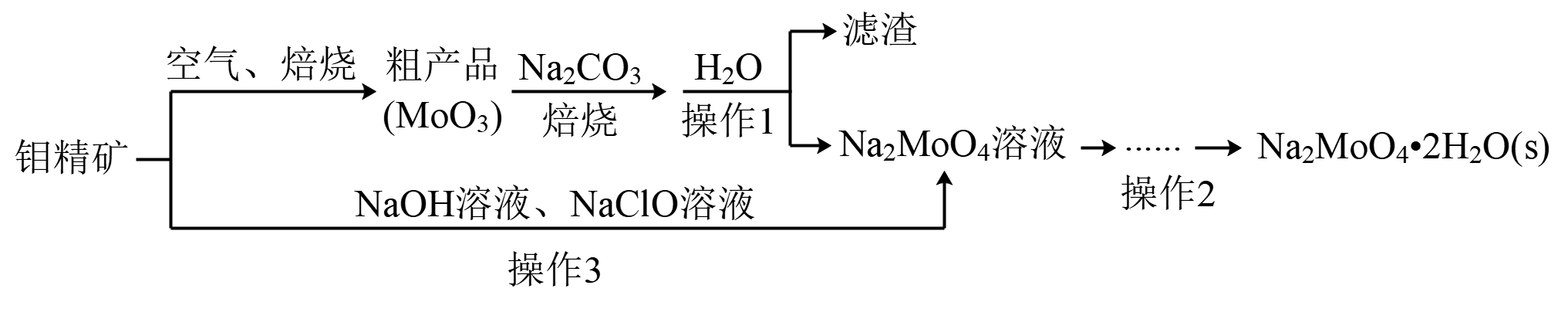
回答下列问题:
-
(1) 可以提高钼精矿焙烧效率的措施有。(任写一种)
-
(2) NaClO的电子式。
-
(3) 粗产品焙烧的化学方程式。
-
(4) 实验室进行操作1所用的玻璃仪器是:烧杯、,操作2的步骤是:、过滤、洗涤、干燥。
-
(5) 操作3中硫元素被氧化为最高价,发生反应的离子方程式为。
-
(6) 钼的化合物间有如下转化关系。八钼酸铵的化学式为:。
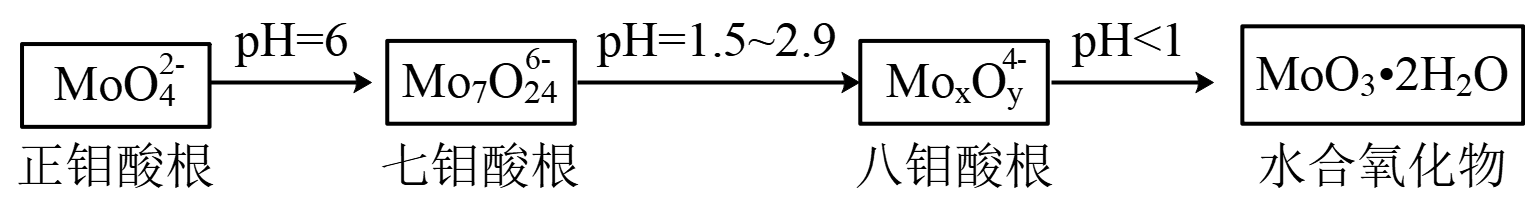
-
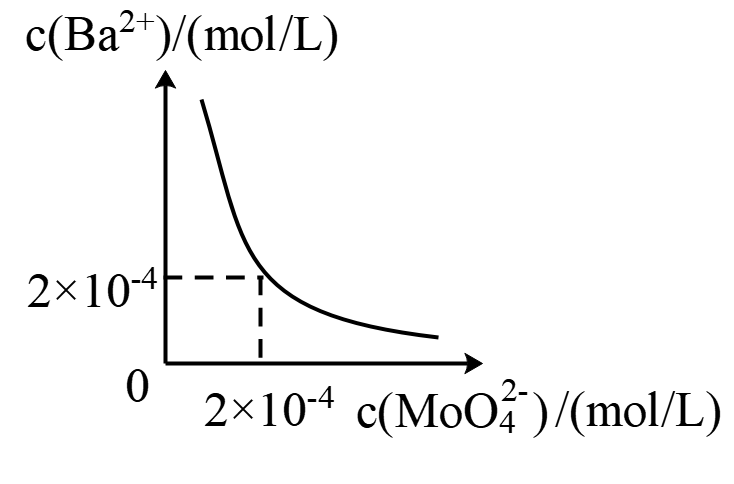
(7) 某温度下,BaMoO4在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于1×10-5mol/L),溶液中Ba2+的浓度应大于mol/L。
 增大,pH不变,仍为中性
B . 常温下,向
增大,pH不变,仍为中性
B . 常温下,向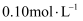 的
的 溶液中加入少量
溶液中加入少量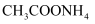 晶体,溶液的pH增大,说明
晶体,溶液的pH增大,说明 溶液存在电离平衡
C . 常温下,酸式盐NaHA的
溶液存在电离平衡
C . 常温下,酸式盐NaHA的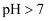 , 则
, 则 一定是弱酸
D . 常温下,等pH的盐酸和醋酸溶液加水稀释10倍后,
一定是弱酸
D . 常温下,等pH的盐酸和醋酸溶液加水稀释10倍后,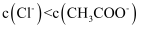
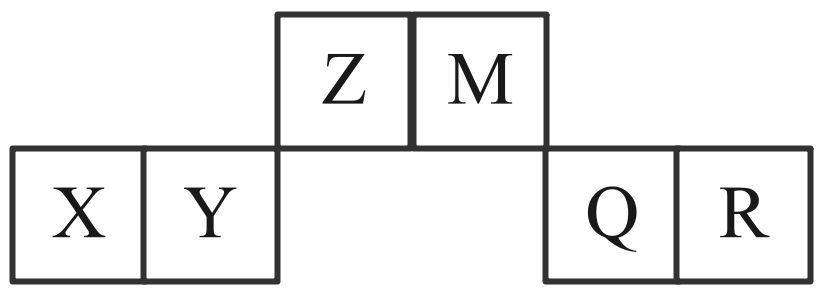
 B . X能从
B . X能从 中置换出Z
C . Y能与
中置换出Z
C . Y能与 反应得到Fe
D . M最高价氧化物的水化物能与其最低价氢化物反应
反应得到Fe
D . M最高价氧化物的水化物能与其最低价氢化物反应
 和
和 合成甲醇:
合成甲醇: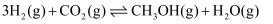 ,
,  也能在一定条件下与
也能在一定条件下与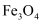 反应,制得“引火铁”,磁铁矿中的
反应,制得“引火铁”,磁铁矿中的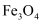 不溶于水和酸,其中的
不溶于水和酸,其中的 和
和 之间存在快速的电子传递。下列有关
之间存在快速的电子传递。下列有关 和磁铁矿中的
和磁铁矿中的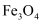 的说法正确的是( )
的说法正确的是( )
 属于电解质
B .
属于电解质
B .  和
和 不能形成分子间氢键
C .
不能形成分子间氢键
C . 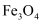 和稀
和稀 反应生成二种硫酸盐
D .
反应生成二种硫酸盐
D . 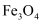 导电能力强于
导电能力强于
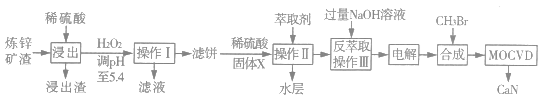
已知:①常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
金属离子 | Fe2+ | Fe3+ | Zn2+ | Ga3+ |
开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
沉淀完全pH | 9.6 | 3.2 | 8.0 | 4.9 |
萃取率(%) | 0 | 99 | 0 | 97~98.5 |
②当溶液中剩余离子的浓度小于10-5mol·L-1时,视为沉淀完全。
③MOCVD:化学气相沉积,以合成的三甲基镓为原料,使其与NH3反应得到GaN。
请回答下列问题:
-
(1) 已知铁酸锌可以用ZnO·Fe2O3表示,写出浸出时铁酸锌参加反应的化学方程式。
-
(2) 浸出后调节pH至5.4的目的是。
-
(3) 固体X最佳选择为,电解过程可得粗镓,则得到金属镓的电极反应式为。
-
(4) 三甲基镓与NH3反应得到GaN的同时获得的副产物为。
-
(5) 滤液中残留的镓离子的浓度为mol·L-1。由滤液可制备ZnC2O4·2H2O,再通过热分解探究其产物,制备ZnC2O4·2H2O时,为提高晶体的纯度,Na2C2O4溶液和滤液混合时应将加入到中,已知ZnC2O4·2H2O的TG-DTA(热重分析一差热分析)曲线如图所示。
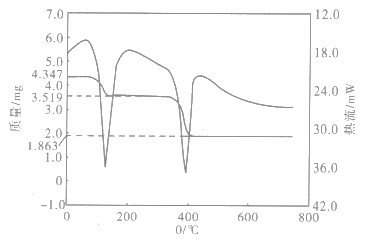
则ZnC2O4·2H2O分解是反应(填“放热”或“吸热”),分解的总化学方程式为。
 Y(g)+Z(g),以下不能说明该反应达到化学平衡状态的是( )
Y(g)+Z(g),以下不能说明该反应达到化学平衡状态的是( )
-
(1) 下列物质中,属于电解质的是(填序号,下同),可以导电的是。
①
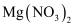 固体②
固体②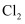 ③酒精④
③酒精④ 溶液⑤碳酸钠溶液⑥
溶液⑤碳酸钠溶液⑥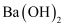 溶液⑦
溶液⑦ ⑧
⑧ 固体
固体 -
(2) 向上述⑤中逐滴加入⑥,写出发生反应的离子方程式:。
-
(3) 某实验小组在对(1)中某些物质进行性质探究实验后,将废液收集得到了澄清的溶液,该澄清溶液中可能含有
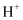 、
、 、
、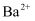 、
、 、
、 、
、 , 取该澄清溶液进行以下实验:
, 取该澄清溶液进行以下实验:①用pH试纸检验。结果表明溶液呈强酸性,可以排除的存在。(填离子符号,下同)
②取出部分溶液逐滴加入NaOH溶液。使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明的存在。
③取部分②中碱性溶液滴加
 溶液,有白色沉淀生成,证明的存在,同时可以排除的存在。
溶液,有白色沉淀生成,证明的存在,同时可以排除的存在。④综上实验,该澄清溶液中肯定存在的离子是。
 的
的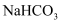 溶液的性质。
溶液的性质。实验 | 实验操作及现象 |
1 | 用pH传感器测定其pH约为8.47 |
2 | 向10mL0.5 |
3 | 向10mL0.5 |
4 | 向10mL0.5 |
下列有关说法正确的是( )
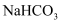 溶液中:
溶液中: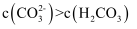 B . 实验2的溶液中微粒浓度存在:
B . 实验2的溶液中微粒浓度存在: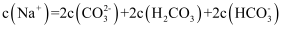 C . 实验3反应静置后的上层清液中存在:
C . 实验3反应静置后的上层清液中存在: D . 实验4中溶液中一定存在:
D . 实验4中溶液中一定存在: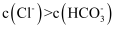
 4NO2(g)+O2(g) △H>0,测得部分实验数据如表所示:
4NO2(g)+O2(g) △H>0,测得部分实验数据如表所示:时间/s | 0 | 500 | 1000 | 1500 |
n(N2O5)/mol | 8 | 5 | 4 | 4 |
则下列说法错误的是( )
- 关于精子变形的叙述错误的是 ( ) A.线粒体退化消失 B.高尔基体
- 下列各组词语,书写全都正确的一组是( )A.糟蹋 副食店 流连忘返 前事不忘
- I saw no more than one copy left in the bookshop. Will you g
- 下列各项与蛋白质的功能无关的是 A.催化生物化学反应 B.调节生命活动 C.帮助
- 可持续发展原则与相关内容的组合你认为合理的是 A.公平性——联合国推广“人与生物圈计划” B.持续性——保持适度的人口规
- 下列制取物质的过程均发生化学变化的是() A. 工业制氧气、实验室制氧气 B. 海水制“碱”、海水淡化 C. 以石英砂等
- 某城市是中国近代历史上最早被迫开放的五处通商口岸之一,改革开放后又是最早建立的四个经济特区之一。该城市是 A.上海
- A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种。他们之间
- 短周期中的A、B、C、D、E 5种元素,原子序数依次增大,A、D同主族;A、B的原子序数之和等于C的原子序数;C2−离子
- 已知双曲线()的离心率为,右准线方程为。 (1)求双曲线的方程; (2)已知直线与双曲线交于不同的两点A、B,且线段AB
- 电荷量为q、质量为m的带电粒子,以水平初速度v0沿电场线方向射入电场中,场强的变化如图6所示(从粒子进入时开始计时).则
- 化学就在我们身边,生活中处处有化学。根据你所学过的化学知识,下列说法错误的是A.体温表中的水银不是银,是金属汞B.熟石灰
- 已知命题,命题,则下列命题为真命题的是
- 下图是某反应的微观变化过程示意图,据此分析错误的是A.化学反应前后原子数目没有变化B.化学反应的本质是原子的重新组合过程
- 如图,二次函数的图象与x轴相交于点A(﹣3,0)、B(﹣1,0),与y轴相交于点C(0,3),点P是该图象上的动点;一次
- 23.用四个关键词提取下面这段话的主要信息。(总共不超过16个字,每空1分共4分) 当药物作用于细菌时,细菌会自卫、防御
- 如图所示(a)(b)中,R和自感线圈L的电阻都很小,接通K,使电路达到稳定,灯泡S发光.下列说法正确的是( )A.
- 赠言是给别人留下的美好祝愿或真诚的希望,它可以增强信心、增进友谊。假如你是高三的同学,在这即将毕业离别之际,你最想把
- 下列物质在空气中放置均会变质,在变质过程中,既有氧化还原反应,又有非氧化还原反应发生的是( ) A.烧碱
- 下表是中国近代参加某一不平等条约签订的部分代表名单。该条约签订后大清钦命全权大臣便宜行事总理外务部和硕庆亲王;总督部堂一



