化学反应原理 知识点题库
 2CO2(g)+6H2(g) △H,测得相同时间内不同水醇比下乙醇转化率随温度变化的关系如图所示。
2CO2(g)+6H2(g) △H,测得相同时间内不同水醇比下乙醇转化率随温度变化的关系如图所示。 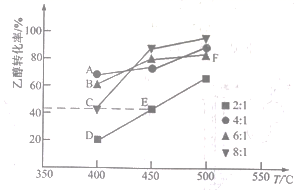
已知:①水醇比为2:1时,各点均已达到平衡状态
②不同的水醇比会影响催化剂的催化效果
下列说法正确的是( )

 H2(g)+
H2(g)+  I2(s) ΔH=-26.5 kJ·mol-1 , 由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量
D . 由C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ·mol-1 , 可知:石墨比金刚石更稳定
I2(s) ΔH=-26.5 kJ·mol-1 , 由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量
D . 由C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ·mol-1 , 可知:石墨比金刚石更稳定
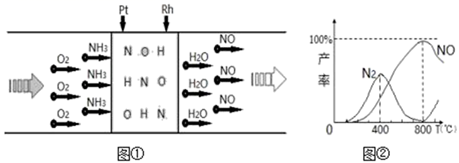
 4NO+6H2O
C . 400℃﹣800℃间,Pt﹣Rh合金对N2的吸附力逐渐减弱
D . 800℃以上,发生了反应:2NO(g)⇌O2(g)+N2(g)△H>0
4NO+6H2O
C . 400℃﹣800℃间,Pt﹣Rh合金对N2的吸附力逐渐减弱
D . 800℃以上,发生了反应:2NO(g)⇌O2(g)+N2(g)△H>0
-
(1) 用单线桥法表示下列反应的电子转移方向和数目。

-
(2) 反应
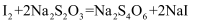 常用于测定溶液中I2的含量。反应的还原剂是,每生成1moLNaI,反应转移电子mol。
常用于测定溶液中I2的含量。反应的还原剂是,每生成1moLNaI,反应转移电子mol。
-
(3) 反应 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中氧化剂与还原剂的物质的量之比为。
-
(4) 高铁酸钾(K2FeO4)可作为高效、多功能水处理剂。用FeCl3与KClO在强碱条件下反应可制取高铁酸钾,完成反应的离子方程式。
2Fe3++_ClO-+_OH-=_FeO
 +3Cl-+_
+3Cl-+_
 在第七十五届联合国大会上发表重要讲话指出,中国将力争于2030年前实现碳达峰,2060年前实现碳中和。“碳中和”是指CO2的排放总量和减少总量相当。下列说法中错误的是( )
在第七十五届联合国大会上发表重要讲话指出,中国将力争于2030年前实现碳达峰,2060年前实现碳中和。“碳中和”是指CO2的排放总量和减少总量相当。下列说法中错误的是( )
主反应:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g)+127.8kJ
CH2=CH2(g)+4H2O(g)+127.8kJ
-
(1) 在容积为2L的恒容密闭容器中充0.4molCO2(g)和1.2molH2(g),若只发生主反应,反应时间2.0min,CO2的转化率为20%,在这段时间内CH2=CH2(g)的平均反应速率为。
-
(2) 在一定温度下,向恒容密闭容器中充入CO2(g)和H2(g),若只发生主反应,下列情况不能说明反应达到平衡的是(填编号)。
A.混合气体密度保持不变B.混合气体总压强保持不变
C.乙烯体积分数保持不变D.平均摩尔质量保持不变
达到平衡后能提高CO2平衡转化率的措施是(任填一条)
-
(3) 在At1、At2、At3三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率(v正-v逆)与温度关系如图所示。
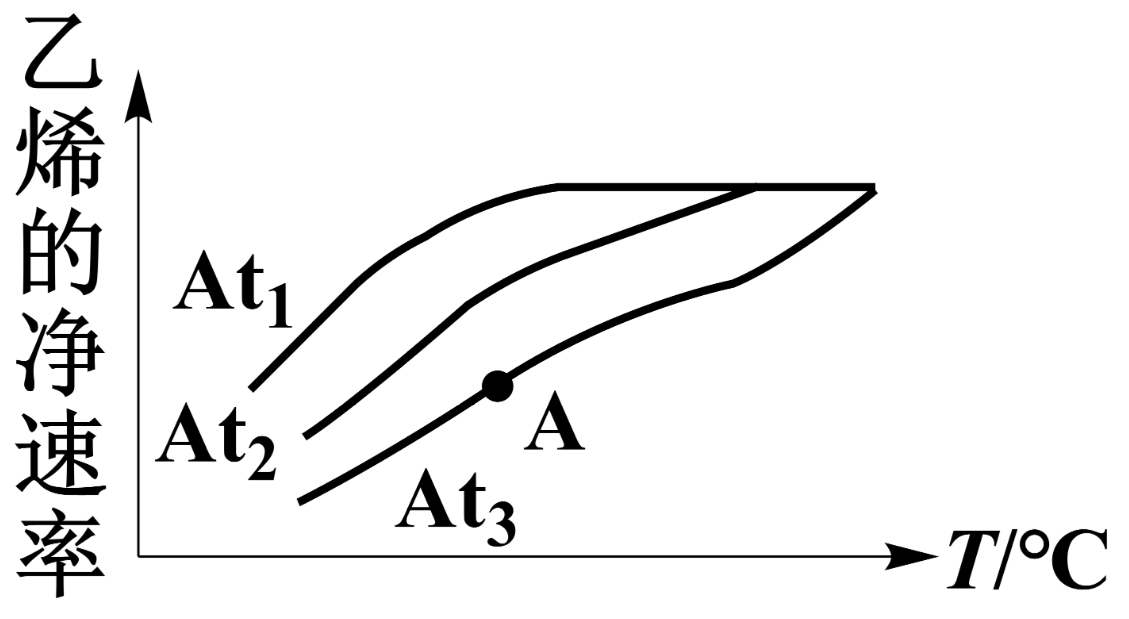
催化效率最高的是(填“At1”、“At2”或“At3”),A点的正反应速率(填“大于”“小于”或“等于”)逆反应速率。
在发生主反应的同时,还发生了副反应:CO2(g)+H2(g)
 HCOOH(g)
HCOOH(g) -
(4) 一定温度下,在容积为2L的恒容密闭容器中充0.4molCO2(g)和1.2molH2(g)同时发生了主反应和副反应,达到平衡时CO2的转化率为45%,C2H4的选择性为80%,则该温度下,副反应的平衡常数K=(结果保留2位小数)。提示:C2H4的选择性=
 ×100%
×100%
-
(5) 0.1mol·L-1的NaOH溶液和0.2mol·L-1的HCOOH(甲酸)溶液等体积混合,得到混合溶液的pH<7,溶液中c(HCOOH)c(Na+)(填“大于”或“小于”),要使c(HCOOH)=c(Na+),可加入。
I.利用二氧化碳催化加氢制甲醇(CH3OH)。
CO2和H2在一定条件下合成甲醇。在2L恒容密闭容器中充入总物质的量为6mol的CO2和H2发生反应: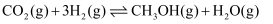 , 改变氢碳比[
, 改变氢碳比[ ],在不同温度下反应达到平衡状态,测得的实验数据如下表。
],在不同温度下反应达到平衡状态,测得的实验数据如下表。
温度/K CO2转化率/%
| 500 | 600 | 700 | 800 |
1.5 | 45 | 33 | 20 | 12 |
2.0 | 60 | 43 | 28 | 15 |
3.0 | 83 | 62 | 40 | 22 |
-
(1) 下列说法中正确的是____(填标号);A . v(CH3OH)=v(CO2)时,反应达到平衡 B . 增大氢碳比,平衡正向移动,平衡常数增大 C . CO2和H2合成甲醇为放热反应 D . 当混合气体密度不变时,达到平衡
-
(2) 在700K、氢碳比为3.0的条件下,若5min时反应达到平衡状态,则0~5min内用H2表示的平均反应速率为;
-
(3) 该反应一般认为通过如下步骤来实现:
①

②
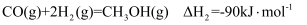
总反应的
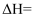
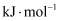 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是(填标号)。
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是(填标号)。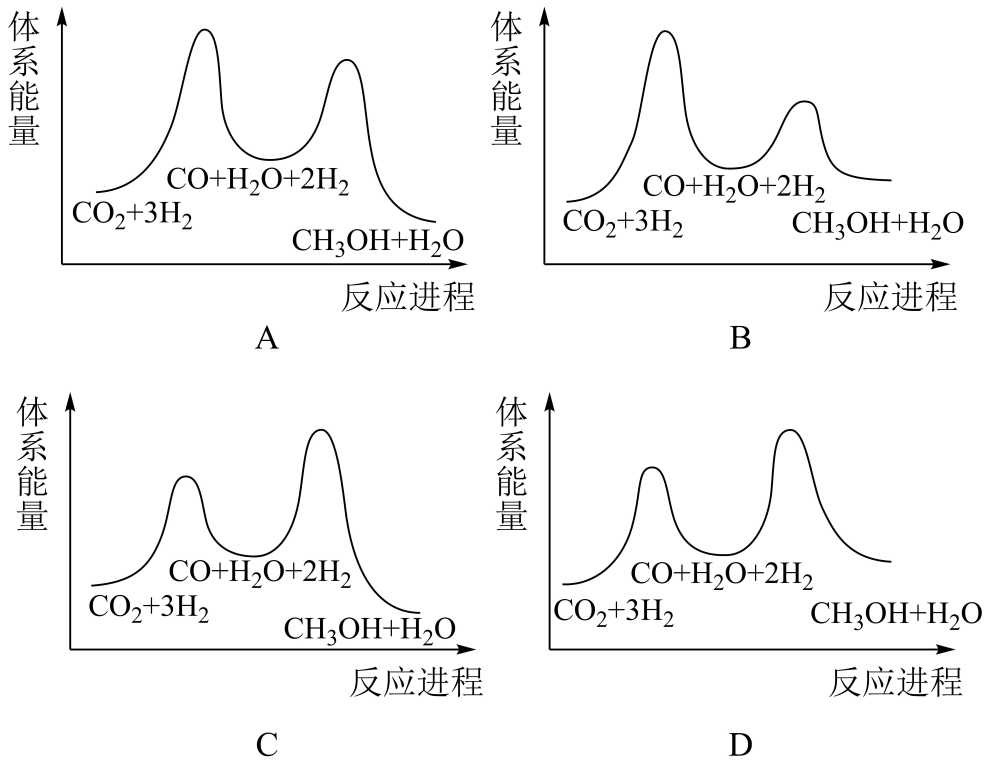
-
(4) II.二氧化碳催化加氢合成乙烯的原理为
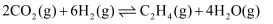 。原料初始组成
。原料初始组成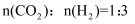 , 体系压强恒定为0.1MPa,不同温度下反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
, 体系压强恒定为0.1MPa,不同温度下反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。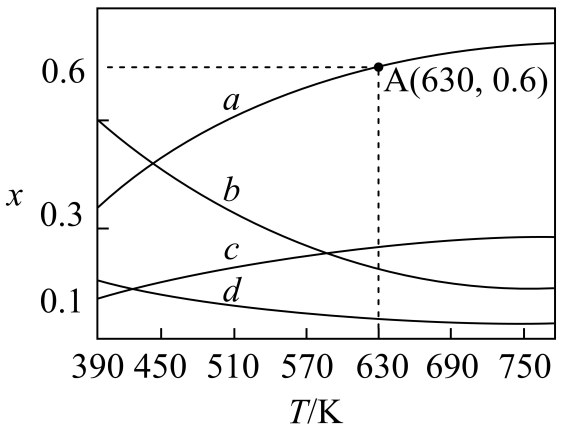
图中曲线a代表四种物质中的(填化学式);
-
(5) 利用A点数据,计算630K时反应的平衡常数Kp=
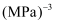 (列出计算式即可。以分压表示,分压=总压×物质的量分数)。
(列出计算式即可。以分压表示,分压=总压×物质的量分数)。
-
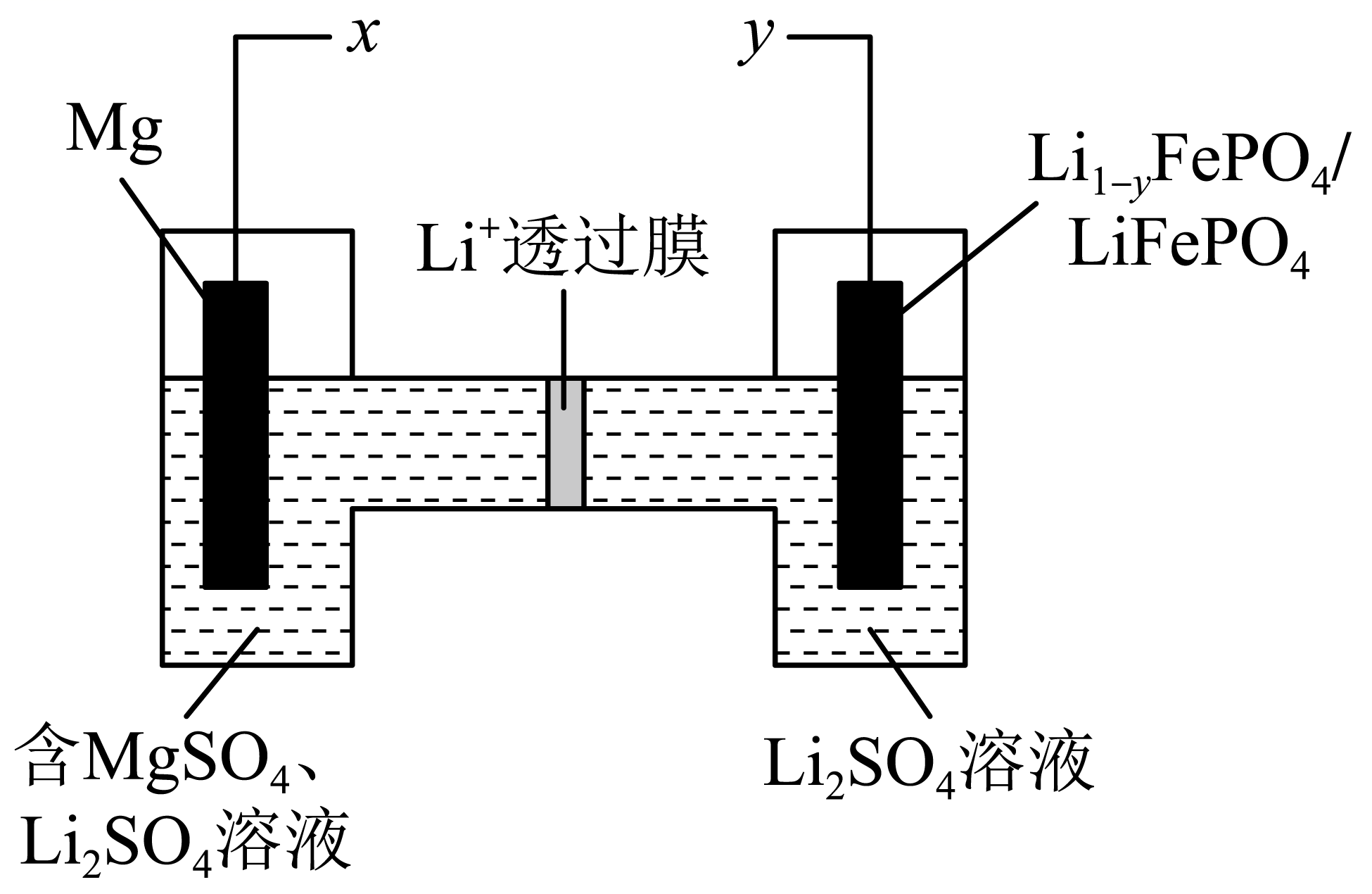
(6) III.电解法转化CO2可实现CO2的资源化利用。
电解CO2制
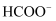 的原理示意图如下所示,反应时阴极电极反应式为。
的原理示意图如下所示,反应时阴极电极反应式为。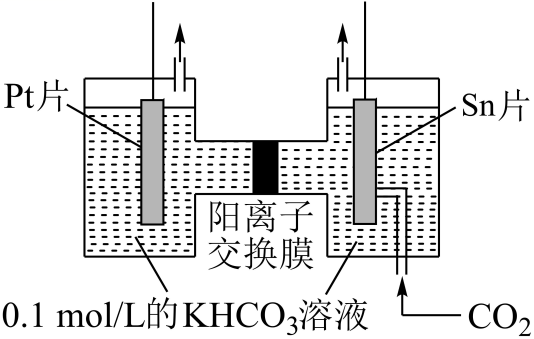
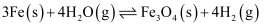 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
 (g)和
(g)和 (g)
C . 保持容器体积不变,移走少量
(g)
C . 保持容器体积不变,移走少量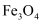 (s)
D . 保持容器压强不变,充入氦气使容器体积变大
(s)
D . 保持容器压强不变,充入氦气使容器体积变大
 )是一种环保、高效、多功能的饮用水处理剂,制备流程如图所示:
)是一种环保、高效、多功能的饮用水处理剂,制备流程如图所示: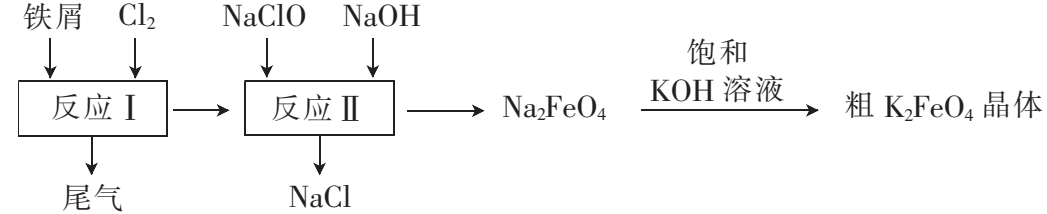
下列叙述不正确的是( )
 对饮用水杀菌消毒的同时,还能吸附杂质起到净化饮用水的作用
B . 用
对饮用水杀菌消毒的同时,还能吸附杂质起到净化饮用水的作用
B . 用 溶液吸收反应Ⅰ中尾气后可再利用
C . 反应Ⅱ中氧化剂与还原剂的物质的量之比为3:2
D . 该生产条件下,物质的溶解性:
溶液吸收反应Ⅰ中尾气后可再利用
C . 反应Ⅱ中氧化剂与还原剂的物质的量之比为3:2
D . 该生产条件下,物质的溶解性:
含钒元素的不同微粒 | VO | VO | V2O | VO |
pH | 4~6 | 6~8 | 8~10 | 10~12 |
另外,V价态不同在溶液中颜色不同,如V2+(紫色)、V3+(绿色)、VO2+(蓝色)、VO (黄色)、VO
(黄色)、VO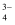 (无色)、V5O
(无色)、V5O (红棕色)等。下列说法正确的是( )
(红棕色)等。下列说法正确的是( )
 转化为V2O
转化为V2O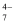 的离子反应为2VO
的离子反应为2VO +H2O=V2O
+H2O=V2O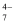 +2H+
B . 含VO
+2H+
B . 含VO 的溶液中滴加氨水有NH4VO3沉淀产生,该过程V元素被还原
C . 酸性VO
的溶液中滴加氨水有NH4VO3沉淀产生,该过程V元素被还原
C . 酸性VO 滴加烧碱溶液,溶液显红棕色时离子反应为5VO
滴加烧碱溶液,溶液显红棕色时离子反应为5VO +8OH-=V5O
+8OH-=V5O +4H2O
D . 紫色VSO4溶液中滴加酸性高锰酸钾溶液,溶液颜色出现绿色→蓝色→黄色,两个过程均失去1mol电子
+4H2O
D . 紫色VSO4溶液中滴加酸性高锰酸钾溶液,溶液颜色出现绿色→蓝色→黄色,两个过程均失去1mol电子
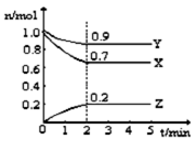
-
(1) 由图中所给数据进行分析,该反应的化学方程式为。
-
(2) 若上述反应中X、Y、Z分别为H2、N2 、NH3 , 某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2 , 一段时间后反应达平衡状态,实验数据如下表所示:
t/s
0
50
150
250
350
n(NH3)
0
0.24
0.36
0.40
0.40
0~50s内的平均反应速率 v(N2) = ,250s时,H2的转化率为。
-
(3) 已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。
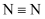 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中(填“吸收”或“放出”)的能量为, 反应达到(2)中的平衡状态时,对应的能量变化的数值为kJ。
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中(填“吸收”或“放出”)的能量为, 反应达到(2)中的平衡状态时,对应的能量变化的数值为kJ。
-
(4) 反应达平衡时容器内混合气体的平均相对分子质量比起始时(填增大、减小或不变),混合气体密度比起始时(填增大、减小或不变)。
-
(5) 为加快反应速率,可以采取的措施是
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH3
 Cu2O+H2↑。下列说法正确的是( )
Cu2O+H2↑。下列说法正确的是( ) 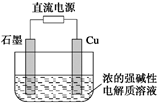
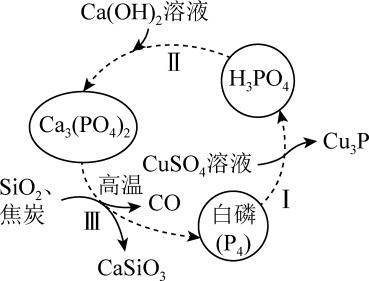
 的空间结构为正四面体形
C . 过程Ⅰ、Ⅱ、Ⅲ中发生的均为氧化还原反应
D . 流程中所涉及元素的基态原子未成对电子数最多的是P
的空间结构为正四面体形
C . 过程Ⅰ、Ⅱ、Ⅲ中发生的均为氧化还原反应
D . 流程中所涉及元素的基态原子未成对电子数最多的是P
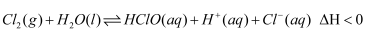 , 达到平衡后,下列说法不正确的是( )
, 达到平衡后,下列说法不正确的是( )
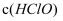 减小
B . 氯水中加入少量醋酸钠固体,上述平衡正向移动,
减小
B . 氯水中加入少量醋酸钠固体,上述平衡正向移动,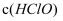 增大
C . 取氯水稀释,
增大
C . 取氯水稀释,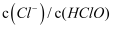 增大
D . 取两份氯水,分别滴加
增大
D . 取两份氯水,分别滴加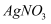 溶液和淀粉
溶液和淀粉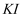 溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度
溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度
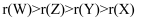 C . W的简单气态氢化物的热稳定性比Z的强
D . Z的最高价氧化物对应水化物的酸性比X的强
C . W的简单气态氢化物的热稳定性比Z的强
D . Z的最高价氧化物对应水化物的酸性比X的强
 2NH3 , 当生成2molNH3时体系放出92.4kJ能量。下列说法正确的是( )
2NH3 , 当生成2molNH3时体系放出92.4kJ能量。下列说法正确的是( )
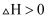 ,
, 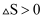 B . 化学反应中的能量变化都是以热能形式表现出来的
C .
B . 化学反应中的能量变化都是以热能形式表现出来的
C . 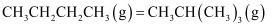
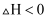 , 则正丁烷比异丁烷稳定
D . 等质量的固态硫与气态硫完全燃烧的反应热(△H),前者小于后者
, 则正丁烷比异丁烷稳定
D . 等质量的固态硫与气态硫完全燃烧的反应热(△H),前者小于后者
- 读下图示意的是东半球,结合图中信息完成1~4题) 1.图中地点甲的纬度为0°经度为 ( ) A.70°E
- —Isthis your book? —No, it is ______book. It belong
- 下列说法正确的是A.需要加热方能发生的反应一定是吸热反应 B.放热反应在常温下一定很容易发生C.反应是放热还是吸热,必须
- 下列计算正确的是( )A.a+2a2=3a2B.a8÷a2=a4C.a3·a2=a6D.(a3)2=a6
- 如图1所示用一根长1m的轻质细绳将一幅质量为1kg的画框对称悬挂在墙壁上,已知绳能承受的最大张力为10N。为使绳不断裂,
- 2007年8月8日晚上8点整,距北京2008年奥运会倒计时一周年,北京天安门广场举行了隆重的庆祝活动,共有205个国家和
- 对于以下三个实验的相关叙述正确的是 () ①观察植物细胞的质壁分离和复原 ②观察DNA、RNA在细胞中的分布
- 《杂文月刊》曾刊登过一篇名为《中国简史》的文章,其中有:“林则徐说:我销;洪秀全说:我反;康有为说:我变;孙中山说:看我
- 为了测量A、B两物体之间的滑动摩擦力,某同学设计了如图所示四个实验方案.在实验操作过程中,当测力计读数稳定时,认为其读数
- 小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如图1:(1)小华同学应称取氯化钠的质量是
- “微电影”是微时代——网络时代的电影形式。“微电影”之“微”在于:微时长、微制作、微投资,以其短小、精练、灵活的形式风
- 假如俄国的农民伊凡,将自己家里的粮食拿到市场上出售,然后将一部分赚得的钱在商店里买了一双马靴。你认为这件事不可能发生于(
- 窑洞这一民居建筑常见于下列哪一个区域:( ) A.吐鲁番盆地 B.黄土高原 C.
- 据有关数据统计,2007年发达国家最终消费率对GDP增长的贡献率约为80%,世界平均水平约为60%,而我国却只有37%。
- 7.阅读下面的文字,完成文后各题。 这一天晚上,少安回家后不多功夫,就被父亲有点神秘地叫到院子里,把刘玉升要重建庙宇的事
- 下列有关细胞器成分及功能的叙述中,错误的是 A.线粒体中含有RNA,能产生ATP和CO2 B.叶绿体中含有DNA,能产生
- 给试管里的物质加热必须使用_________。试管夹应从试管的_________套入,夹在____________。用手
- 在高速发展的信息时代,我们要学会获取和辨别信息,下列信息中正确的是() A. 为了提高粮食产量,应大量使用农药、化肥
- _________the __________ of the class, he played a very beaut
- 下列有关实验装置及用途叙述完全正确的是( )A. a装置检验消去反应后有丙烯 B. b装置检验酸性:盐酸>碳酸>苯



