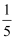化学反应原理 知识点题库
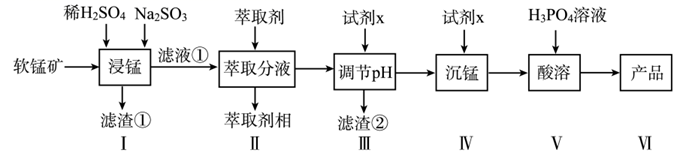
试回答下列问题:
-
(1) 滤渣①的主要成分是;浸锰时,FeO生成Fe3+的离子方程式为,适量的Na2SO3固体的作用是。
-
(2) 检验滤液①中是否含有Fe2+ , 除了用K3Fe(CN)6溶液外,还可以用试剂,若滤液①中含有Fe2+其现象是。
-
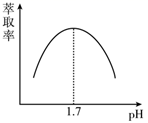
(3) 步骤II中,Fe3+的萃取率与pH的关系如图,如pH>1.7后,随pH增大,Fe3+萃取率下降的原因是。
-
(4) 试剂x为某种钠的正盐,从环保、经济角度,x最好为(写化学式);若c(Mn2+)=1.0 mol·L-1 , 调节pH范围应为(该条件下,Ksp[Al(OH)3]=1.0×10-33 , Ksp[Mn(OH)2]=1.0×10-14)。
-
(5) 步骤V酸溶时逐滴加入H3PO4溶液呈酸性才能保证生成物质较多为Mn(H2PO4)2·2H2O,试结合离子方程式说明原因。
 增大
C . 相同温度下,相同浓度的NH4Cl溶液与(NH4)2SO4溶液pH前者小于后者
D . 相同温度下,足量的氯化银固体分别溶于相同浓度的盐酸和氯化镁溶液中,Ag+的浓度:前者大于后者
增大
C . 相同温度下,相同浓度的NH4Cl溶液与(NH4)2SO4溶液pH前者小于后者
D . 相同温度下,足量的氯化银固体分别溶于相同浓度的盐酸和氯化镁溶液中,Ag+的浓度:前者大于后者
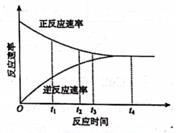
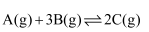 在不同条件下的反应速率表示如下,其中反应进行最快的是( )
在不同条件下的反应速率表示如下,其中反应进行最快的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 向无水乙醇中加入浓硫酸并加热,将产生的气体通入酸性高锰酸钾溶液 | 溶液紫红色褪去 | 产生了乙烯气体 |
B | 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液 | 溶液先变红后褪色 | 溶液中含有SO |
C | 室温下,测定浓度均为0.1mol•L-1的CH3COONa与HCOONa溶液的pH | CH3COONa溶液的pH大 | 结合H+的能力:HCOO-3COO- |
D | 向1mL蛋白质溶液中逐滴加入饱和硫酸铵溶液 | 出现沉淀 | 蛋白质发生变性 |
-
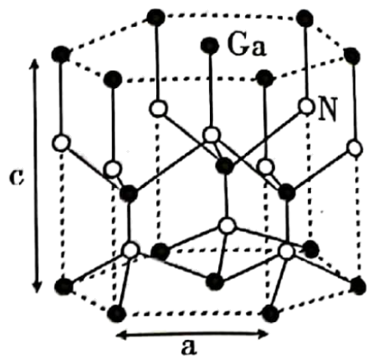
(1) N、Si、Ga三种元素的基态原子中,第一电离能由大到小的顺序是,其中未成对电子数最少原子的外围电子排布式为,该元素位于周期表的区。
-
(2) 制备GaN的工艺中用到GaCl3。GaCl3分子的空间构型为,其中Ga的杂化方式为;GaCl3的熔点为77.9℃,GaN的熔点为1700℃,二者熔点差异的原因是。
-
(3) GaN的一种六方晶胞如图所示,品胞参数为anm、cnm。晶体中N原子的配位数为;晶体密度ρ=g·cm-3(设阿伏加德罗常数的值为NA , 用含a、c、NA的代数式表示)。
 催化重整可得到合成气(
催化重整可得到合成气(  和
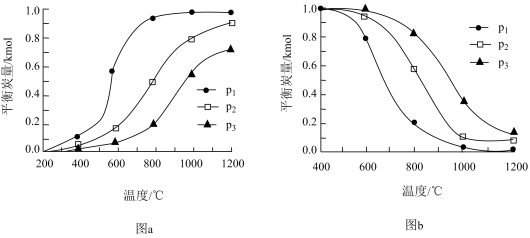
和  ),其主要反应为
),其主要反应为 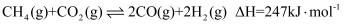 。同时存在以下反应:
。同时存在以下反应: 积碳反应: 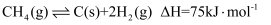 ;
;
消碳反应: 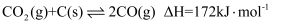
在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。
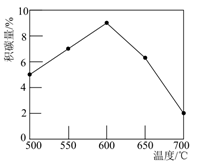
下列说法正确的是( )
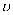 消(消碳反应速率)增加的倍数比
消(消碳反应速率)增加的倍数比 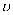 积(积碳反应速率)增加的倍数大
D . 升高温度K积(积碳反应平衡常数)减小、K消(消碳反应平衡常数)增加
积(积碳反应速率)增加的倍数大
D . 升高温度K积(积碳反应平衡常数)减小、K消(消碳反应平衡常数)增加
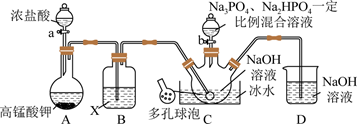
已知:①“消洗灵”是一种含氯消毒剂,消毒原理与“84消毒液”相似
②磷酸三钠对金属表面具有一定的保护作用
回答下列问题:
-
(1) a仪器的名称为,X试剂为。
-
(2) C中采用多孔球泡的目的是。
-
(3) Na10P3O13Cl·5H2O中氯元素的化合价为,C中Na3PO4与Na2HPO4的物质的量之比为1:2,则C中反应的化学方程式为。
-
(4) “消洗灵”对医疗器械消毒比“84消毒液”效果好,原因是。
-
(5) 产品纯度测定(Na10P3O13Cl·5H2O的摩尔质量为656.5 g/mol)。
①取6.565g待测试样溶于蒸馏水配成250 mL溶液;
②取20.00 mL待测液于锥形瓶中,加入10 mL2 mol/L稀硫酸、25mL0.1 mol/L碘化钾溶液(过量),此时溶液出现棕色;
③滴入3滴5%淀粉溶液,用0.05 mol/L硫代硫酸钠溶液滴定至终点,消耗硫代硫酸钠溶液20.00 mL。已知:2
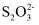 +I2=
+I2= 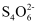 +2I- , 达到滴定终点的现象为,产品的纯度为。
+2I- , 达到滴定终点的现象为,产品的纯度为。
元素符号 | X | Y | Z | R | T |
原子半径(nm) | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
根据表中信息,判断以下说法正确的是( )
|
序号 |
元素 |
结构及性质 |
|
① |
A |
A单质是一种活泼金属,它可以与E的单质反应生成淡黄色固体m |
|
② |
B |
B原子最外层电子数是内层电子总数的 |
|
③ |
C |
C是常见化肥的主要元素,单质常温下呈气态 |
|
④ |
D |
D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
|
⑤ |
E |
通常情况下,E没有最高正化合价,A、B、C、D、F都能与E形成化合物 |
|
⑥ |
F |
F在周期表中可以排在ⅠA族,也有人提出可排在ⅦA族 |
-
(1) A原子在周期表中的位置为。
-
(2) B与C形成的化合物的化学式为,它属于化合物(填“离子”或“共价”)。
-
(3) ①F与E可以形成原子个数比分别为2∶1、1∶1的两种无色液态化合物X和Y,写出物质m和X的反应方程式。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的分子构型为,N的分子式为。
-
(1) 在C和O2的反应体系中:
反应1:C(s)+O2(g)=CO2(g) ΔH1=-394kJ·mol-1
反应2:2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
反应3:2C(s)+O2(g)=2CO(g) ΔH3。
① 设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是。
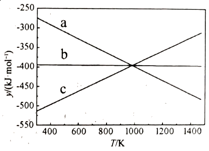
②一定压强下,随着温度的升高,气体中CO与CO2的物质的量之比。
A.不变 B.增大 C.减小 D.无法判断
-
(2) 水煤气反应:C(s)+H2O(g)=CO(g)+H2(g) ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是。
-
(3) 一氧化碳变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41kJ·mol-1。
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPa、p(H2O)=0.25MPa、p(CO2)=0.75MPa和p(H2)=0.75MPa,则反应的平衡常数K的数值为。
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中水蒸气和CO的物质的量之比为。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是。
A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气
④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过程如图2所示。
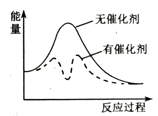
用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:;步骤Ⅱ:。
 催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。
催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。CO岐化:
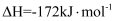
 裂解:
裂解: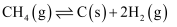
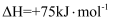
积炭反应中,温度和压强与平衡炭量的关系如下图a所示。
下列说法正确的是( )
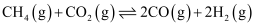
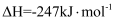 B . 图中压强
B . 图中压强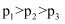 C . 表示温度和压强对
C . 表示温度和压强对 裂解反应中平衡炭量影响的是图b
D . 在重整反应中,低温、高压时会有显著积炭产生,积炭主要由CO岐化反应产生
裂解反应中平衡炭量影响的是图b
D . 在重整反应中,低温、高压时会有显著积炭产生,积炭主要由CO岐化反应产生
 (三氯六氨合钴)是一种重要的化工产品,常用于合成其他Co(Ⅲ)配合物,以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
(三氯六氨合钴)是一种重要的化工产品,常用于合成其他Co(Ⅲ)配合物,以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
-
(1) Ⅰ.氯化钴的制备。
已知氯化钴(CoCl2)易潮解,Co(Ⅲ)的氧化性强于Cl2 , 可用高熔点金属钴与氯气反应制取。
实验室提供下图装置进行组合(连接用橡胶管省略):
A中用于滴加液体的仪器名称是;用上图中的装置组合制备氯化钴,连接顺序为:A→。
-
(2) 用正确的连接装置进行实验,C的作用是。
-
(3) Ⅱ.三氯六氨合钴晶体的制备(流程如下)。
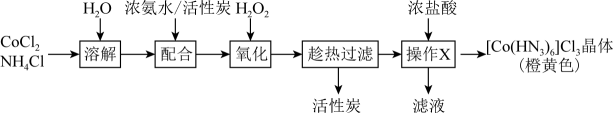
“氧化”应控温在60℃进行,控温方式可采取。
-
(4) 制备
 总反应的化学方程式为。反应中活性炭的作用是(填标号)。
总反应的化学方程式为。反应中活性炭的作用是(填标号)。a.脱色剂 b.氧化剂 c.还原剂 d.催化剂
-
(5) 在
 中Co、N、H三种元素的电负性由大到小的顺序为;在元素周期表中,Co分布在区。
中Co、N、H三种元素的电负性由大到小的顺序为;在元素周期表中,Co分布在区。
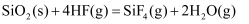 , 下列反应速率关系正确的是( )
, 下列反应速率关系正确的是( )
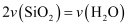 B .
B . 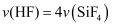 C .
C . 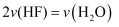 D .
D . 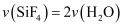
- 漫画《有口难辩》告诉我们 ①要尊重书本知识,尊重权威 ②做到不唯上,不唯书,只唯实 ③追求真理是一个永无止境的过程
- 2010年1月15日,本世纪首场日环食在天空中上演,这是近22年来首次在中国发生的日环食。日环食从中非西部开始,15点0
- 阅读下面的一首宋词,然后回答问题。(6分) 满 庭 芳 周邦彦 风老莺雏,雨肥梅子,午阴嘉树清圆。地
- 对于可逆反应:2A(g)+B(g) 2C(g); △H<0,下列各图正确的是 A
- 已知某星球的质量是M,一颗卫星绕该星球做匀速圆周运动,卫星的轨道半径是r,万有引力常量是G。根据所给的条件可求出的物理量
- 如图所示,电源的电动势为E,内电阻为r外电路接有定值电阻R1和滑动变阻器R,合上开关S,当滑动变阻器的滑动头P从R的最左
- 我寄愁心与明月,_____________________。 (《闻王昌龄左迁龙标遥有此寄》)
- 阅读下面的内容,完成下面4题 睡美人 清丽、优美的芭蕾舞剧《睡美人》序曲奏响了。可是扮演公主奥罗拉的A角却突然“失踪”了
- 在由计划经济体制向社会主义市场经济体制转变的过程中,最根本的转变是( ) A、资源配置方式的转变 B、分配
- 阅读下面的文字,根据要求作文。 闻一多先生用诗的语言表达了他对色彩的感悟:“生命是张没价值的白纸,自从绿给了我发展,红给
- 古诗词是古人留给我们的宝贵精神财富。下列诗词中涉及化学变化的是() A.日照香炉生紫烟B.何意百炼钢,化为绕指柔C.白玉
- 如图所示,用两个定滑轮和一个动滑轮组成滑轮组,每个滑 轮重为30N.用这个滑轮组把重300N的物体匀速提升2m,不计绳重
- 某些金银首饰加工者在为顾客打造黄金首饰如戒指、耳环时,会偷窃部分黄金,为防顾客发现短斤少两,又会在首饰中掺入黄铜,达到欺
- 18.根据语境,仿照划线的句子,在横线上补写出合适的句子。(3分) 山,包罗万物,孕育生灵,默默奉献之态可谓仁哉水,
- Attention, coffee lovers! We have for you, the best coffee m
- 2006年7月1日,青藏铁路全线胜利建成通车。青藏铁路的建设者们发扬创新精神,依靠科技力量创造性地解决了高寒缺氧、多年冻
- 下列有关DNA复制、转录、翻译的叙述中,正确的是 A.转录和翻译发生的部位相同 B.转录需要以信使RNA为模板,以核糖核
- (09年雅礼中学月考理)已知数列:1,1,2,1,1,3,1,1,1,4,1,1,1,1,5,…,,…….(i)对应的项
- ......
- 根据下列四种微粒的结构示意图判断下列说法正确的是( ) ①它们属于不同种元素 ②它们的核外电子排布相同 ③它们都
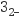 或HSO
或HSO