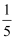化学反应原理 知识点题库
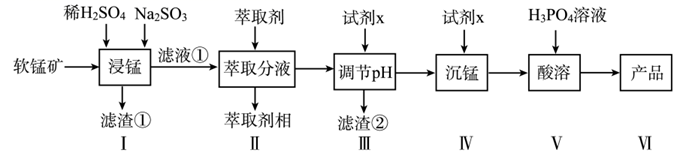
试回答下列问题:
-
(1) 滤渣①的主要成分是;浸锰时,FeO生成Fe3+的离子方程式为,适量的Na2SO3固体的作用是。
-
(2) 检验滤液①中是否含有Fe2+ , 除了用K3Fe(CN)6溶液外,还可以用试剂,若滤液①中含有Fe2+其现象是。
-
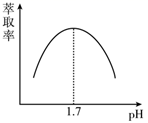
(3) 步骤II中,Fe3+的萃取率与pH的关系如图,如pH>1.7后,随pH增大,Fe3+萃取率下降的原因是。
-
(4) 试剂x为某种钠的正盐,从环保、经济角度,x最好为(写化学式);若c(Mn2+)=1.0 mol·L-1 , 调节pH范围应为(该条件下,Ksp[Al(OH)3]=1.0×10-33 , Ksp[Mn(OH)2]=1.0×10-14)。
-
(5) 步骤V酸溶时逐滴加入H3PO4溶液呈酸性才能保证生成物质较多为Mn(H2PO4)2·2H2O,试结合离子方程式说明原因。
 增大
C . 相同温度下,相同浓度的NH4Cl溶液与(NH4)2SO4溶液pH前者小于后者
D . 相同温度下,足量的氯化银固体分别溶于相同浓度的盐酸和氯化镁溶液中,Ag+的浓度:前者大于后者
增大
C . 相同温度下,相同浓度的NH4Cl溶液与(NH4)2SO4溶液pH前者小于后者
D . 相同温度下,足量的氯化银固体分别溶于相同浓度的盐酸和氯化镁溶液中,Ag+的浓度:前者大于后者
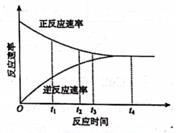
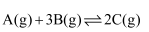 在不同条件下的反应速率表示如下,其中反应进行最快的是( )
在不同条件下的反应速率表示如下,其中反应进行最快的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 向无水乙醇中加入浓硫酸并加热,将产生的气体通入酸性高锰酸钾溶液 | 溶液紫红色褪去 | 产生了乙烯气体 |
B | 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液 | 溶液先变红后褪色 | 溶液中含有SO |
C | 室温下,测定浓度均为0.1mol•L-1的CH3COONa与HCOONa溶液的pH | CH3COONa溶液的pH大 | 结合H+的能力:HCOO-3COO- |
D | 向1mL蛋白质溶液中逐滴加入饱和硫酸铵溶液 | 出现沉淀 | 蛋白质发生变性 |
-
(1) N、Si、Ga三种元素的基态原子中,第一电离能由大到小的顺序是,其中未成对电子数最少原子的外围电子排布式为,该元素位于周期表的区。
-
(2) 制备GaN的工艺中用到GaCl3。GaCl3分子的空间构型为,其中Ga的杂化方式为;GaCl3的熔点为77.9℃,GaN的熔点为1700℃,二者熔点差异的原因是。
-
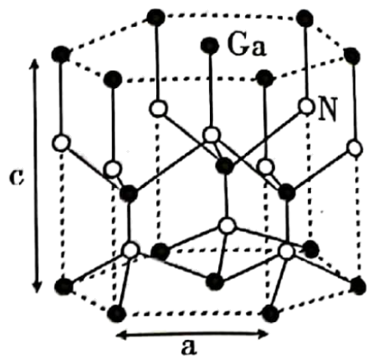
(3) GaN的一种六方晶胞如图所示,品胞参数为anm、cnm。晶体中N原子的配位数为;晶体密度ρ=g·cm-3(设阿伏加德罗常数的值为NA , 用含a、c、NA的代数式表示)。
 催化重整可得到合成气(
催化重整可得到合成气(  和
和  ),其主要反应为
),其主要反应为 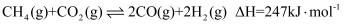 。同时存在以下反应:
。同时存在以下反应: 积碳反应: 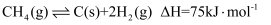 ;
;
消碳反应: 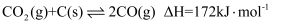
在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。
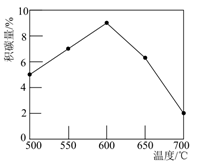
下列说法正确的是( )
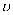 消(消碳反应速率)增加的倍数比
消(消碳反应速率)增加的倍数比 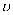 积(积碳反应速率)增加的倍数大
D . 升高温度K积(积碳反应平衡常数)减小、K消(消碳反应平衡常数)增加
积(积碳反应速率)增加的倍数大
D . 升高温度K积(积碳反应平衡常数)减小、K消(消碳反应平衡常数)增加
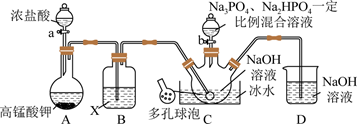
已知:①“消洗灵”是一种含氯消毒剂,消毒原理与“84消毒液”相似
②磷酸三钠对金属表面具有一定的保护作用
回答下列问题:
-
(1) a仪器的名称为,X试剂为。
-
(2) C中采用多孔球泡的目的是。
-
(3) Na10P3O13Cl·5H2O中氯元素的化合价为,C中Na3PO4与Na2HPO4的物质的量之比为1:2,则C中反应的化学方程式为。
-
(4) “消洗灵”对医疗器械消毒比“84消毒液”效果好,原因是。
-
(5) 产品纯度测定(Na10P3O13Cl·5H2O的摩尔质量为656.5 g/mol)。
①取6.565g待测试样溶于蒸馏水配成250 mL溶液;
②取20.00 mL待测液于锥形瓶中,加入10 mL2 mol/L稀硫酸、25mL0.1 mol/L碘化钾溶液(过量),此时溶液出现棕色;
③滴入3滴5%淀粉溶液,用0.05 mol/L硫代硫酸钠溶液滴定至终点,消耗硫代硫酸钠溶液20.00 mL。已知:2
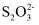 +I2=
+I2= 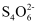 +2I- , 达到滴定终点的现象为,产品的纯度为。
+2I- , 达到滴定终点的现象为,产品的纯度为。
元素符号 | X | Y | Z | R | T |
原子半径(nm) | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
根据表中信息,判断以下说法正确的是( )
|
序号 |
元素 |
结构及性质 |
|
① |
A |
A单质是一种活泼金属,它可以与E的单质反应生成淡黄色固体m |
|
② |
B |
B原子最外层电子数是内层电子总数的 |
|
③ |
C |
C是常见化肥的主要元素,单质常温下呈气态 |
|
④ |
D |
D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
|
⑤ |
E |
通常情况下,E没有最高正化合价,A、B、C、D、F都能与E形成化合物 |
|
⑥ |
F |
F在周期表中可以排在ⅠA族,也有人提出可排在ⅦA族 |
-
(1) A原子在周期表中的位置为。
-
(2) B与C形成的化合物的化学式为,它属于化合物(填“离子”或“共价”)。
-
(3) ①F与E可以形成原子个数比分别为2∶1、1∶1的两种无色液态化合物X和Y,写出物质m和X的反应方程式。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的分子构型为,N的分子式为。
-
(1) 在C和O2的反应体系中:
反应1:C(s)+O2(g)=CO2(g) ΔH1=-394kJ·mol-1
反应2:2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
反应3:2C(s)+O2(g)=2CO(g) ΔH3。
① 设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是。
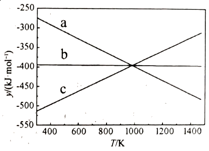
②一定压强下,随着温度的升高,气体中CO与CO2的物质的量之比。
A.不变 B.增大 C.减小 D.无法判断
-
(2) 水煤气反应:C(s)+H2O(g)=CO(g)+H2(g) ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是。
-
(3) 一氧化碳变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41kJ·mol-1。
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPa、p(H2O)=0.25MPa、p(CO2)=0.75MPa和p(H2)=0.75MPa,则反应的平衡常数K的数值为。
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中水蒸气和CO的物质的量之比为。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是。
A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气
④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过程如图2所示。
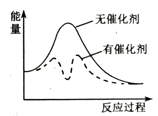
用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:;步骤Ⅱ:。
 催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。
催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。CO岐化:
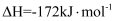
 裂解:
裂解: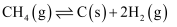
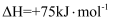
积炭反应中,温度和压强与平衡炭量的关系如下图a所示。
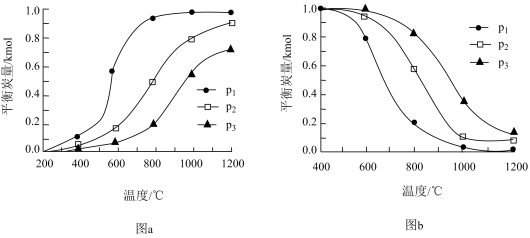
下列说法正确的是( )
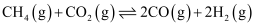
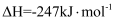 B . 图中压强
B . 图中压强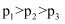 C . 表示温度和压强对
C . 表示温度和压强对 裂解反应中平衡炭量影响的是图b
D . 在重整反应中,低温、高压时会有显著积炭产生,积炭主要由CO岐化反应产生
裂解反应中平衡炭量影响的是图b
D . 在重整反应中,低温、高压时会有显著积炭产生,积炭主要由CO岐化反应产生
 (三氯六氨合钴)是一种重要的化工产品,常用于合成其他Co(Ⅲ)配合物,以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
(三氯六氨合钴)是一种重要的化工产品,常用于合成其他Co(Ⅲ)配合物,以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
-
(1) Ⅰ.氯化钴的制备。
已知氯化钴(CoCl2)易潮解,Co(Ⅲ)的氧化性强于Cl2 , 可用高熔点金属钴与氯气反应制取。
实验室提供下图装置进行组合(连接用橡胶管省略):
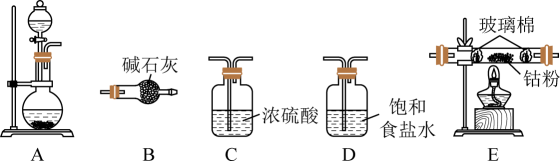
A中用于滴加液体的仪器名称是;用上图中的装置组合制备氯化钴,连接顺序为:A→。
-
(2) 用正确的连接装置进行实验,C的作用是。
-
(3) Ⅱ.三氯六氨合钴晶体的制备(流程如下)。
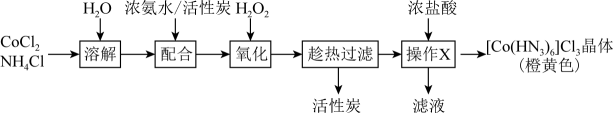
“氧化”应控温在60℃进行,控温方式可采取。
-
(4) 制备
 总反应的化学方程式为。反应中活性炭的作用是(填标号)。
总反应的化学方程式为。反应中活性炭的作用是(填标号)。a.脱色剂 b.氧化剂 c.还原剂 d.催化剂
-
(5) 在
 中Co、N、H三种元素的电负性由大到小的顺序为;在元素周期表中,Co分布在区。
中Co、N、H三种元素的电负性由大到小的顺序为;在元素周期表中,Co分布在区。
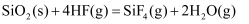 , 下列反应速率关系正确的是( )
, 下列反应速率关系正确的是( )
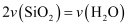 B .
B . 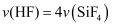 C .
C . 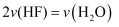 D .
D . 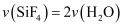
- 没有细胞结构的微小生物是——( )。
- 依次填入下列各句横线处的词语.最恰当的一组是 ①著名律师朱妙春在谈到自己的创作体会时说,他写书的目的是“将自已的经验和教
- 在全国政协提案委员会关于海水利用的提案协商办理座谈会综述:“水资源不仅是涉及民族发展的问题,而且是涉及民族生存的问题”。
- 下列各项不属于动物行为的是( ) A、母鸡下蛋 B、猫吃老鼠 C、竖起耳朵 D、心脏跳动
- 下图是我国黄淮海地区某地的土地利用现状图,读后回答问题。根据图中信息可知,该地最容易发生的自然灾害是_______ ,判
- 2011年11月19日,温家宝总理在东亚领导人系列峰会上就南海问题阐明中方立场时强调,南海争议应由直接有关的
- 如题20 图所示电路中,电源电压保持不变,灯L 标有“6V0.5A”,字样,定值电阻R 的阻值为6Ω。闭合开关S 时,灯
- 潮汐现象主要是由于月球对地球的不同部分施加不同的万有引力而产生的。可以近似认为地球表面均有水覆盖,如果地球与月球的相对位
- (本小题满分12分) 已知函数. (1)若,求函数的极值; (2)若对任意的,都有成立,求的取值范围.
- 图3中雄伟壮观的布达拉宫位于( ) A.云贵高原B.内蒙古高原C.黄土高原D.青藏高原
- 《中国对外开放的新里程碑》:“如果说1971年中国恢复在联合国的合法席位,从此登上政治大舞台;那么,30年后……标志中国
- 很多文字专家指出,欧洲各国媒体发出的报道不夹带他国文字,因为他们认为使用本国文字就能够把要说的话表达清楚。中国的媒体却出
- 下面哪项有关密码子转录的叙述是不真实的? A含有3种核苷酸 B是基因密码的基本单位 C对相同的氨基酸可
- 物体以12 m/s的初速度从斜面底端冲上倾角为37°的斜坡,已知物体与斜面间的动摩擦因数为0.25,g取10 m/s2,
- 已知函数,若函数有三个零点,则实数 的取值范围是 。
- (·黑龙江省哈三中高三上月月考) 30. ---Where did you meet him? ---I
- 如图6所示,甲图中AB和CD是长度不同,粗细相同的镍铬合金线,乙图中AB和CD是长度相同,粗细不同的镍铬合金线,用图示装
- 如图18-3-9所示,平行板电容器和电池组相连.用绝缘工具将电容器两板间的距离逐渐增大的过程中,关于电容器两极板间的电场
- 若用实验证明FeCl3溶液显黄色不是由Cl-造成的,下列实验无意义的是() A.观察KCl溶液的颜色 B.向FeCl3溶
- 阿杜的《天黑》异常受FANS们的追捧,尤其其中一句“闭上眼睛就是天黑”传达了一种对现实生活的逃避,更是受到许多年轻人的追
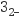 或HSO
或HSO