化学反应原理 知识点题库
-
(1) 以CO2和乙苯为原料合成的苯乙烯,其过程如图1,有“一步”途径1和“二步”途径2的两种推测:
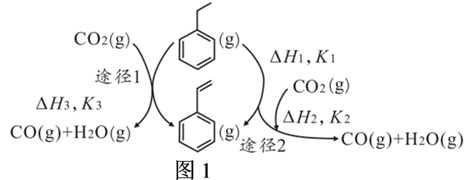
则CO2(g)+
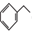 (g)
(g) 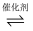
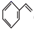 (g)+CO(g)+H2O(g)的K3(用含K1、K2的代数式表达)。
(g)+CO(g)+H2O(g)的K3(用含K1、K2的代数式表达)。 -
(2) 向刚性容器中充入10 mol CO2和10 mol乙苯,发生反应CO2(g)+
 (g)
(g) 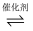
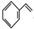 (g)+CO(g)+H2O(g),在不同温度下测得平衡时各物质的体积分数如图2。可知∆H30。相同温度下CO2转化率低于乙苯,推知发生了副反应CO(g)+H2O(g)
(g)+CO(g)+H2O(g),在不同温度下测得平衡时各物质的体积分数如图2。可知∆H30。相同温度下CO2转化率低于乙苯,推知发生了副反应CO(g)+H2O(g)  CO2(g)+H2(g),由图像知该反应∆H0。
CO2(g)+H2(g),由图像知该反应∆H0。 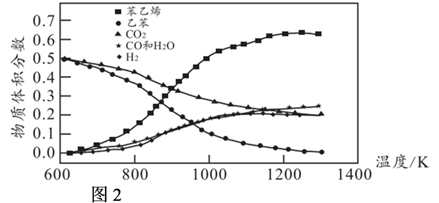
-
(3) 某研究团队找到乙苯直接脱氢的高效催化剂,反应原理如图:
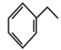 (g)
(g) 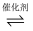 H2(g)+
H2(g)+ 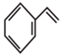 (g) ∆H1
(g) ∆H1①已知部分化学键键能数据如表所示:
共价键
C-C
C-H
C=C
H-H
键能(kJ/mol)
347.7
413.4
615
436
则∆H1=。
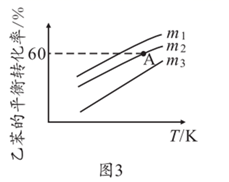
②实际过程中,通常向乙苯中掺入水蒸气,保持体系总压为100 kPa的条件下进行。乙苯平衡转化率与温度、投料比m[m=
 ]的关系如图3。则投料比m1、m2、m3由大到小的关系为。
]的关系如图3。则投料比m1、m2、m3由大到小的关系为。③若m2=5:1,则A点温度下,该反应的平衡常数Kp=。若其他条件不变,将恒压调整为恒容状态,则A点对应的乙苯的平衡转化率(填“增大”、“不变”或“减小”)。
-
(4) 实验测得,乙苯脱氢的速率方程为
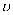 正=k正p乙苯 ,
正=k正p乙苯 , 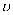 逆=k逆p苯乙烯p氢气(k正、k逆为速率常数,只与温度有关),图4中③代表lgk逆随
逆=k逆p苯乙烯p氢气(k正、k逆为速率常数,只与温度有关),图4中③代表lgk逆随 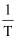 的变化关系,则能代表lgk正随
的变化关系,则能代表lgk正随 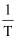 的变化关系的是。
的变化关系的是。 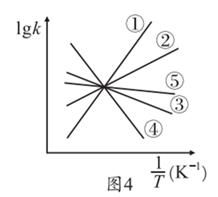
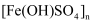 能用作净水剂(絮凝剂),可由绿矾(
能用作净水剂(絮凝剂),可由绿矾(  )与
)与 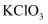 在水溶液中反应得到:
在水溶液中反应得到: 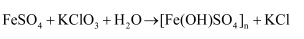 (未配平)下列说法正确的是( )
(未配平)下列说法正确的是( )
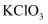 作氧化剂,每消耗
作氧化剂,每消耗 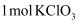 可生成
可生成 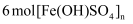 B . 生成聚合硫酸铁后,水溶液的
B . 生成聚合硫酸铁后,水溶液的  变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下,
变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下, 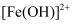 比
比  的水解能力更强
的水解能力更强
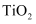 为催化剂,光热化学循环分解
为催化剂,光热化学循环分解  的反应,该反应机理及各分子化学键完全断裂时的能量变化如下图所示。
的反应,该反应机理及各分子化学键完全断裂时的能量变化如下图所示。 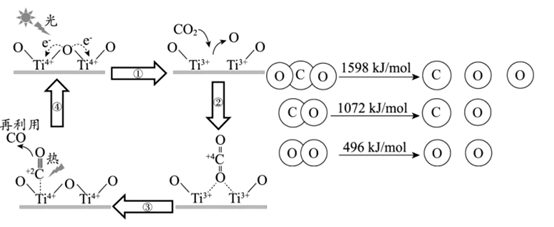
下列说法正确的是( )
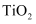 作催化剂可以降低反应的焓变,从而提高化学反应速率
D . 分解
作催化剂可以降低反应的焓变,从而提高化学反应速率
D . 分解  反应的热化学方程式:
反应的热化学方程式: 
-
(1) 汽车尾气净化的主要原理为2NO(g)+2CO(g)
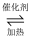 2CO2(g)+N2(g)
2CO2(g)+N2(g) ①在一定条件下,在一个容积固定为 2L的密闭容器中充入 0.8molNO和1.20mol CO,开始反应至 3min时测得 CO 的转化率为20%,则用 N2表示的平均反应速率为 v(N2)=。
②对于气相反应,用某组分(B)的平衡压强 (pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应平衡常数的表达式Kp=。
③在某一绝热,恒容的密闭容器中充入一定量的NO、CO 发生上述反应,测得正反应的速率随时间变化的曲线如图所示(已知 t2~t1=t3~t2)。则下列说法错误的是。(填编号)
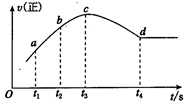
A.反应在 c 点未达到平衡状态 B.反应速率 a 点小于 b 点
C.反应物浓度 a 点大于 b 点 D.NO 的转化率 t1~t2=t2~t3
-
(2) 使用甲醇汽油能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,恒温条件下,在 体积可变的密闭容器中发生反应:CO(g)+2H2(g)
 CH3OH(g),到达平衡时,测得 CO、H2、 CH3OH 分别为 1mol 、1mol 、1mol,容器的体积为 3L,现往容器中继续通入 3molCO ,此时v(正)v(逆)(填‘‘>”、“<’’或“=”)。
CH3OH(g),到达平衡时,测得 CO、H2、 CH3OH 分别为 1mol 、1mol 、1mol,容器的体积为 3L,现往容器中继续通入 3molCO ,此时v(正)v(逆)(填‘‘>”、“<’’或“=”)。
-
(3) 二甲醚也是清洁能源,用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g) 已知一定条件下,该反应中CO的平衡转化率随温度、投料比
 的变化曲线如图:
的变化曲线如图: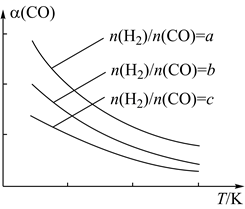
①a、b、c 按从大到小的顺序排序为 。
②某温度下,将 2.0molCO(g)和 4.0mol H2(g)充入容积为 2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的 关系判断正确的是 ;
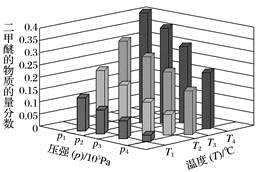
A.p3>p2 , T3>T2 B.p2>p3 , T1>T3 C.p3>p4 , T4>T2 D.p1>p4 , T2>T3
③在恒容密闭容器里按体积比为1∶2 充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应 的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是 。
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数 K 值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小
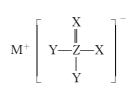
 、NO
、NO  ,则该溶液中还可能大量存在的离子组是( )
,则该溶液中还可能大量存在的离子组是( )
 、Cl-
C . K+、SO
、Cl-
C . K+、SO  、Mg2+
D . Cu2+、I-、Na+
、Mg2+
D . Cu2+、I-、Na+
 。测得SO2的生成速率与S2(g)的生成速率随温度变化如图所示。下列说法正确的是( )
。测得SO2的生成速率与S2(g)的生成速率随温度变化如图所示。下列说法正确的是( ) 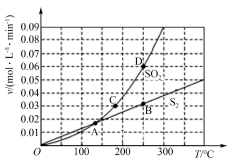
 CH3COCH2Br+HBr。研究反应物浓度与反应速率的关系。反应速率v通过测定溴的颜色消失所需的时间来确定,在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr。研究反应物浓度与反应速率的关系。反应速率v通过测定溴的颜色消失所需的时间来确定,在一定温度下,获得如下实验数据: | 实验序号 | 初始浓度c/mol∙L-1 | 溴颜色消失所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.0010 | 290 |
| ② | 1.60 | x | 0.0010 | 145 |
| ③ | y | 0.40 | 0.0010 | 145 |
| ④ | 0.80 | 0.20 | 0.0020 | 580 |
| ⑤ | 0.80 | 0.20 | 0.0040 | t1 |
-
(1) 表格中x=,y=。
-
(2) 已知该反应速率方程:v=kca(CH3COCH3)cb(HCl)cd(Br2),其中k为仅与温度有关的速率常数。由上表数据可推测出a=,b=,d=。
-
(3) t1=。已知反应物分子一步直接转化为产物的反应称为基元反应,则该反应(填“是”或“不是”)基元反应。
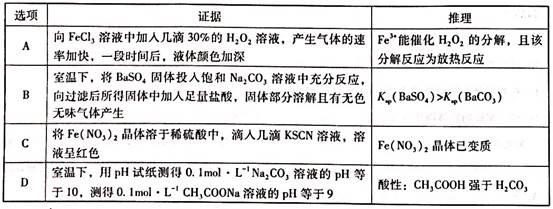
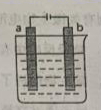
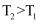 )。则下列说法正确的是( )
)。则下列说法正确的是( )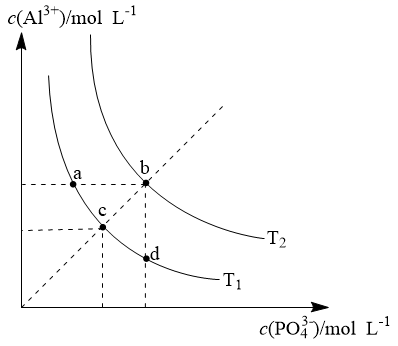
 D . T1温度下,在AlPO4饱和溶液中加入AlCl3固体可使溶液由c点变到a点
D . T1温度下,在AlPO4饱和溶液中加入AlCl3固体可使溶液由c点变到a点
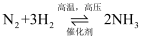 。下列有关说法正确的是( )
。下列有关说法正确的是( )
 浓度可减慢化学反应速率
B . 降低温度可加快化学反应速率
C . 加入催化剂可加快化学反应速率
D . 达到平衡时,
浓度可减慢化学反应速率
B . 降低温度可加快化学反应速率
C . 加入催化剂可加快化学反应速率
D . 达到平衡时, 的转化率为100%
的转化率为100%
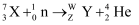 的说法正确的是( )
的说法正确的是( )
 充入
充入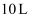 恒容密闭容器中,在一定温度下发生下列反应:①
恒容密闭容器中,在一定温度下发生下列反应:①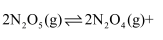

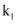 ;②
;②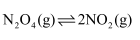
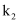 (
(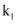 、
、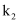 为反应平衡常数)。
为反应平衡常数)。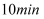 末,该反应达到平衡,此时
末,该反应达到平衡,此时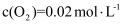 ,
, 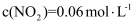 , 下列说法正确的是( )
, 下列说法正确的是( )
 的物质的量分数为
的物质的量分数为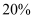 B .
B . 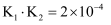 C .
C . 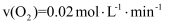 D . 若反应
D . 若反应
 , 则
, 则
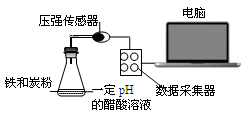
- 今年的海南省中考体育成绩提高到5分,说明国家越来越重视体育运动,对下列体育活动分析正确的是A.仰卧起坐相当于费力杠杆,引
- “第五届国际青少年黑森林文化艺术节”将于2015年7月18日在德国弗洛依登拉开帷幕。届时,来自中国、德国、巴西等国的青
- We all know that the Beijing Olympic Games a great su
- .16~17世纪,英国物价上涨了256%,工资上涨了145%。地租涨幅远远低于物价涨幅。这一现象出现的原因有 ①英国成为
- 如图所示,两个相同的绝缘细圆环带有等量正电荷,电荷在圆环上的分布是均匀的,两圆环相隔一定距离同轴平行固定放置,B、D分别
- 有专家提出水循环可分为自然循环和社会循环两大类,下图为某城市水循环示意图。读图完成6~7题。6.图中①②③⑦分别表示 A
- “嫦娥一号”探月卫星沿地月转移轨道直奔月球,在距月球表面200 km的P点进行第一次变轨后被月球捕获,先进入椭圆轨道Ⅰ
- 是定义在上的偶函数,且在上是增函数,则与的大小关系是____________________.
- She used____on theright in China, so she is not used___on t
- 长方体中共点的三条棱长分别为a、b、c(a<b<c),分别过这三条棱中的一条及其对棱的对角面的面积分别记为S
- 关于古代实行的“重农抑商”政策和“闭关锁国”政策的叙述不正确的是 A.都是封建统治者为维护和加强统治实行的经济政策 B.
- 17.在下面一段文字横线处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过15个字。(5分) 静和
- 下图说明城市经济体制改革后( )①国有企业、集体企业的比重明显下降②城市个体及其他企业成分占有较大比重③由单一公有制经济
- 甲、乙两只普通照明灯泡的铭牌如图所示,下列说法中正确的是( )A.两灯均正常发光时,乙灯消耗的电能较多B.两灯均正
- 已知|a|=10,|b|=12,a与b的夹角θ=120°,且a=(3y-x),b=(y+2x),求x·y.
- 当你乘火车从绵阳到海口参加全国地理知识竞赛,火车经过的地方地球自转线速度总体变化是 A.越来越快 B.越来越慢
- 补写出下列名篇名句中的空缺部分。(只选做3个小题) (1)凤兮!凤兮!何德之衰! ,
- 文言文阅读(22分。其中,选择题12分,每小题3分;翻译题10分) 阅读下面的文言文,完成下面试题。 诸葛孔明 陈亮 孔
- 从结构的角度可以帮助我们更好的理解有机物的化学性质。 (1) 乙炔是一种重要的化工原料,将乙炔通入[Cu(NH3)2]C
- Though small, the ant is as much a creature as al



