第1章 认识化学科学 知识点题库
化学学科的特征是( )
A . 研究物质的变化
B . 制造新物质
C . 认识分子和制造分子
D . 做实验
下列有关叙述正确的是( )
A . 研究质子和中子的结构是化学学科研究的一项新任务
B . 在通风橱进行有毒气体的实验是一种符合“绿色化学”思想的防污染手段
C . 根据能量守恒定律,燃烧一定量的煤和燃烧同量的煤干馏后的焦炭产生的能量一样多
D . 随着化学的发展,化学实验方法并不是化学研究的唯一手段
把少量过氧化钠投入下列溶液中,有白色沉淀生成的是( )
A . 1mol/L氢氧化钠
B . 饱和碳酸氢钠
C . 1mol/L硫酸亚铁
D . 饱和碳酸钠
自来水厂常将氯气通入水中杀菌消毒.
-
(1) 请写出氯气与水反应的化学方程式:.
并据此推断氯水中主要含有的离子是;含有的分子是(均填写化学式).
-
(2) 写出氯气与水反应的产物中发生电离的电离方程式.
;.
-
(3) 写出久置氯水漂白作用会明显减弱的原因的化学方程式:.
-
(4) 向氯水中加入试剂,既能促使氯气与水反应的化学平衡向正反应方向移动又可增加次氯酸的量.
配制250mL 0.1mol•L﹣1的盐酸时,下列实验操作使所配溶液浓度偏大的是( )
A . 用量筒量取所需的浓盐酸时俯视刻度线
B . 定容时仰视刻度线
C . 用量筒量取所需浓盐酸倒入烧杯后,用水洗涤量筒2~3次,洗涤液倒入烧杯中
D . 定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,再补几滴蒸馏水
用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量.若需配制浓度为0.01000mol•L﹣1的K2Cr2O7标准溶液250mL,应准确称取一定质量的K2Cr2O7(保留4位有效数字,已知M(K2Cr2O7)=294.0g•mol﹣1 .
-
(1) 计算配制250mol0.01000mol/L(K2Cr2O7溶液时需要准确计量K2Cr2O7的质量是 g.
-
(2) 配制该标准溶液时,下列仪器中不必要用的有(用编号表示).
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
-
(3) 配制0.01000mol/LK2Cr2O7溶液的操作步骤为(填写空白):计算、称量、、移液、洗涤、、摇匀.
-
(4) 配制0.01000mol/LK2Cr2O7溶液时,下列操作对配制结果有何影响?
①配制过程中未洗涤烧杯和玻璃棒.
②定容时,仰视刻度线.
-
(5) 配制0.01000mol/LK2Cr2O7溶液;定容时不慎加水超过了刻度线,应如何操作?
-
(6) 用0.01000mol/L的K2Cr2O7溶液滴定20.00mL未知浓度的含Fe2+的溶液.恰好完全反应时消耗10.00mL K2Cr2O7溶液,则溶液中Fe2+的物质的量浓度是多少?(已知:6Fe2++Cr2O72﹣+14H+=2Cr3++6Fe3++7H2O)
某同学在实验中需配制250ml 0.1mol/L NaCl溶液,如图为该学生转移溶液的示意图,图中的错误有( )
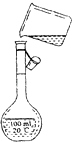
A . 1处
B . 2处
C . 3处
D . 4处
下列叙述正确的是( )
A . 含4NA个离子的固体Na2O2溶于水配成1L溶液,所得溶液中Na+的物质的量浓度为2 mol•L﹣l
B . Na2S在空气中长期放置变浑浊的离子方程式为:2S2﹣+O2+2H2O=2S+4OH﹣
C . 过量的澄清石灰水分别与Na2CO3溶液和NaHCO3溶液反应,现象不同
D . 滴加KSCN显红色的溶液中大量存在:NH4+、K+、Cl﹣、I﹣
相同条件下,下列气体密度最大的是( )
A . 氯气
B . 二氧化硫
C . 氮气
D . 氢气
下列关于Na及其化合物的叙述正确的是( )
A . 将钠投入FeSO4溶液中,可以得到单质铁
B . 足量Cl2、S分别和二份等质量的Na反应,前者得到电子多
C . Na2O与Na2O2中阴阳离子的个数比均为1:2
D . 在2Na2O2+2H2O=4NaOH+O2反应中,每生成1mol O2 , 消耗2mol氧化剂
只用胶头滴管和试管通过两试剂的互滴,不能区别的下列溶液(浓度均为0.1mol/L)( )
A . NaAlO2和稀盐酸
B . NaHCO3和Ca(OH)2
C . NaOH和Al2(SO4)3
D . HCl和Na2CO3
下列物质性质和应用的对应关系正确的是:( )
A . 84消毒液具有碱性,可用作消毒剂和漂白剂
B . 氢氟酸具有酸性,可用于玻璃的腐蚀剂
C . 过氧化钠具有漂白性,可作航空和潜水的供氧剂
D . 活性铁粉具有还原性,在食品袋中可用作除氧剂
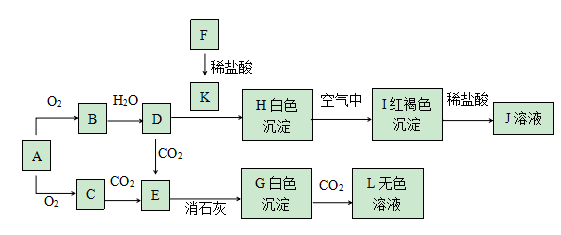
已知A、F为金属单质,C是淡黄色粉末,回答下题。
-
(1) 实验室中A常常保存在中,若将0.1mol C直接转化成D,转移电子数为个。
-
(2) 写出E转化为G的离子反应方程式。
-
(3) 写出D与J混合的离子反应方程式。
-
(4) 用化学方程式表示沉淀H转化成I颜色发生变化的原因:。
-
(5) 直接向K溶液中加入C固体,写出可能出现的现象:。
-
(6) 向盛有L溶液的水槽中加入一小块金属A,下列现象描述不符合实际情况的是。
a.金属A浮在液面,并四处游动
b.金属A会熔化成一个小球
c.反应开始后,溶液由无色变成红色
d.恢复到室温时,烧杯底部有固体物质析出
将6.5
g锌放入足量的稀硫酸中充分反应,得到80 mL密度为1.25 g/mL的溶液。试计算回答:
①所得溶液中硫酸锌的物质的量浓度为,质量分数为。
②生成的气体在标准状况下的体积为。
下列相关实验的叙述中正确的是( )
A . 在胆矾溶液中滴入少许烧碱溶液,再加入有机物加热可验证含醛基类物质
B . 实验室测定硫酸铜晶体中结晶水含量时,需要进行的称量操作一定为4次
C . 为验证氯乙烷中含氯,将其与氢氧化钠溶液混合加热后再滴入硝酸银溶液
D . 需要约480mL0.100mol/L的NaOH溶液,配制时可准确称量NaOH2.000g
下列说法错误的是( )
A . 纯碱广泛应用于小苏打、烧碱和普通玻璃的生产
B . 氧化镁、氧化铝都可用作耐火材料
C . 二氧化硫可用于漂白纸浆以及草帽等编织物
D . 某些硅酸盐具有多孔结构,可用于分离、提纯气体或液体混合物,还可作干燥剂、催化剂
化学与生活密切相关,下列说法正确的是( )
A . 为了防止蛋白质变性,疫苗等生物制剂应冷藏保存
B . 煎炸食物的花生油和牛油都属于饱和高级脂肪酸的甘油酯
C . 铺设在隧道中的钢轨每隔一根轨枕系一块锌片,原理是牺牲阳极的阴极保护法
D . 科学家研制成功的新材料“聚乙烯纺织面料”具有耐高温、吸水性好、快速干燥的特点
合理正确应用化学物质会使生活更加丰富多彩。下列有关物质的性质和用途不对应的是( )
选项 | 物质 | 性质 | 用途 |
A. | ClO2 | 强氧化性 | 自来水消毒剂 |
B. | Fe2O3 | 红色 | 油漆中的红色颜料 |
C. | Na2CO3 | 水解显碱性 | 治疗胃酸的药物成分 |
D. | 钛合金 | 耐高温、耐腐蚀 | 制做发动机的火花塞 |
A . A
B . B
C . C
D . D
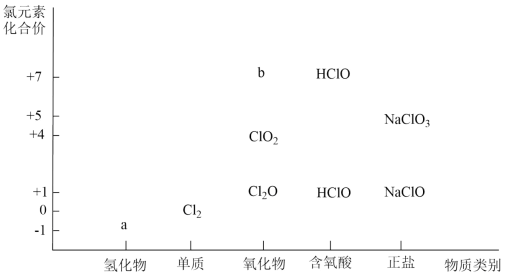
利用如图可从不同角度研究含氯物质的性质及其转化关系。回答下列问题:
-
(1) a物质的化学式为,b属于 (填“酸性”或“碱性”)氧化物。
-
(2) 用ClO2消毒水时,ClO2还可将水中的Fe2+转化为Fe3+ , Fe3+再水解生成Fe(OH)3胶体,说明ClO2具有性,检验有胶体生成的简便方法是。
-
(3) 工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4 , 制备ClO2 , 若生成1molClO2 , 则反应中转移电子的物质的量为。
-
(4) 实验室可用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的化学方程式:。
①浓盐酸在该反应中体现的性质有 (填字母)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.2molCl2 , 需消耗MnO2的质量为 g。
实验室需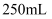
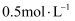 的稀硫酸,现用98%的浓硫酸(
的稀硫酸,现用98%的浓硫酸(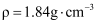 )进行配制。请回答下列问题:
)进行配制。请回答下列问题:
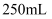
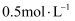 的稀硫酸,现用98%的浓硫酸(
的稀硫酸,现用98%的浓硫酸(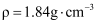 )进行配制。请回答下列问题:
)进行配制。请回答下列问题:
-
(1) 盛浓硫酸的试剂瓶标签上印有下列危险化学品标志中的____(填字母)。A .
 B .
B .  C .
C .  D .
D . 
-
(2) 所需浓硫酸的体积为
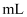 ;如果实验室有
;如果实验室有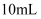 、
、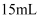 、
、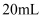 、
、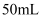 的量筒,应选用
的量筒,应选用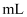 的量筒。
的量筒。
-
(3) 取用任意体积的该稀硫酸,下列物理量中不随所取体积的多少而变化的是____(填字母)。A . 溶液中
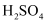 的物质的量
B . 溶液的浓度
C . 溶液中
的物质的量
B . 溶液的浓度
C . 溶液中 的数目
D . 溶液的密度
的数目
D . 溶液的密度
-
(4) 将
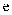 步骤补充完整,配制时正确的操作顺序是(用字母表示)。
步骤补充完整,配制时正确的操作顺序是(用字母表示)。A.用适量蒸馏水洗涤烧杯及玻璃棒2~3次,洗涤液均注入容量瓶
B.用量筒量取所需浓硫酸,沿烧杯内壁缓慢注入盛有少量蒸馏水的烧杯中,用玻璃棒不断搅拌,使其混合均匀
C.将已冷却的稀硫酸沿玻璃棒注入
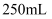 的容量瓶中
的容量瓶中D.将容量瓶盖紧,反复上下颠倒,摇匀
E.继续往容量瓶内小心地加蒸馏水,使液面接近瓶颈上的刻度线1~2cm,。
-
(5) 下列操作造成配制的溶液浓度偏小的是____(填字母)。A . 溶解浓硫酸后未冷却直接转移溶液 B . 容量瓶洗涤后残留少量的蒸馏水 C . 所用过的烧杯、玻璃棒未洗涤 D . 用量筒量取浓硫酸时俯视刻度 E . 用蒸馏水洗净量筒后直接量取浓硫酸配制溶液
-
(6) 若实验过程中加蒸馏水时不慎超过了刻度线,该如何处理?。
最近更新
- 根据有机化合物的命名原则,下列命名正确的是 A. 2-甲基-4-戊炔 B.CH2=C(C2H5)2
- 从同一水平直线上两位置分别沿通方向水平抛出两个小球A和B,其运动轨迹如图所示,不计空气阻力,要使两球在空中相遇,则必须(
- 砂石的比热容为0.92×103J/(kg·℃),它表示质量为 的砂石,温度每升高1℃所吸收的热量为
- .I ordered_________pizza and salad. The pizza was nice but__
- 下图甲为“探究求合力的方法”的实验装置. (1)下列说法中正确的是________. A.在测量同一组数据F1、F2和合
- 在家庭电路中,电热水器正常工作的电压为___▲___V,它与家中的空调器是___▲___ 连接的(串联/并联),家庭中每
- 阅读材料,回答问题。 材料一 2010年新春,浙江W市在经济转型中遭遇了前所未遇的“民工荒”。 许多企业因为招不到足够
- 下列句子中加点词语使用不正确的一项是( ) A“六一”儿童节,孩子们在市民广场上载歌载舞,引得行人驻足观赏。 B
- 珠江三角洲地区发展石化、钢铁、汽车、造船等原材料工业和装备制造业,以推动地区的产业升级,其基地是A.深圳 B.
- 西周实行分封制的目的是( )。 A.拱卫皇室,防止外族侵入 B.巩固国家政权C.
- 已知是锐角三角形,,则( ) A. B. C. D.的大小不能确定
- 下列有关我国国情的叙述错误的是( ) A.自然资源总量丰富,人均资源占有量少 B.人口分布不均,是世界上人口最多的
- 阅读下面的歌词,根据要求作文。(60分) 一天,有个富翁带着小儿子去乡下旅行,想让他见识一下穷人是怎么生活的。在
- 如图6-1-21所示,两个正、负点电荷,在库仑力作用下,它们以两者连线上的某点为圆心做匀速圆周运动.以下说法正确的是(
- 如图表示胰腺细胞合成与分泌酶原颗粒的大体过程,请据图回答有关问题:(1)如果图示细胞是一个胰腺细胞,通常分泌到④部位外的
- 下列各组性质比较中,正确的是() ①酸性:HClO4>HBrO4>HIO4 ②离子还原性:S2﹣>Cl﹣>Br﹣>I﹣
- —Anyway,I’ve decided to accept his suggestion. —_____ your m
- 提出问题 →________→ 收集证据(实验方案设计)→________ →________ →交流评价 → 进行反思
- 已知函数. (1)判断函数的奇偶性和单调性(不要求给出证明); (2)若函数在的值域为,求实数的取值范围
- 假设你是李华,圣诞节你到美国旅游,期间借住在笔友John家,回国后,请给他写一封感谢信,信的要点如下: 1. 表示



