第1章 认识化学科学 知识点题库
用氯化钠固体配置一定质量分数的氯化钠溶液,不需要用的仪器是( )
A . 烧杯
B . 量筒
C . 托盘天平
D . 蒸发皿
对下列事实的解释错误的是( )
A . 氨溶于水的喷泉实验,说明氨气极易溶于水
B . 常温下,浓硝酸可用铝罐来贮存,说明浓硝酸具有强氧化性
C . 向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性
D . 氯气可使湿润的红色布条褪色,而不能使干燥的有色布条褪色,说明次氯酸具有漂白性
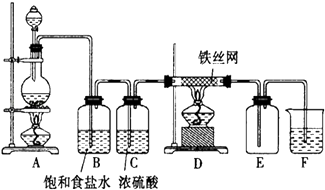
实验室用如图所示装置探究氯气的性质,请回答有关问题:
-
(1) A烧瓶中反应的离子方程式为.
-
(2) 装置B的作用是.
-
(3) 写出D中发生反应的化学方程式:.
-
(4) 装置F中发生反应的化学方程式为.
在给定条件下,下列加点的物质在化学反应中完全消耗的是( )
A . 用50mL 12 mol•L﹣1的氯化氢水溶液与足量二氧化锰共热制取氯气
B . 向100mL 3 mol•L﹣1的硝酸中加入5.6g铁
C . 将1g铝片投入20mL 18.4 mol•L﹣1的硫酸中
D . 常温常压下,0.1mol氯气通入1L水中反应
现用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4来配制500mL、0.2mol•L﹣1的稀H2SO4 . 可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙.请回答下列问题:
-
(1) 上述仪器中,在配制稀H2SO4时用不到的有(填代号).
-
(2) 经计算,需浓H2SO4的体积为mL(保留一位小数).现有①10mL ②50mL ③100mL三种规格的量筒,你选用的量筒是(填代号)
-
(3) 在配制过程中,其他操作都准确,下列操作中:错误的是,能引起实验结果偏低的有(填代号).
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线.
混合气体由N2和CH4组成,测得混合气体在标准状况下的密度是0.821g/L,则混合气体中N2和CH4的体积之比为( )
A . 5∶1
B . 4∶1
C . 1∶4
D . 1∶5
在标准状况下,将1g氦气,11g二氧化碳和4g氧气混合,求该混合气体的体积。
下列说法错误的是( )
A . 能与酸反应生成盐和水的这类物质通常称为碱性氧化物
B . 在人类研究物质的微观结构的过程中,光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器先后得到了使用
C . 汤姆生发现原子中存在电子,从而提出了“葡萄干面包式”原子结构模型
D . 元素周期律是元素原子核外电子排布随元素核电荷数的递增呈现周期性变化的必然结果
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是①向饱和碳酸钠溶液中通入过量的CO2;②向NaAlO2溶液中逐滴加入过量的稀盐酸;③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液;④向硅酸钠溶液中逐滴加入过量的盐酸;⑤向Fe(OH)3胶体中滴入稀盐酸至过量( )
A . ①②
B . ④⑤
C . ①④
D . ①④⑤
对1 mol·L-1的MgCl2溶液的有关叙述中,正确的是( )
A . 该溶液中Cl-浓度为2 mol·L-1
B . 该溶液中Mg2+的物质的量是1 mol
C . 可使用250 mL容量瓶分两次完成490 mL该浓度的MgCl2溶液的配制
D . 该溶液可由95g MgCl2·6H2O固体在水中溶解并稀释至1L获得。
卤素指周期表中倒数第二列的元素,它们的化合物在生活生产中都有很重要的作用.氯化钾是临床常用的电解质平衡调节药,广泛用于临床各科,也常用于无机工业,是制造各种钾盐或碱如氢氧化钾、硫酸钾、硝酸钾、氯酸钾、红矾钾等的基本原料.
-
(1) Ⅰ.老卤中主要含KCl和少量MgCl2、CaCl2、MgSO4等,需要分离提纯得到KCl.现有几种试剂:①盐酸;②K2CO3;③Na2CO3;④NaOH;⑤KOH;⑥Ba(OH)2;⑦BaCl2;⑧Ba(NO3)2 .
为有效除去老卤中的杂质,加入试剂的合理顺序为_________.
A . 先加NaOH,后加Na2CO3 , 再加BaCl2 B . 先加BaCl2 , 后加NaOH,再加Na2CO3 C . 先加K2CO3 , 后加KOH,再加Ba(NO3)2 D . 先加Ba(NO3)2 , 后加K2CO3 , 再加KOH E . 先加Ba(OH)2 , 后加K2CO3 -
(2) 过滤除去沉淀后还需要加入的试剂为 (填序号),还需要进行的实验为.
A.蒸发结晶 B.降温结晶
-
(3) Ⅱ.现有如下图仪器:
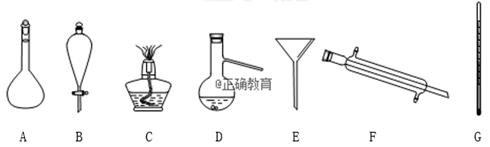
①仪器F的名称是.
②在实验室组成一套蒸馏装置肯定需要所给仪器中的一部分,按照实验仪器由下到上、从左到右的顺序,这些仪器依次是(填字母).
-
(4) Ⅲ.小明同学将16.0 g NaOH固体溶于水配成100 mL溶液,其密度为1.60 g/mL,小明计划用配好的NaOH溶液制取简易消毒液。回答下列问题:
①用量筒取小明同学所配的NaOH溶液 mL才能与标准状况下2.24 L氯气恰好完全反应.
②该消毒液即市面上的“84消毒液”,小明将(2)所取体积的NaOH溶液吸收好氯气后的溶液稀释到5 L使用,稀释后溶液中c(Na+)=
③“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员需要520 mL 2.3 mol/L的稀硫酸,拟采用98%(密度为1.84 g/cm3)的浓硫酸进行配制.
①需取用的浓硫酸的体积为mL.
②取上述配好的硫酸溶液50 g与50 g 水混合,所得溶液的物质的量浓度
A.等于1.15 mol/L B.小于2.30 mol/L 大于1.15 mol/L
C.小于1.15 mol/L D.大于2.30 mol/L
下列说法正确的是( )
A . 1mol氧气的质量是16g,它所占的体积是22.4L
B . H2O的摩尔质量为18g
C . 1mol任何物质都含有约6.02×1023个分子
D . 标准状况下,以任意比例混合的H2和CO2混合物22.4L,含有的分子数为NA
下列关于Na2CO3、NaHCO3的说法正确的是( )
A . 受热时Na2CO3较NaHCO3更不稳定,更易分解产生CO2
B . 等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多
C . CaCl2溶液无法鉴别Na2CO3溶液和NaHCO3溶液
D . 等物质的量的两种盐与足量盐酸完全反应,Na2CO3所消耗HCl的物质的量是NaHCO3的两倍
下列说法错误的是( )
A . 煤的干馏属于化学变化
B . 实验室金属钠应保存在煤油中
C . 晶体硅的导电性介于导体和绝缘体之间
D . 糖类、油脂、蛋白质都是高分子化合物
图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
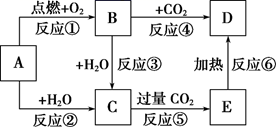
-
(1) 写出A的原子结构示意图,B的化学式。
-
(2) 以上6个反应中属于氧化还原反应的有(填写编号)。
-
(3) 写出B→D反应的化学方程式,C溶液→E反应的离子方程式。
-
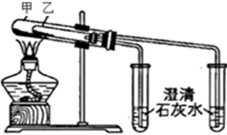
(4) 若用所示装置验证D和E的稳定性,则试管乙中装入的固体最好是(填化学式)。
-
(5) 将一定量的B投入到含有下列离子的溶液中:
 、
、  、
、 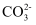 、Na+ , 反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)填离子符号)。
、Na+ , 反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)填离子符号)。
下列装置应用于实验室制取氯气并回收氯化锰溶液,不能达到实验目的的是( )
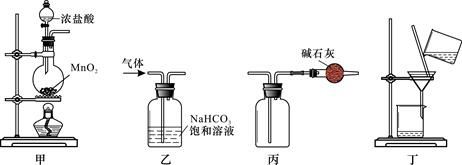
A . 用装置甲制取氯气
B . 用装置乙除去氯气中的少量氯化氢
C . 用装置丙收集氯气并防止污染空气
D . 用装置丁分离二氧化锰和氯化锰溶液
按要求回答下列问题:
-
(1) 写出
 的电子式;
的电子式;
-
(2) 用电子式表示
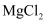 的形成过程;
的形成过程;
-
(3) 写出
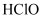 的结构式,它的空间构型为;
的结构式,它的空间构型为;
-
(4) 写出铜和浓硫酸反应的化学方程式;
-
(5) 写出实验室用
 代替
代替  制氯气的离子方程式。
制氯气的离子方程式。
配制400mL0.100mol/L的KCl溶液,下列说法正确的是( )
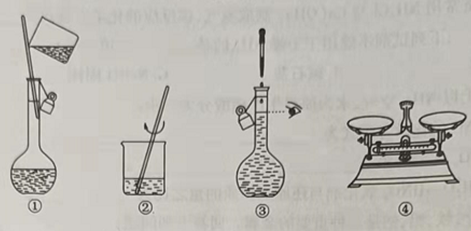
A . 上述实验操作步骤的符合题意顺序为:④①②③
B . 容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
C . 实验中需称量2.98 g KCl固体
D . 定容时,若仰视容量瓶的刻度线,使配得的KCl溶液浓度偏低
下列我国古代的技术应用中,其不涉及化学反应的是( )
A.火药使用 | B.粮食酿酒 | C.活字印刷 | D.湿法炼铜 |
|
|
|
|
A . A
B . B
C . C
D . D
“84消毒液”稀释一定比例后能有效杀灭新冠病毒。某同学购买了一瓶某牌的“84消毒液”,查阅相关资料和消毒液包装说明得到如下信息:
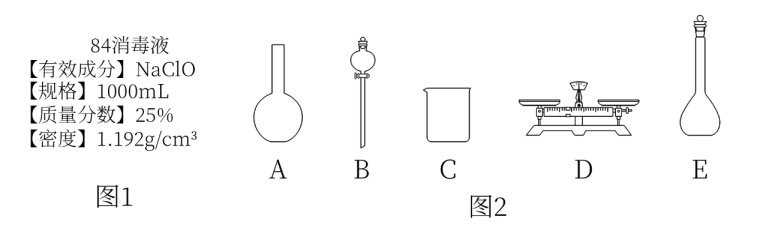
-
(1) 该“84消毒液”中NaClO的物质的量浓度为mol·L−1。
-
(2) 该同学欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。
①如图2所示的仪器中,配制此溶液不需要使用的是(填仪器序号),还缺少的是 (填仪器名称)。
②该同学配制上述溶液时需称量的NaClO固体的质量为g。
-
(3) 若实验遇下列情况,导致所配溶液的物质的量浓度偏低是____(填序号)。A . 容量瓶在使用前未干燥,里面有少量蒸馏水 B . 定容时仰视刻度线读数 C . 定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 D . 未冷至室温就转移定容
最近更新
- 估算的值是在( ) A、和之间 B、和之间 C、和之间 D、和之间
- 植物从土壤中吸收的N可用来合成下列哪种物质( ) A.脱氧核糖 B.葡萄糖 C.磷脂
- —Would you like some salad?—No, _____ A.I'm not.
- 已知25℃、时: ; ; 下列说法正确的是( ) A.比稳定,由转化为是吸热反应 B.比稳定,由转化为是放热反应
- 下列说法正确的是 A.做焰色反应实验时,火焰的颜色呈黄色,说明有钠元素存在 B.欲除去Cl2中混有的HCl,最好
- (06年上海卷)(5 分)1919 年卢瑟福通过如图所示的实验装置,第一次完成了原子核的人工转变,并由此发现
- 写出四种化合物,它们完全燃烧产生 CO2 和 H2O(g) 的体积比均为1∶1(在同温同压下测得),且能被新制 Cu(O
- 已知氘核质量为2.013 6 u,中子质量为1.008 7 u,的质量为3.015 0 u. (1)写出两个氘核聚变成的
- He imagines that people don’t like him, _____ they do. A
- 《钱塘湖春行》中用植物写早春的句子是
- 有关卵子的发生叙述不正确的是( ) A.卵原细胞通过有丝分裂的方式增加数量 B.初级卵母细胞在胎儿期形成 C.减数
- No matter how hard it is, don’t . Things will
- 下列各对物质中,互为同系物的是
- 如果支配左腿的传入神经及中枢完整,而传出神经受损,那么该左腿会 A.能运动,针刺有感觉
- (3分)当车辆发生剧烈碰撞,安全气囊会在瞬间弹出,防止驾驶员受伤。撞车时,约在0.01 s内引发下列反应:2NaN3 2
- 在制备蛇毒抗毒素血清时,需将灭毒的蛇毒液注入家兔体内引起免疫反应,参与这一免疫反应的细胞有( ) A.吞噬细胞、效应
- 学习科学知识,提高自护能力。以下事件处理正确的是( )
- 构建社会主义和谐社会是我们党提出的重大战略任务,而解决民生问题是构建和谐社会的着力点。为贯彻党中央精神,国务院制定了一系
- 读下图,同答下列问题:(每空1分,共10分)(1)A处地形名称是____ ____,这里目前面临的最突出的环境问
- 某阻值为10欧的定值电阻连在一节新干电池两端,则它两端的电压为 (7) 伏,,通过它的电流是 (8) 安;若把它