第1章 认识化学科学 知识点题库
设NA为阿伏加德罗常数。如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下雪时,常用融雪剂清理路面,醋酸钾(CH3COOK)是效果较好的融雪剂.下列关于1molCH3COOK的叙述正确的是( )
A . 1 mol CH3COOK含有1 mol钾元素
B . CH3COOK的摩尔质量为98 g
C . 1molCH3COOK含有2 mol氧
D . 1molCH3COOK含有3×6.02×1023个H
下列陈述Ⅰ、Ⅱ正确且有因果关系的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Cl2有漂白作用 | Cl2能使湿润的有色布条褪色 |
B | SiO2有导电性 | SiO2可用于制备光导纤维 |
C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
D | 浓氨汽化时要吸收大量的热 | 浓氨可用作制冷剂 |
A . A
B . B
C . C
D . D
配制一定物质的量浓度溶液时,会导致所配溶液浓度偏大的操作是( )
A . 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中
B . 用量筒量取浓硫酸时,俯视刻度线
C . 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理
D . 定容时俯视刻度线
饱和氯水长期放置后,下列微粒在溶液中不减少的是( )
A . HClO
B . Cl﹣
C . Cl2
D . ClO﹣
完成下列填空
-
(1) 决定物质体积的因素有①构成物质的粒子数;②粒子大小;③粒子间的距离.对固体、液体物质而言,它主要是由上述决定(填写编号,下同);对气体物质而言,它主要由上述决定.上述三种因素中,与外界条件有关的是.
-
(2) 配制100mL2mol•L﹣1的 H2SO4溶液,需要某98%H2SO4溶液(密度为1.8g/cm﹣3)的体积为﹣﹣﹣﹣mL;需要的仪器有量筒、玻璃棒、胶头滴管、烧杯和;若配制溶液时,玻璃棒和烧杯未洗干净,则所配溶液的浓度;取配制后的溶液10mL,加入足量的锌,则生成标况下氢气的体积为 L.
某课外实验小组设计的如图实验合理的是( )
A . 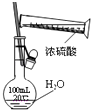 配制一定浓度硫酸溶液
B .
配制一定浓度硫酸溶液
B . 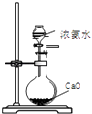 制备少量氨气
C .
制备少量氨气
C . 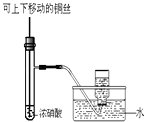 制备并收集少量NO2气体
D .
制备并收集少量NO2气体
D . 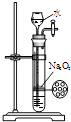 制备少量氧气
制备少量氧气
 配制一定浓度硫酸溶液
B .
配制一定浓度硫酸溶液
B .  制备少量氨气
C .
制备少量氨气
C .  制备并收集少量NO2气体
D .
制备并收集少量NO2气体
D . 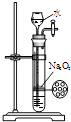 制备少量氧气
制备少量氧气
将过量的二氧化碳分别通入:①CaCl2溶液 ②Na2SiO3溶液 ③饱和Na2CO3溶液④Ca(ClO)2 溶液 ⑤澄清的石灰水.最终溶液中有白色沉淀析出的是( )
A . ②③⑤
B . ②④
C . ①②④⑤
D . ②③
下列有关氧气的摩尔质量表示正确的是( )
A . 32
B . 32 g
C . 32 mol
D . 32 g/mol
下列化合物中不可能通过化合反应制得的是( )①Fe(OH)3②FeCl2③FeI3④SO3⑤CuS⑥NaHCO3
A . ③⑤⑥
B . ③④⑤⑥
C . ③⑤
D . ②③⑤
下列关于钠的说法中,正确的是( )
A . 金属钠的熔点很高
B . 钠是一种银白色金属,硬度很大
C . 钠着火时,可用沙土灭火
D . 豆粒大的钠投入硫酸铜溶液中,生成铜和硫酸钠
常见的含钠元素的物质A,B,C,D,存在如图转化关系(部分生成物和反应条件已略去)。
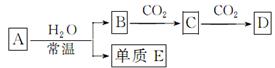
-
(1) 若A为金属钠,则E为,A与水反应的离子方程式为。
-
(2) 若A为过氧化钠,则E为,A与水反应的化学方程式为。
-
(3) A不论是Na还是Na2O2 , 依据转化关系判断物质物质D是。
-
(4) 向B(NaOH)溶液中通入CO2 , CO2的量不同时,所得的产物相同吗?(填“相同”或“不相同”),试分别写出足量CO2和少量CO2时反应的离子方程式:
。
-
(5) 如何通过实验的方法鉴别同浓度的C、D溶液?
。
中国沿海某城市采用反渗透法将海水淡化,得到淡水供市民使用,剩余母液继续加工获得其他产品。母液中主要含有Cl-、Na+、K+、Mg2+
、Ca2+、SO42-、Br-等离子。某实验小组同学模拟工业生产流程,进行如下实验.
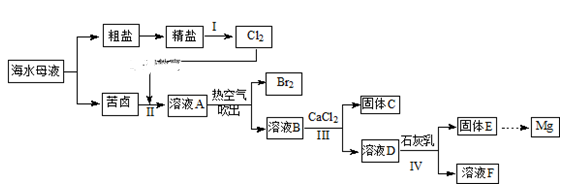
-
(1) 写出实验室制备氯气的化学方程式;
-
(2) 海水淡化的方法还有(写出一种);
-
(3) I中,电解饱和食盐水的工业生产叫做氯碱工业,写出该反应的离子方程式;
-
(4) Cl2和Br2均为双原子分子,从原子结构的角度解释其原因;
-
(5) Ⅲ中,加入适量CaCl2固体的目的是;
-
(6) 写出IV中反应的离子方程式;
-
(7) 与过程II类似,工业上常用“空气吹出法”实现海水提溴,将1m3海水浓缩至1L,使用该法最终得到36g Br2 , 若提取率为60%,则原海水中溴的浓度为 mg/L。
配制100mL1.0mol·L-1的NaOH溶液,下列情况不会影响溶液浓度的是( )
A . 容量瓶使用前有蒸馏水
B . 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C . 俯视确定凹液面与刻度线相切
D . 称量NaOH固体时使用了称量纸
氯气是一种重要的化工原料,它的发现和研究经历了以下几个阶段。
-
(1) 1774 年,舍勒在研究软锰矿(主要成分是二氧化锰)时,将软锰矿与浓盐酸混合并加热,无意间制得了氯气,此反应中氯元素被(填“氧化”或“还原”)
-
(2) 贝托莱发现,氯气能溶于水,向此溶液中滴加紫色石蕊溶液,观察到的现象是。
-
(3) 泰纳将氯气通入石灰水,并一步步改进,制得了我们现在常用的漂白粉,漂白粉的有效成分是。
-
(4) 盖吕萨克发现氯气能与金属反应。氯气与铝反应的化学方程式是。
-
(5) 1810 年,戴维经过大量实验研究,确认氯气是一种单质,且有毒。实验室吸收氯气的常用方法是(用化学方程式表示)
下列符合实际并用于工业生产的是( )
A . 工业炼铝:电解熔融的氯化铝
B . 制取漂粉精:将氯气通入澄清石灰水
C . 工业制硫酸:用硫磺为原料,经燃烧、催化氧化、最后用98.3%浓硫酸吸收
D . 工业制烧碱:电解饱和食盐水,在阳极区域得到烧碱溶液
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 将4.6g 钠用铝箔包裹并刺小孔,与足量水充分反应生成H2分子数为0.1 NA
B . 标准状况下,22.4L 己烷中含有的共价键的数目为19NA
C . 标准状况下,11.2L 12C18O中含有的中子数为8NA
D . 标准状况下,7.1 gCl2通入足量石灰水中反应转移的电子数为0.2NA
如图所示物质之间的转化,已知:A是金属单质,且焰色试验为黄色,Y是非金属单质,且呈黄绿色,X为常见温室气体。按要求回答下列问题:
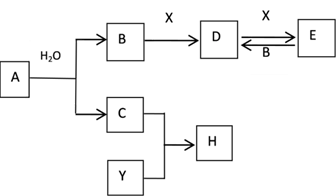
-
(1) E的化学式:;E常用来治疗胃酸过多,写出此反应的离子方程式:;
-
(2) 写出A→B的离子方程式,并用双线桥法标出电子转移的方向和数目:。
-
(3) C在Y中燃烧的实验现象:。
在给定条件下,下列选项所示的物质间转化不能一步实现的是( )
A .  B .
B . 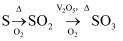 C .
C .  D .
D . 
 B .
B . 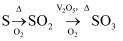 C .
C .  D .
D . 
自来水厂可用氯气对自来水杀菌、消毒,在自来水出厂前,自来水厂的水质检验员利用化学分析仪器等对水中的一些物质(如 )进行检测,并进行数据分析。
)进行检测,并进行数据分析。
 )进行检测,并进行数据分析。
)进行检测,并进行数据分析。
-
(1) 氯气的命名由来如图所示,在第一次世界大战中,氯气被用来制作毒气弹,使受害者的身体遭受严重损伤。由此可知Cl2为气体。
资料卡片
氯气的命名
1810年,英国化学家戴维以大量事实为依据,确认黄绿色气体是一种新元素组成的单质,并将这种元素命名为chlorine。这一名称来自希腊文,有“绿色”的意思。中文译名曾为“绿气”,后改为“氯气”。
-
(2) 某化学兴趣小组设计实验制备Cl2。
①利用KMnO4与浓盐酸制备氯气,则应选择装置(填标号),发生反应的离子方程式为。
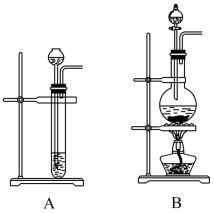
②①中制得的Cl2中含有少量的HCl,原因是,通常用(填试剂名称)除去Cl2中的HCl。
-
(3) 将上述制得的Cl2通入水中可得到新制氯水,该过程可选用装置(填标号),其中NaOH溶液的作用是。
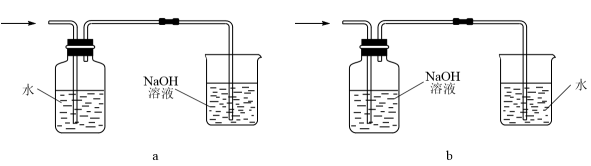
-
(4) 若将氯气通入紫色石蕊溶液中,现象为。
最近更新
- 关于硝酸的说法正确的是 A.硝酸与金属反应时,主要是+5价的氮得电子 B.浓HNO3与浓HCl按3∶1的体积比所得的
- 从日本大化改新的措施可以看出, 中国哪一时期文化对它影响很大: A、秦汉时期 B、三国时期
- 他在位时发展科举、开凿运河,造福后世。他好大喜功、不惜民力,结果落了个万世唾骂的恶名。这里说的“他”是( ) A.秦
- 将10 g质量分数为20%的氢氧化钠溶液与10 g质量分数为20%的盐酸混合,充分反应后滴入紫色石蕊溶液,溶液变为
- 用斐林试剂鉴定还原糖的实验中,教材要求必须将斐林试剂甲液和乙液混合均匀后使用,切勿分别使用,但在实验过程中,实验者设想按
- 阅读下面一首唐诗,完成后面的二题。白云泉 白居易 天平山上白云泉,云自无心水自闲。 何必奔冲山下去,更添波浪向人间! (
- 如图13所示,一个质量为m、电荷量为+q的小球以初速度v0水平抛出,在小球经过的竖直平面内,存在着若干个如图所示的无电场
- 给下面加点字注音,并根据拼音在横线上填写汉字。(2分) (1)阔绰( ) (2
- 阅读下面的文言文,完成下题。 陈矩,安肃人。万历中为司礼监秉笔太监,二十六年提督东厂。为人平恕,识大体。尝奉诏收
- 的倒数是 A.2 B. C. D.
- 若(a+2b)2=(a-2b)2+M,则M= .
- 阅读下面一份请柬,指出用语不得体的毛病并修改。 请柬 ×××老师: 您好! 我校定于10月20日下午3时在校图书馆报告厅
- 下列各项中,标点符号的使用合乎规范的一项是 A.姚明在整个NBA赛季中都会因为这样那样的原因成为关注的目标。这到底是什么
- 为大力弘扬伟大抗震救灾精神,激励广大干部群众奋力推进改革开放和社会主义现代化建设事业,不断夺取全面建设小康社会新胜利,党
- 在6张完全相同的卡片上分别画上线段、等边三角形、平行四边形、直角梯形、正方形和圆,在看不见图形的情况下随机摸出1张,这张
- 超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料经研磨烧结可合成 一种高温超导物质Y2Ba4Cu
- 在采矿时,要大量剥离表土,处理不当往往会造成水土流失,破坏土地资源,这主要说明了( ) A.自然资源具有分布的规律性
- 在一个布口袋里装有红色、黑色、蓝色和白色的小球各1个,如果闭上眼睛随机地从布袋中取出一个球,记下颜色,放回布袋搅匀,再闭
- 判断下列函数的奇偶性: (1)f(x)=+x2,x∈(-1,0)∪(0,1]; (2)f(x)=.
- 中、美、日、法、英等6国科学家联合公布人类基因组图谱及初步分析结果,标志着生命科学又向深层迈进一步。人们担心转基因产品对



