第1章 认识化学科学 知识点题库
下列关于定量实验中的基本操作和仪器的描述正确的是( )
A . 用托盘天平称取20.00 g NaOH固体
B . 用碱式滴定管准确量取20.00 mL K2Cr2O7溶液
C . 用电子(分析)天平测得铁片质量是15.524 g
D . 在配制一定物质的量浓度的溶液时,定容后,经摇匀发现液面低于刻度线,此时再加入蒸馏水使其液面与刻度线持平
下面有关氯气的叙述正确的是( )
A . 氯气可使湿润的红布条退色,所以氯气具有漂白性
B . 在通常情况下,氯气可以和任何金属直接化合
C . 氯气没有漂白性,但通入品红溶液中,品红会退色
D . 氯气是黄绿色气体,闻其气味时要小心将集气瓶放在鼻孔下直接闻
下列实验方案可行的是( )
A . 用浓硫酸干燥氨气
B . 用酚酞试液检验酸性溶液
C . 通入Cl2除去FeCl3溶液中的FeCl2
D . 加入Fe粉除去Al3+溶液中的杂质Cu2+
某化学兴趣小组利用以下各装置连接成一整套装置,探究氯气与氨气之间的反应.其中D为纯净干燥的氯气与纯净干燥氨气反应的装置.
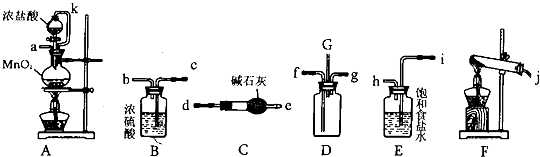
请回答下列问题:
-
(1) 整套装置从左向右的连接顺序是(j)接、接(f)、(g)接、
接、接(a).
-
(2) 连接好装置后,必需进行的一步实验操作是
-
(3) 装置E的作用是,橡胶管k的作用是
-
(4) 从装置D的G处逸出的尾气中可能含有黄绿色的有毒气体,处理方法
是
-
(5) 装置F中试管内发生反应的化学方程式
-
(6) 接入D装置的两根导管左边较长、右边较短,目的是.
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是:( )
A . 甲的分子数比乙的分子数多
B . 甲的摩尔体积比乙的摩尔体积小
C . 甲的物质的量比乙的物质的量少
D . 甲的相对分子质量比乙的相对分子质量小
实验室常用盐酸的质量分数为36.5%,密度为1.20g/cm3。
-
(1) 此浓盐酸的物质的量浓度是多少?(列式计算)
-
(2) 配制100mL3.00mol/L的盐酸,需以上浓盐酸多少mL?(列式计算)
-
(3) 用浓盐酸配制该稀盐酸需要以下哪些步骤(按操作顺序填写序号)
①计算②装瓶③用50mL量筒量取一定体积的浓盐酸④洗涤⑤移液⑥稀释⑦定容⑧摇匀
将一小块钠投入到NH4Cl溶液中,产生的气体是( )
A . 只有H2
B . 只有NH3
C . H2和NH3
D . O2和H2
下列说法不正确的是( )
A . 化学家鲍林提岀了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础
B . 屠呦呦参照古文记载“青蒿一握,以水二升渍,绞取汁”,对青蒿素进行提取,该过程属于化学变化
C . 门捷列夫根据元素的性质随着相对原子质量递増呈现周期性变化规律,制岀了第一张元素周期表
D . 道尔顿的“原子论”和阿伏加德罗的“分子学说”对化学的发展都起到了极大推动作用
已知阿伏加德罗常数为NA , 某原子的相对原子质量为M、实际质量为m0 , 一个12C原子的实际质量为m1 , 则该原子的摩尔质量是( )
A . m0NA
B . M
C . ( 12m0/m1) g/mol
D . M/NA
下列有关化学用语表示正确的是( )
A . 中子数为10的氧原子:  B . 氯原子的结构示意图:
B . 氯原子的结构示意图: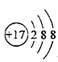 C . 硝酸钡的化学式:BaNO3
D . 水的摩尔质量为18g
C . 硝酸钡的化学式:BaNO3
D . 水的摩尔质量为18g
 B . 氯原子的结构示意图:
B . 氯原子的结构示意图: C . 硝酸钡的化学式:BaNO3
D . 水的摩尔质量为18g
C . 硝酸钡的化学式:BaNO3
D . 水的摩尔质量为18g
某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
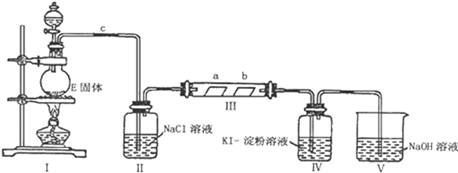
-
(1) 实验室以二氧化锰和浓盐酸制备氯气的离子方程式是。
-
(2) 装置Ⅱ的作用是。
-
(3) 实验过程中,装置IV中的实验现象为;发生反应的化学方程式为。
-
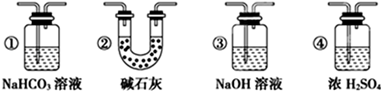
(4) 实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的装置(填序号),该装置的作用是。
-
(5) 装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式。
NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,11.2LCl2溶于水,溶液中Cl2、Cl-、ClO-和HClO的微粒数之和为NA
B . MnO2与足量浓盐酸反应产生22.4 LCl2时转移电子效为2NA
C . 100mL18mol·L-1浓硫酸与足量Cu粉加热反应,产生SO2分子数为0.9NA
D . 常温常压下,9.5g羟基(-18OH)含有的中子数为5.5NA
下图是某同学用250 mL容量瓶配制0.20 mol·L-1 NaOH溶液的过程:
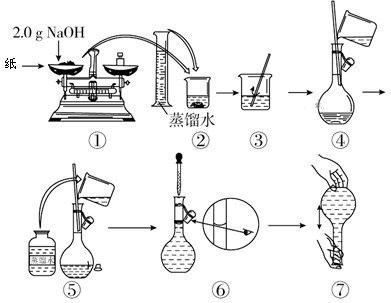
该同学的错误步骤有( )
A . 1处
B . 2处
C . 3处
D . 4处
某同学通过以下装置测定M样品(只含Fe、Al、Cu)中各成分的质量分数。取两份质量均为m g的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为V1 mL和V2 mL(已折算到标准状况下)。
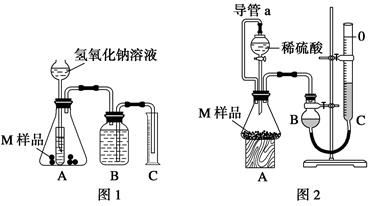
-
(1) 写出实验1中可能发生反应的离子方程式:。
-
(2) 该实验需要0.50 mol·L-1的NaOH溶液480 mL,请回答下列问题:
①配制时应用托盘天平称量g NaOH,应选择 ml容量瓶。
②配制NaOH溶液时,NaOH固体中含有Na2O杂质会导致所配溶液浓度。(填“偏大”、“偏小”或“无影响”)。
-
(3) 该实验中所用稀硫酸是用98%的浓硫酸(ρ=1.84g/cm3)配制的,则该浓硫酸的物质的量浓度是。
-
(4) 对于实验2,读数时冷却至室温除视线平视外,还应进行的操作是: 。
-
(5) 实验2中导管a的作用。
-
(6) M样品中铜的质量的数学表达式为(用V1和V2 表示):。
向盛有紫色石蕊溶液的试管中持续通入氯气至过量,溶液颜色可能出现无色、浅黄绿色、红色等变化。
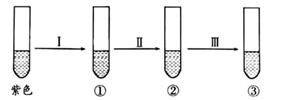
下列叙述正确的是( )
A . 过程Ⅰ溶液由紫色变成红色,起作用的微粒是H+
B . 过程Ⅱ溶液由红色变成无色,证明试管②溶液不再呈酸性
C . 过程Ⅲ溶液颜色由无色变成浅黄绿色,证明溶液中有Cl2
D . 若向紫色石蕊试液中持续加入Na2O2粉末,也会出现相同的颜色变化
常温常压下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1NaOH溶液,整个过程溶液中H+的浓度变化如图所示。(已知常温常压下Cl2溶于水时,只有部分Cl2会与水发生反应),下列叙述中正确的是( )
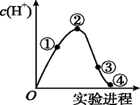
A . ②处溶液的酸性比①处溶液的酸性弱
B . 依据②处c(H+)可计算溶解的Cl2的物质的量
C . 整个实验过程中,溶液的颜色先变深后变浅,最后变为无色
D . ④处表示Cl2与NaOH溶液恰好完全反应,共转移了0.1mol电子
有关一定物质的量浓度的溶液的配制,下列说法正确的是( )
A . 容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液
B . 配制一定物质的量浓度的稀盐酸时,用量筒量取9.82mL浓盐酸
C . 配制 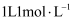 的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D . 定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁
的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D . 定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁
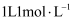 的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D . 定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁
的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D . 定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁
对于金属钠与无水乙醇的反应,下列说法错误的是( )
A . 有气泡产生
B . 比水与钠反应缓慢
C . 发生加成反应
D . 乙醇的氢氧键发生断裂
化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( )
A . 以食盐、氨、二氧化碳为原料制取碳酸钠
B . 以软锰矿、浓盐酸为原料制取氯气
C . 用  溶液刻蚀铜制印刷电路板
D . 从海水中提取粗盐
溶液刻蚀铜制印刷电路板
D . 从海水中提取粗盐
 溶液刻蚀铜制印刷电路板
D . 从海水中提取粗盐
溶液刻蚀铜制印刷电路板
D . 从海水中提取粗盐
宋应星著作的《天工开物》被称为中国十七世纪生产工艺百科全书,它翔实记述了明代居于世界先进水平的科技成就.下列说法错误的是( )
选项 | 记载内容 | 涉及化学操作或物质分类 |
A | 作咸卷海水盐篇记载:“火燃釜底,滚沸延及成盐” | 采用蒸发结晶的方法获取食盐 |
B | 甘嗜卷造糖篇记载:“每汁一石,下石灰( | 用石灰中和甘蔗汁中的酸性物质 |
C | 治铸卷·钟篇记载:“内模干燥后,用牛油加黄蜡涂附在上面约有几寸厚” | 牛油为天然高分子化合物 |
D | 五金卷·铜篇记载:“以炉甘石或倭铅参和,转色为黄铜:以砒霜等药制炼为白铜:矾、硝等药制炼为青铜” | 黄铜、白铜和青铜均为铜合金 |
A . A
B . B
C . C
D . D
最近更新
- 短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子最外层电子数是内层的2倍,Z是地壳中含量最高的元素,W是同周期
- 图l为“用DIS研究物体的加速度与力的关系”的实验装置图,A为带有位移传感器发射器的小车,B为若干规格相同的回形针。实验
- 如图是一种衣藻细胞的结构示意图。①为鞭毛,②为红色的眼点,衣藻能够依靠眼点的感光和鞭毛的摆动,游到光照和其他条件都适宜的
- 英语单词“china”的意思是“瓷器”,当第一个字母大写即写成“China”时,意思就是指中国,中国有名的瓷都景德镇,著
- 阅读下面的文字,根据要求写一篇不少于800字的文章。 有一个晚上,古希腊哲学家泰勒斯见星空晴朗,便在草地上观察星星。他仰
- 山东省龙口市90%以上的人大代表向选民述职,人民群众对人大代表的监督由评议转变为对其履职情况进行量化考核,群众形象地把这
- 2014年3月22日是第二十二个“世界水日”,它的主题是“水与能源”.关于水的知识有下列话题,请按要求填空: (1)自来
- 对生物进行分类的主要目的不包括 A.了解生物的多样性 B.了解生物之间的亲缘关
- The filmGoodbye Mr Loser(《夏洛特烦恼》)has neither a team ofshinin
- 青藏高原是全球海拔最高的独特地域单元。它的隆起是近数百万年来地球史上重大的事件之一。中国科学家在隆起过程与环境变迁等方面
- 某中学数学兴趣小组12名成员的年龄悄况如下: 年龄(岁) 12 13 14 15 16 人数 1 4 3 2 2则这个小
- 温家宝总理在十一届全国人大三次会议上作《政府工作报告》时指出,要促进哲学社会科学发展。之所以要这样做,是因为 () ①真
- (4分)解方程:.
- 下列关于生物工程中酶的作用不正确的是 ( ) A.纤维素酶可用于
- 下列有机物水解时,键断裂处不正确的是() A.①② B.②④
- 下列化学用语正确的是()A. 氟化氢的电子式: B. 氯原子的结构示意图: C. 氯化钠的电离方程式:NaCl=Na++
- 2012年11月23日,国产歼-15舰载机首次在航空母舰—“辽宁号”上成功起降,如图3,一举突破了阻拦着舰等飞行关键技术
- 以淀粉为基本原料可制备许多物质,如: 下列有关说法中正确的是() A. 淀粉是糖类物质,有甜味,与纤维素互为同分异构体
- Don't worry.It's nothing serious at all and you _________ ta
- Every day the teacher gives us a one-minute in Engli
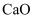 )五合于中”
)五合于中”


