第1章 认识化学科学 知识点题库
(1)现需要配制500mL 1mol/L硫酸溶液,需用质量分数为98%、密度为1.84g/cm3的浓硫酸 mL。
(2)从上述仪器中,按实验使用仪器的先后顺序.其编号排列是 。
(3)若实验遇到下列情况,所配硫酸溶液的物质的量浓度偏小的有 (填序号)。
①用以稀释硫酸的烧杯未洗涤;
②未经冷却趁热将溶液注入容量瓶中;
③摇匀后发现液面低于刻度线再加水;
④容量瓶中原有少量蒸馏水;
⑤定容时仰视观察液面。
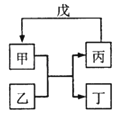
下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)
甲 | 乙 | 丙 | 戊 | |
A | NH3 | Cl2 | N2 | H2 |
B | C | SiO2 | CO | CuO |
C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | CO2 |
D | 乙醇乙酯 | NaOH溶液 | 乙醇 | 乙酸 |
( )
A.摩尔是国际单位制中七个基本物理量之一
B.固体氯化钠不能导电,但氯化钠是电解质
C.6.02×1023个12C原子数就是阿伏加德罗常数
D.1mol一氧化碳的质量为28g/mol
E.Na2CO3和NaHCO3的电离方程式分别是Na2CO3═2Na++CO32﹣、NaHCO3═Na++H++CO32﹣
F.金刚石不能导电,所以金刚石是非电解质
G.氧化物只能分为酸性、碱性、两性三类
H.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA .
可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙.
-
(1) 上述仪器中,在配制稀H2SO4时用不到的有 (填代号).
-
(2) 所用浓H2SO4的物质的量浓度为,配制时所需浓硫酸的体积为 mL.(计算结果数据保留到小数点后一位)
-
(3) 溶液配制操作步骤如下:
①用量筒量取所需的浓硫酸,小心倒入250mL烧杯中.
②向250mL烧杯倾倒约100mL蒸馏水.
③用蒸馏水洗涤烧杯及玻璃棒2~3次,将洗涤液注入容量瓶中.
④用玻璃棒慢慢搅动,待溶液冷却至室温,沿玻璃棒注入500mL的容量瓶中.
⑤将容量瓶盖紧,振荡,摇匀.
⑥向容量瓶中小心加蒸馏水至液面接近刻度1~2cm处,改用胶头滴管滴加蒸馏水,使溶液凹液面最低点恰好与刻度线相切.操作步骤顺序正确为(填代号)
-
(4) 由于操作不慎,进行⑥时,使液面略超过了容量瓶的刻度(标线),这时应采取的措施是A . 再加浓硫酸 B . 吸出标线以上的溶液 C . 影响不大,不再处理 D . 重新配制
-
(5) 容量瓶是专门用来配制一定体积一定浓度的溶液的仪器,以下有关容量瓶的叙述正确的有A . 容量瓶上标有压强、温度、刻线 B . 容量瓶不能长时间贮存试剂 C . 为使实验更准确,容量瓶洗净后最好用欲配制的溶液润洗 D . 用容量瓶配制溶液,容量瓶必须是干燥的
-
(6) 下列操作会使所配溶液的浓度偏高的是 .A . 浓硫酸稀释后未冷至室温即进行定容 B . 容量瓶未干燥即用来配制溶液 C . 往容量瓶中转移溶液时,有少量液体溅出 D . 摇匀后发现液面低于刻度线,没采取任何措施 E . 用量筒取浓硫酸时俯视刻度线 F . 定容时,俯视刻度线.
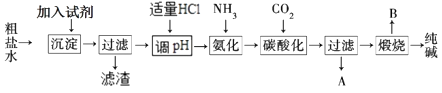
I.工业生产纯碱的工艺流程示意图如下:
-
(1) 为除去粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入试剂顺序合理的是________。A . 碳酸钠、氢氧化钠、氯化钡 B . 碳酸钠、氯化钡、氢氧化钠 C . 氢氧化钠、碳酸钠、氯化钡 D . 氯化钡、氢氧化钠、碳酸钠
-
(2) 工业生产纯碱工艺流程中,碳酸化时产生的现象是。
-
(3) 碳酸化后过滤,滤液A最主要的成分是(填写化学式),检验这一成分的阴离子的具体方法是:。
-
(4) 煅烧制取Na2CO3在(填字母序号)中进行。
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.氧化铝坩埚
-
(5) II.纯碱在生产生活中有广泛的用途。
工业上,可能用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为。
-
(6) 纯碱可制备重铬酸钠(Na2Cr2O7),铬铁矿中的1molCr2O3反应时需要通入标准状况下O2的体积为。
-
(1) 写出正丁烷的结构简式:;写出漂白粉有效成分的化学式:。
-
(2) 写出镁条和氮气反应的化学方程式。写出铁和氯化铁溶液反应的离子方程式。写出乙烯和水反应的化学方程式。
| 选项 | 用途 | 解释 |
| A | Na可用于与TiCl4反应得Ti粉 | Na具有强还原性 |
| B | 明矾可用于净水 | 明矾能杀菌消毒 |
| C | Na2O2可用于潜水艇制O2 | Na2O2具有强氧化性 |
| D | MgO、Al2O3可用于制作耐高温坩埚 | MgO、Al2O3在高温下化学性质稳定 |
-
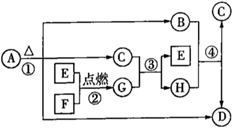
(1) G的化学式为,G中阴、阳离子个数比为,每生成1 mol G转移电子的物质的量为。
-
(2) A、D的水溶液均呈(填“酸性”“碱性”或“中性”)。反应①②③④中属于氧化还原反应的有个。A~H中焰色呈黄色的物质有种。
-
(3) 写出下列反应的化学方程式。
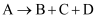 :,
:, 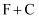 :。
:。

已知:2NO+Na2O2=2NaNO2 , 2NO2+Na2O2=2NaNO3。
-
(1) 装置A中发生反应的离子方程式为。
-
(2) 反应开始时先打开止水夹K,通入氮气至F中产生大量气泡后再关上止水夹K。
①通入N2的目的是,若实验时观察到,说明通入N2未达到预期目的。
②若通入N2未达到预期目的,装置B可除去NO中的NO2杂质,该反应的化学方程式为。
-
(3) 实验时装置D中的实验现象是。
-
(4) 装置C、E不可省去,省去会导致产品中混有杂质和。
-
(5) 装置F的作用是。
-
(1) 以上气体所含元素原子中,未成对电子最多的原子是(填元素符号),S原子中能量最高电子的电子云形状为。
-
(2) 化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是,若反应中有0.08mol的氨气被氧化,则有mol电子发生转移。
-
(3) ①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=。
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
离子
Na+
K+
NH

H+
SO

NO

Cl-
浓度/(mol·L-1)
6×10-6
4×10-6
2×10-5
a
4×10-5
2×10-5
3×10-5
根据表中数据计算,检测的溶液pH=。
-
(4) NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体L(标准状态)。
- 两颗行星的质量分别为m1和m2,它们绕太阳运动的轨道半径为R1和R2、若m1=2m2、R1=4R2,则它们的周期之比T1
- Michael Jackson’s sudden death really astonished(震惊) his fan
- 已知数列{an}的通项公式为,则数列{bn}的前10项和T10=() A.70
- 古代诗歌阅读 中夜起望西园值月上 柳宗元 觉闻繁露坠,开户临西园。寒月上东岭,泠泠疏竹根。 石泉远逾响,山鸟时一喧。倚楹
- 下列粒子可以通过得到电子变成原子的是( ) A.Cl B.O2- C. D.
- 在对“人体吸入的空气和呼出的气体”的探究实验所得出的结论中,不正确的是( ) A.人体呼出的气体中氧气的含量比空气中氧
- 在25℃、101KPa时,______mol______物质_______燃烧生成_________的氧化物时所放出的热
- In the cross-lake swimming race, a boat will be ____in case
- 阅读下面的材料,按要求作文(60分)请以“生活中的加减法”为题,写一篇不少于800字的文章。要求:①自拟题目。②立意自定
- 与发达国家相比,现阶段发展中国家城市化速度慢、水平低
- 在中,若,则的形状一定是( ) A.锐角三角形 B.钝角三角形 C.直角三角形 D.等腰三角
- 河北钢铁集团通过联合重组抵御和化解金融危机带来的风险,先后组建成立国际贸易公司、矿业公司、销售总公司、采购总公司,实现了
- 有一道竞赛题,甲解出它的概率为,乙解出它的概率为,丙解出它的概率为,则甲、乙、丙三人独立解答此题,只有1人解出的概率是(
- 关于意识的本质问题,唯心主义的错误在于 A. 否认意识对物质的决定作用 B. 夸大物质决定意识的作用 C. 否认意识对物
- 已知sinθ=,cosθ=,其中θ∈[],则下列结论正确的是()A. m∈[3,9] B. m∈(﹣∞,5)∪[3,+∞
- In a time of social reform, people’s state of mind tends to
- 对下列句中加点词的解释不正确的一项是 A.长不满七尺,滑稽多辩 滑稽:形容口齿流利,圆转自如。B.先生少之乎
- 在直角坐标系中,已知△ABC三个顶点的坐标分别是 A(0,),B(-1,0),C(1,0),则∠ABC的度数为 °
- 把方程化成的形式,则m、n的值是( ) A、4,13 B、-4,19 C、-4,1
- 2010年6月11日﹣﹣7月11日举行的南非世界杯给无数的球迷留下多个充满激情的时刻.下列关于足球运动所包含的生物学知识



