第一节 化学实验基本方法 知识点题库
A、加热分解 B、结晶法 C、分液法 D、蒸馏法 E、过滤法
①分离水和汽油的混合物;②除去氧化钙中的碳酸钙.
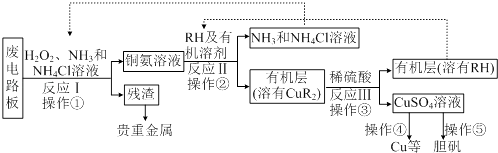
回答下列问题:
-
(1) 反应Ⅰ是将Cu转化为Cu(NH3)2+4,反应中H2O2 的作用是.
-
(2) 反应II是铜氨溶液中的Cu(NH3)2+4与有机物RH反应,写出该反应的离子方程式:.操作②用到的主要仪器名称为,其目的是(填序号).
a.富集铜元素 b.使铜元素与水溶液中的物质分离 c.增加Cu2+在水中的溶解度
-
(3) 操作④以石墨作电极电解CuSO4 溶液.阴极析出铜,阳极产物是.操作⑤由硫酸铜溶液制胆矾的主要步骤是.
-
(4) 流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是.
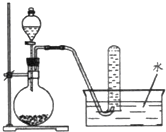
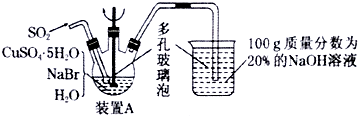
实验步骤:
①在装置A中加入50.0gCuSO4·5H2O、30.9gNaBr、150 mL蒸馏水,60℃时不断搅拌,以适当流速通入SO2;
②溶液冷却后倾去上层清液,在避光的条件下过滤;
③依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤;
④在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4 h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。
回答下列问题:
-
(1) 步骤②中过滤需要避光的原因是。
-
(2) 步骤①中实验所用蒸馏水事先要进行的处理操作是,控制反应在60℃条件下进行,实验中可采取的措施是。
-
(3) 步骤③中洗涤剂需“溶有SO2”的原因是;最后洗涤剂改用乙醚的目的是。
-
(4) 装置A中反应生成CuBr的离子方程式为;说明反应已完成的现象是。
-
(5) 本实验产品的产率是。
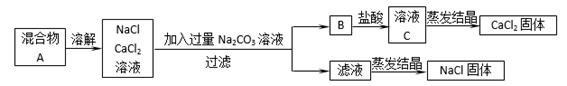
回答下列问题:
-
(1) 物质B的名称为;
-
(2) 将此实验分离得到的NaCl,经分析含杂质是因为上述方法中某一步设计的错误,请写出错误的这一步正确的设计方案:
-
(3) 写出上述过程中所涉及的化学反应方程式:
-
(4) 若实验结束时,称量得到的NaCl固体的质量为17.55g,CaCl2固体的质量为11.1g,则原混合物中NaCl和CaCl2的物质的量之比为。
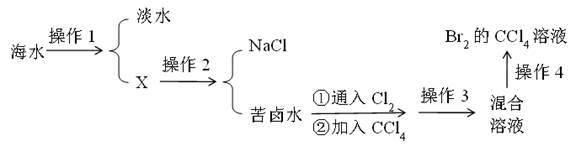
实验中的操作1、操作2、操作3、操作4分别为( )
-
(1) 方案一:铜粉还原CuSO4溶液
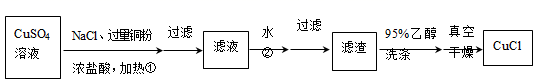
请回答:
步骤①中发生反应的离子方程式为。
-
(2) 步骤②中,加入大量水的作用是。
-
(3) 如图流程中用95%乙醇洗涤和真空干燥是为了防止。
-
(4) 随着pH减小,Cu2(OH)4﹣nCln中铜的质量分数。
A.增大 B.不变 C.减小 D.不能确定
-
(5) 方案二:在氯化氢气流中加热CuCl2•2H2O晶体制备,其流程和实验装置(夹持仪器略)如图:
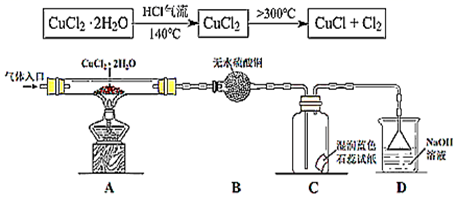
请回答:
实验操作的先后顺序是a→→→→e(填操作的编号)
a检查装置的气密性后加入药品b点燃酒精灯,加热
c在“气体入口”处通入干燥HCl d熄灭酒精灯,冷却
e停止通入HCl,然后通入N2
-
(6) 在实验过程中,观察到B中无水硫酸铜由白色变为蓝色,C中试纸的颜色变化是。
-
(7) 反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2杂质,请分析产生CuCl2杂质的原因。
-
(1) 某同学采用萃取-分液的方法从碘水中提取碘,主要操作步骤如图:
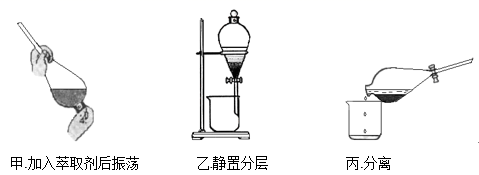
①该同学所采用的萃取剂可能是(填“A”、“B”或“C”)。
A.酒精 B.苯 C.四氯化碳
②甲、乙、丙3步实验操作中,错误的是(填“甲”、“乙”或“丙”)。
-
(2) 实验室制取、净化并收集氯气涉及以下几个主要阶段:

实验室制取氯气的化学方程式。
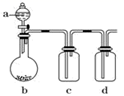
| 选项 | 目的或叙述 | 操作或叙述 |
| A | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
| B | BaSO4难溶于酸 | 用盐酸和BaCl2溶液检验SO42- |
| C | 原溶液中有SO42- | 滴加BaCl2溶液,生成白色沉淀 |
| D | 某钾盐是K2CO3 | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 |
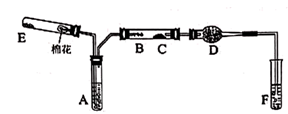
图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水 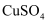 粉末,D为碱石灰,F为新制的碱性
粉末,D为碱石灰,F为新制的碱性 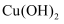 悬浊液。
悬浊液。
-
(1) 在上述装置中,实验时需要加热的仪器从左到右依次为(填仪器或某部位的代号)、、、(可以填满,也可以不填满);
-
(2) 为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是;
-
(3) 检验乙醇氧化产物时F中的实验现象是;
-
(4) E处是一种纯净物,其反应方程式为;
-
(5) 写出乙醇发生催化氧化成乙醛的化学方程式。
 ):加入NaOH溶液,振荡,静置后分液
):加入NaOH溶液,振荡,静置后分液
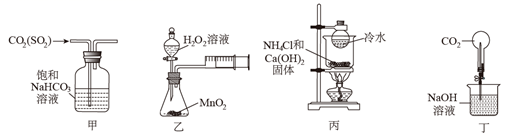
 中混有的
中混有的  B . 利用乙装置测定
B . 利用乙装置测定  的生成体积
C . 利用丙装置分离
的生成体积
C . 利用丙装置分离  和
和 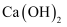 固体
D . 利用丁装置做喷泉实验
固体
D . 利用丁装置做喷泉实验
 , 还有部分
, 还有部分 、
、 , 以及少量不溶于酸碱溶液的其它杂质.工业上从铝土矿中提取铝可采取如图工艺流程:下列说法中描述正确的是( )
, 以及少量不溶于酸碱溶液的其它杂质.工业上从铝土矿中提取铝可采取如图工艺流程:下列说法中描述正确的是( )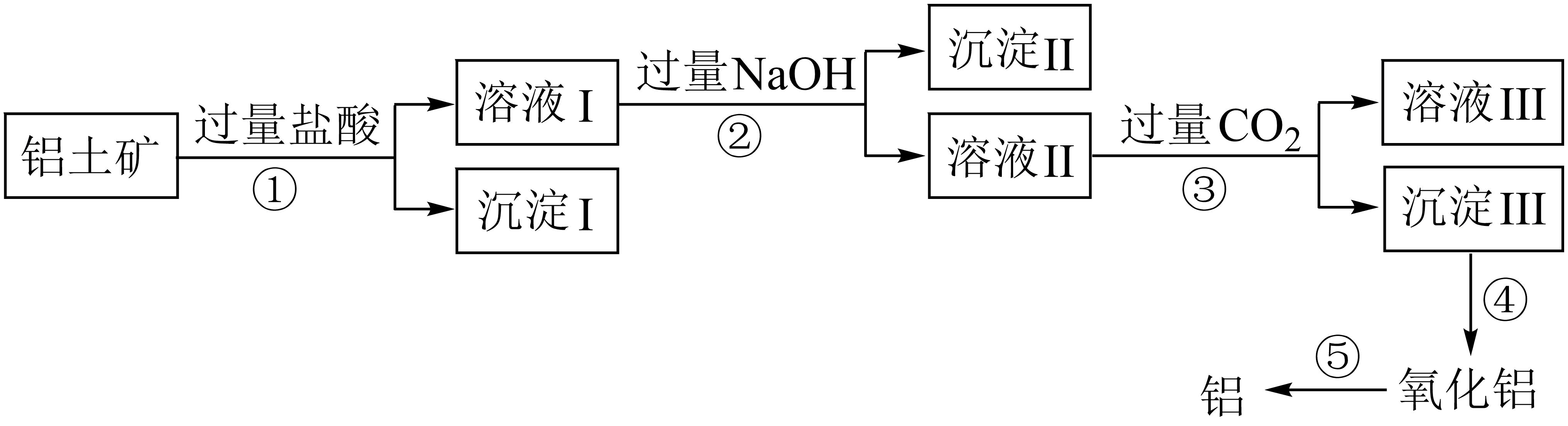
 B . 溶液Ⅱ中含有的阴离子只有
B . 溶液Ⅱ中含有的阴离子只有 C . ①-⑤中,只发生氧化还原反应的是⑤
D . ③的离子方程式只有:
C . ①-⑤中,只发生氧化还原反应的是⑤
D . ③的离子方程式只有: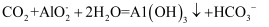
-
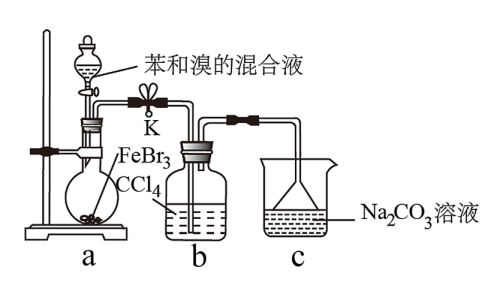
(1) Ⅰ.制备溴苯:
盛放苯和溴的仪器名称为
-
(2) 在该反应中催化剂是;实验中装置b吸收挥发出的和苯,液体颜色逐渐变为。
-
(3) 装置c中倒扣的漏斗作用是。
-
(4) 写出圆底烧瓶中苯发生反应的化学方程式。
-
(5) Ⅱ.分离提纯溴苯:
反应后的混合液加入NaOH溶液振荡、静置、(填写实验操作方法),在有机层中加干燥剂,最后蒸馏分离出沸点较低的苯,得到溴苯。
- 2009年8月21日是乌鲁木齐进入斋月的第一天(伊斯兰教历的第九个月称为斋月,穆斯林每年在这个月实行斋戒,每天从黎明到日
- 阅读下文,完成文后各题。 中国文化的当代处境 王岳川 处在千纪年转换的历史节点上,我们有可能检视一个世纪学术文化
- 在△ABC中,∠C=90°,BC=16cm,∠BAC的平分线交BC于D,且BD︰DC=5︰3,则D到AB的距离为____
- 2006年3月18日,国家统计局公布了根据经济普查资料对2004年消费率重新测算的结果为54.3%。我国居民消费率偏低,
- 下列各句中,加点的词语运用正确的一项是A.一提到大地,让人首当其冲想到的就是母亲。日前,在上海市复兴公园内的道路上,艺术
- 下列电子式书写正确的是 A.氯化钠 B.氨气 Na+[::]2-Na+ C.氯化钙
- 对滴管正确使用方法叙述错误的是() A.滴瓶上的滴管专用,取用试剂后不要洗涤立即放回原位 B.非专用滴管可连续在不同试剂
- 下列说法正确的是( ) A.含有共价键的化合物一定是共价化合物 B.不同元素原子形成的多原子分子中,含有的化学键
- 某海域有、两个岛屿,岛在岛正东4海里处。经多年观察研究发现,某种鱼群洄游的路线是曲线,曾有渔船在距岛、岛距离和为8海里处
- 日常生活中人们常喝纯净水,市场上出售的纯净水有一些是蒸馏水。对于这一类纯净水的下列说法,正确的是 ( ) A.它
- 1999年,中国电信业务分拆,相互竞争的格局出现;2002年,中国电信南北分拆,进一步打破垄断;2008年,新一轮的电信
- I like several skirts on, but _________ of them looked nice.
- 材料一:中国十七届四中全会审议通过了《中共中央关于加强和改进新形势下党 的建设若干重大问题的决定》,指出:世情、国情、
- 下列说法正确的是 A.的一溴代物和的一溴代物都有4种(不考虑立体异构) B.CH3CH=CHCH3分子中的四个碳原子在同
- 分解因式:2m3-8m=____________.
- “达菲”是目前世界上预防甲型H1N1流感的良方之一。生产药品的主要原材料是我国传统香料八角茴香中所含的莽草酸,根据莽草
- (四川延考理3文3)的展开式中含的项的系数为(A)4 (B)6 (C)1
- 往暖水瓶中灌水时,可以根据发出声音的______变化来判断暖水瓶中水的多少;听音乐时,我们能分辨出小号声和钢琴声,是因为
- 将酵母菌研磨离心后得到的上清液(含细胞质基质)和沉淀物(含细胞器),以及未经离心的酵母菌匀浆,分别置于甲、乙、丙三支试管
- 百团大战时期 A.英德战争爆发 B.《大西洋宪章》发表 C.丘吉尔领导英国军民抗击德国法西斯 D.美军取得中



