第一节 化学实验基本方法 知识点题库
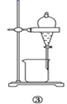
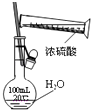 配制一定浓度硫酸溶液
B .
配制一定浓度硫酸溶液
B . 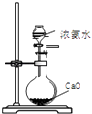 制备少量氨气
C .
制备少量氨气
C . 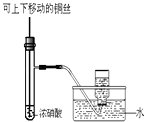 制备并收集少量NO2气体
D .
制备并收集少量NO2气体
D . 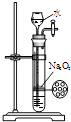 制备少量氧气
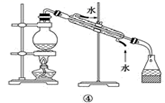
制备少量氧气
-
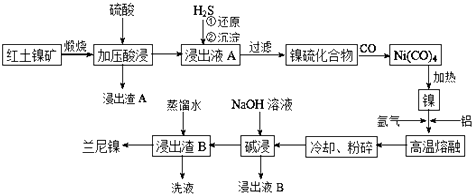
(1) 在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为;
-
(2) 已知红土镍矿煅烧后生成Ni2O3 , 而加压酸浸后浸出液A中含有Ni2+ , 写出有关镍元素的加压酸浸的化学反应方程式;
-
(3) 向浸出液A中通入H2S气体,还原过程中发生反应的离子方程式是;
-
(4) “高温熔融”时能否将通入氩气换为CO并说明原因
-
(5) “碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程中发生反应的离子方程式为.浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,请用化学反应原理加以解释:;
-
(6) 浸出液B可以回收,重新生成铝以便循环利用.请设计简单的回收流程:浸出液B→.(示例:CuOCu2+Cu)
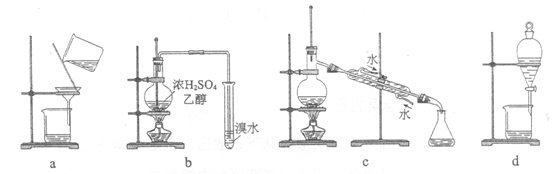
①蒸馏时,先点燃酒精灯,再通冷凝水
②加热氯酸钾和二氧化锰制备氧气,用排水法收集气体后,先移出导管后撤酒精灯
③实验室制取某气体时,先检查装置气密性后装药品
④分液时,先打开分液漏斗上口的塞子,后打开分液漏斗的旋塞
⑤H2还原CuO实验时,先检验气体纯度后点燃酒精灯
⑥使用托盘天平称物质质量时,先放质量较小的砝码,后放质量较大的砝码
⑦蒸馏时加热一段时间,发现忘记加沸石,应迅速补加沸石后继续加热
⑧用98%的浓硫酸配制2mol/L的硫酸时,稀释浓硫酸后先放置至室温后转移到容量瓶中.
请回答:
-
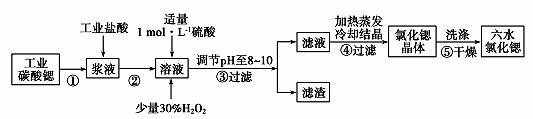
(1) 常温下,氯化锶溶液pH7(填“大于”、“等于”或“小于”);
-
(2) 步骤③所得滤渣的主要成分是(填化学式),调节溶液pH至8~10,宜选用的试剂为 。
A.稀硫酸 B.氢氧化锶粉末 C.氢氧化钠 D.氧化锶粉末
-
(3) 步骤⑤中,洗涤氯化锶晶体最好选用____。A . 水 B . 稀硫酸 C . 氢氧化钠溶液 D . 氯化锶饱和溶液
-
(4) 工业上用热风吹干六水氯化锶,选择的适宜温度范围是____(填字母)。A . 50~60℃ B . 70~80℃ C . 80~100℃ D . 100℃以上
-
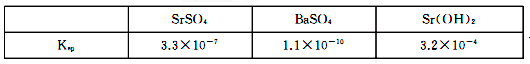
(5) 若滤液中Ba2+浓度为1×10-6 mol/L,依据下表数据可以推算滤液中Sr2+物质的量浓度为 。
| 序号 | 物质 | 杂质 | 选用的试剂或操作方法 |
| A | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
| B | FeCl3 | CaCO3 | 溶解、过滤、蒸发结晶 |
| C | CCl4 | Br2 | 用NaOH溶液洗涤、分液 |
| D | CO2 | SO2 | 通过盛有品红溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
-
(1) I. 甲小组的同学用如图装置制备干燥纯净的Cl2 , 并进行性质实验。

装置A中制取氯气,三种玻璃仪器的名称分别是酒精灯、和,反应的化学方程式为。该反应中盐酸体现了(填字母)。
a.氧化性 b.还原性 c. 酸性 d. 碱性
-
(2) 装置B的作用是。
-
(3) 装置C中盛放的是,目的是除去水蒸气。
-
(4) 装置D可以用作不同的用途。
a. 若装置D用于收集Cl2 , 请将图中装置D的导气管补充完整。
b. 若装置D中放入湿润的蓝色石蕊试纸,可以看到的现象是。
-
(5) II. 乙小组的同学用如图所示装置制取氯水并进行相关实验。
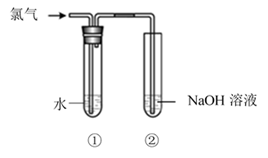
实验进行一段时间后,取少量试管①中的溶液,检验其中有Cl-的方法是。
III. 甲、乙两个小组的同学都用到了NaOH溶液,目的是,反应的离子方程式为。
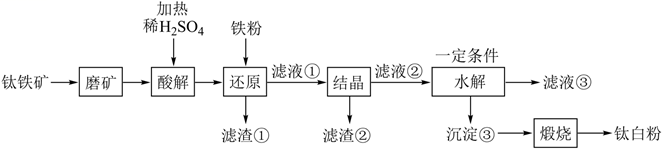 已知:①酸解后,钛主要以TiOSO4形式存在。强电解质TiOSO4在溶液中仅能电离出SO
已知:①酸解后,钛主要以TiOSO4形式存在。强电解质TiOSO4在溶液中仅能电离出SO  和一种阳离子。
和一种阳离子。
②H2TiO3不溶于水和稀酸。
-
(1) 磨矿的目的是。
-
(2) 滤渣①的主要成分是。
-
(3) 酸解过程中,写出FeTiO3发生反应的化学方程式。
-
(4) 还原过程中,加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某实验室做如下尝试。
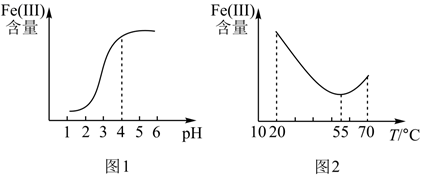
①在其它条件不变的情况下,体系中Fe(Ⅲ)含量随pH变化如图1,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:。
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图2,55℃后,Fe(Ⅲ)含量增大的原因是。
-
(5) 水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的化学式为。
②一定量Fe2+的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中Fe2+的含量。实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理。
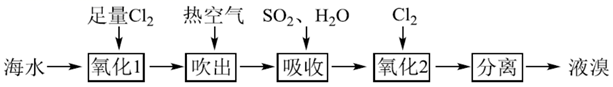
下列有关说法错误的是( )
 溶液制得
B . 吹出后剩余溶液中可能大量存在的离子有
溶液制得
B . 吹出后剩余溶液中可能大量存在的离子有  、
、  、
、  、
、 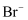 C . 吸收过程发生反应的离子方程式为
C . 吸收过程发生反应的离子方程式为 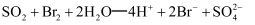 D . 氧化2所得溶液可通过萃取分离出溴
D . 氧化2所得溶液可通过萃取分离出溴
 )可吸收烟气中的
)可吸收烟气中的  ,同时可制备
,同时可制备 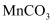 ,工艺流程如下:
,工艺流程如下: 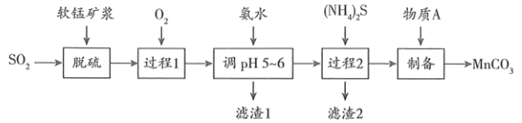
资料:①吸收  后的软锰矿浆中含有
后的软锰矿浆中含有  、
、  、
、  、
、  等阳离子;
等阳离子;
②金属离子沉淀的pH如下表。
| 金属离子 | | | | | |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 6.2 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 8.2 |
-
(1) 脱硫的产物是
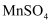 ,软锰矿中
,软锰矿中  所起的作用是。
所起的作用是。
-
(2) 过程1向浆液中通入
 的目的是。
的目的是。
-
(3) 滤渣1的成分是,过程2中发生反应的离子方程式为。
-
(4) 制备
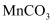 的过程中,一般控制溶液的pH范围为5~7,不宜过大或过小,原因是。
的过程中,一般控制溶液的pH范围为5~7,不宜过大或过小,原因是。
-
(5) 已知:常温下,
 溶液的pH约为9.3,
溶液的pH约为9.3, 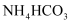 溶液的pH约为7.8.请推测物质A,并写出制备
溶液的pH约为7.8.请推测物质A,并写出制备 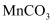 时发生反应的离子方程式:。
时发生反应的离子方程式:。
-
(6) 取m g碳酸锰样品,加适量硫酸加热溶解后,用
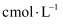 的
的  溶液滴定,至滴定终点时,消耗
溶液滴定,至滴定终点时,消耗  溶液的体积为
溶液的体积为 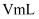 。(已知:反应产物为
。(已知:反应产物为  ,杂质不参与反应),样品中
,杂质不参与反应),样品中 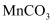 质量分数的计算式为(用质量分数表示)。
质量分数的计算式为(用质量分数表示)。
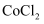 )常用作干湿指示剂、氨的吸收剂、防毒面具和肥料添加剂等。
)常用作干湿指示剂、氨的吸收剂、防毒面具和肥料添加剂等。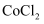 为蓝色粉末,易溶于水和有机溶剂,易升华,吸水潮解会变成红色。某化学实验小组拟选取下列装置来制备无水二氯化钴(装置不能重复使用)。
为蓝色粉末,易溶于水和有机溶剂,易升华,吸水潮解会变成红色。某化学实验小组拟选取下列装置来制备无水二氯化钴(装置不能重复使用)。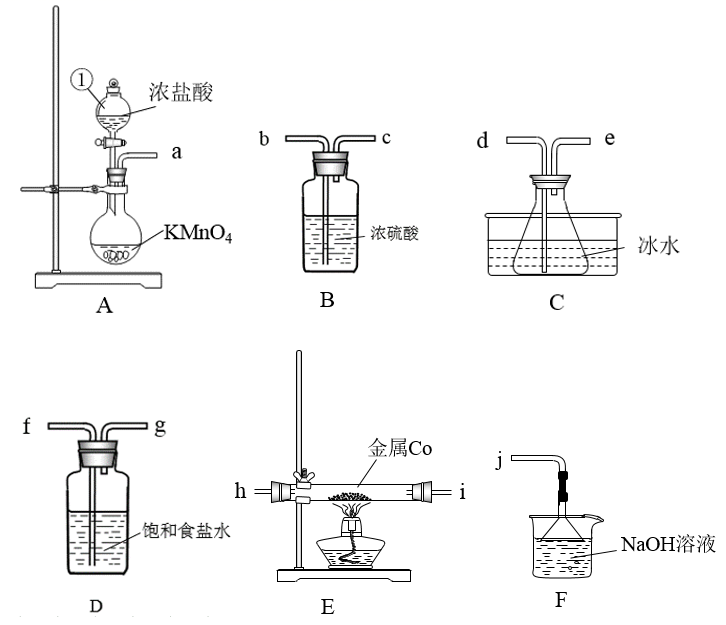
-
(1) 仪器①的名称是,装置
 中发生反应的离子方程式为。
中发生反应的离子方程式为。
-
(2) 根据气流的方向,装置导管口的连接顺序为
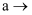
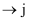 。
。
-
(3) 连接装置,检查气密性,装入药品后,先让
 中发生反应,再点燃
中发生反应,再点燃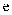 处酒精灯的目的是。
处酒精灯的目的是。
-
(4)
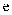 中发生反应的化学方程式为。实验过程中发现,用上述装置制备得到的
中发生反应的化学方程式为。实验过程中发现,用上述装置制备得到的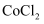 不是蓝色的,而是红色的,原因可能是,若要避免此现象的发生,可采取的措施是。
不是蓝色的,而是红色的,原因可能是,若要避免此现象的发生,可采取的措施是。
-
(5) 实验过程中,装置
 所起的作用是。
所起的作用是。
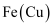 :加过量
:加过量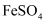 溶液、过滤
B .
溶液、过滤
B .  :通过足量灼热的铜粉,收集气体
C .
:通过足量灼热的铜粉,收集气体
C . 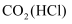 :通入饱和
:通入饱和 溶液,洗气
D . CO气体(
溶液,洗气
D . CO气体( ):通入氧气点燃
):通入氧气点燃
- 25.阅读下面的文字,根据要求作文。(60分) 世间万物总有自己的位置,有的看似在中心,其实已在边缘;有的感觉在边缘,其
- 如图,路灯(点)距地面8米,身高1.6米的小明从距路灯的底部(点)20米的A点,沿OA所在的直线行走14米到B点时,身影
- “ We can’t go out in such bad weather,” said Susan, ___ out
- (﹣)-2﹣+(1﹣)0﹣|﹣2|
- 20.下列关于红绿色盲的说法不正确的是( ) A.红绿色盲患者不能像正常人那样区分红色和绿色 B.Y染色体短小,
- 加强思想控制是维护统治的重要手段,儒学因此而成为我国传统文化的正统。据此回答下面试题 汉武帝问策贤良文学,董仲舒对曰:“
- 下列关于文学常识的表述有误的一组是( ) A.苏轼,北宋文学家、书画家,字子瞻,号东坡居士,与其父苏洵、其弟苏辙合称
- 一辆轿车违章超车,以108km/h的速度驶入左侧逆行道时,猛然发现正前方80m处一辆卡车正以72km/h的速度迎面驶来,
- 下列各句中翻译不正确的一句是( ) A 他日趋庭,叨陪鲤对;今兹捧袂,喜托龙门。 译文:过些日子,(我将到父亲身边),一
- 沸腾是在液体 和液体内部同时进行的汽化现象。
- 将紫色洋葱在完全营养液中浸泡一段时间,撕取外表皮,先用浓度为0.3g/mL的蔗糖溶液处理,细胞发生质壁分离后,立即将外表
- 2008年12月,中国外交部部长杨洁篪在北京说,中日关系通过两国领导人的“破冰”、“融冰”和“迎春”、“暖春”之旅,已经
- 李嘉图认为,商品价格的波动使资本恰好按照必要的数量运行,在没有政府的干预时,农业、商业和制造业最为繁荣,需要国家做的全部
- 如图,直线y=﹣x+m与y=nx+4n(n≠0)的交点的横坐标为﹣2,则关于x的不等式﹣x+m>nx+4n>0的整数解为
- 孔子作为伟大的思想家,他的“有教无类”思想的内涵是( ) A.教育应分类别进行,对不同的人进行不同的教育
- 《春晚》精彩、喜庆,广受观众喜爱。但是不同民族、不同地区、不同年龄、不同性别、不同职业的人,对每年《春晚》的评价有所不同
- 2009年2月1日,全国全面推广“家电下乡”活动,这是应对当前国际金融危机,惠农强农,带动工业生产,促进消费拉动内需的一
- 有人说,中国存在着一种最古老的商朝的书面语。这里的“书面语”是指 A.甲骨文 B.小篆
- 下列生产技术的出现,推动了社会生产关系发生了质的飞跃是( ) A.春秋时期铁制农具和牛耕的推广 B.明朝时引进玉米
- —Howmany teachers are there in your school? —______ them ___




