到实验室去 探究金属的性质 知识点题库

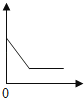
下列实验内容中的横、纵坐标表示的量符合如图所示趋势是( )
序号 | 实验内容 | 横坐标表示的量 | 纵坐标表示的量 |
① | 饱和氯化钠溶液的稀释 | 加入水的量 | 溶质质量分数 |
② | 过量红磷测定空气中氧气含量 | 时间 | 红磷质量 |
③ | 过氧化氢溶液与二氧化锰制氧气 | 时间 | 二氧化锰的质量 |
④ | 向铜、锌混合物粉末中加入盐酸 | 盐酸的质量 | 剩余固体的质量 |
选项 | 括号内为杂质 | 方 法 |
A | CO2(HCl气体) | 通过足量的NaOH溶液 |
B | KCl (KClO3) | 加入少量MnO2加热 |
C | NaCl(Na2CO3) | 加入足量的盐酸后蒸干 |
D | Fe(Cu) | 加入足量的稀H2SO4后过滤 |
某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案

-
(1) 试管乙中观察到的现象是 , 反应的化学方程式为
-
(2) 同学们经讨论后认为该方案可以优化, 试管的实验是多余的.同学经讨论得出三种金属的活动性由强到弱的顺序为
-
(3) 去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物和滤液,并对不溶物的成分进行如下探究:
【提出问题】烧杯中不溶物的成分是什么?
【实验探究】向过滤得到的不溶物中加稀硫酸
①若无气泡产生,则不溶物的成分是 ;
②若有气泡产生,则不溶物中一定含有 ,可能含有 .

-
(1) 实验一:向滤渣中加入稀硫酸,无气泡产生,则滤渣中一定含有的物质是.
-
(2) 实验二:为确定滤液的成分,同学们设计了如下方案:
实验步骤
实验现象
结论
取少量滤液于试管中,向其中加入
有气泡产生,有红色固体析出
-
(3) 该实验涉及的反应的化学方程式为,.
-
(4) 反思,有同学提出滤液中硫酸铜的确定不需要通过化学变化,原因是.
选项 | 物质 | 杂质 | 除杂方法 |
A | CO2 | 水蒸气 | 通入浓硫酸中 |
B | NaCl溶液 | NaOH溶液 | 加入适量BaCl2溶液,过滤 |
C | 铁粉 | 铜粉 | 加入足量的稀硫酸,过滤 |
D | CaO | CaCO3 | 加入适量稀盐酸,过滤 |
【查阅资料】在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
-
(1) 【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是.
【实验现象】
金属
Ti
Mg
Ag
反应现象
反应缓慢
反应强烈
无明显现象
【实验结论】原假设中不正确,理由是.
【结论】用不同浓度的足量稀盐酸反应,是否也能得出同样结论?,请说明理由
-
(2) 小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).

两个图象中存在有错误的是的图象,判断错误的理由是,
图象不同的原因是.
由该实验可以得到的结论:
①金属与酸反应的速率与有关.
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与有关.
-
(3) 将铁粉加到硫酸铜溶液中,可能观察到的现象有.
选项 | 待提纯的物质(括号内为杂质) | 所加试剂 | 操作方法 |
A | CuSO4(铁粉) | 足量水 | 溶解、过滤 |
B | FeCl3溶液(CuCl2) | 过量铁粉 | 过滤 |
C | CaO(石灰石) | 无 | 高温 |
D | Cu(Zn) | 足量稀盐酸 | 过滤、洗涤、干燥 |
-
(1) 汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和性 。
-
(2) 汽车使用天然气作燃料,排放污染较低,天然气的主要成分是。
-
(3) 车体的主要材料为钢,工业上用一氧化碳和赤铁矿炼铁的化学方程式为。

-
(1) 所标物质中,属于合金的是(填一种即可,下同),属于合成材料的是.
-
(2) 铝有很好的抗腐蚀性,其原因是.
-
(3) 用可以鉴别自来水是硬水还是软水,把煮好米饭的盖子打开,从内盖上滴下来的水是(填“硬水”或“软水”).
-
(4) 过去煮饭使用烧柴火的大铁锅,现在可使用自动定时的电饭煲,由此,你对化学与人类生活的关系有何感想.
Ⅰ.制备FeSO4。
-
(1) 请你写出一个以Fe为原料制备FeSO4的化学方程式,若有5.6 g Fe完全反应,理论上生成FeSO4g。
-
(2) Ⅱ.小组同学在用绿矾配制FeSO4溶液时发现,溶液颜色会由绿变黄。然后进行如下探究:
【查阅资料】
ⅰ.FeSO4溶液能与氧气反应,反应生成的可溶性含铁物质遇KSCN溶液会变红。
ⅱ.保存FeSO4溶液时要加入稀硫酸和铁钉,置于阴凉处。
【提出猜想】
影响FeSO4溶液与氧气反应速率的因素可能有温度、浓度、溶液酸碱性、是否有铁钉等。
【进行实验】

【解释与结论】
通过对比实验②和③,得出的结论是 。
-
(3) 欲得出“稀硫酸和铁钉共同存在下才能有效防止FeSO4溶液变质”的结论,需要对比 (填编号)。
-
(4) 实验⑤中,FeSO4溶液变质的反应如下,补全该反应的化学方程式。4FeSO4 + 2H2SO4+ O2 =2Fe2(SO4)3 +
-
(5) 下列说法正确的是 _____ .A . 其他条件相同,溶液酸性增强,FeSO4溶液变质加快 B . 其他条件相同,FeSO4溶液浓度越大,变质越快 C . 实验⑥中,滴加KSCN溶液后,略显红色,振荡后溶液变为浅绿色,可能是发生了反应Fe2(SO4)3 +Fe=3FeSO4 D . “其绛矾本来绿色……烧之赤色”,颜色发生变化的原因可能是铁的化合价发生了变化
 将表面生锈的铁钉放入稀盐酸中
B .
将表面生锈的铁钉放入稀盐酸中
B .  红磷在密闭容器中燃烧
C .
红磷在密闭容器中燃烧
C .  向硫酸铜溶液中加入锌粉
D .
向硫酸铜溶液中加入锌粉
D .  向稀盐酸中滴加硝酸银溶液
向稀盐酸中滴加硝酸银溶液
 国家宝藏
国家宝藏  是央视于2017年底推出的大型文博探索节目,节目中展示了大量中华瑰宝,其中有大量金属材料。
是央视于2017年底推出的大型文博探索节目,节目中展示了大量中华瑰宝,其中有大量金属材料。
-
(1) 下列选项中,不属于金属材料的有______
 填序号,下同
填序号,下同  。
A . 越王勾践剑 B . 曾侯乙编钟 C . 洛神赋图 D . “瓷母”釉彩大瓶
。
A . 越王勾践剑 B . 曾侯乙编钟 C . 洛神赋图 D . “瓷母”釉彩大瓶 -
(2) 越王勾践剑因剑身镀有含铬金属而千年不变形、不生锈,镀铬的作用有______A . 隔绝空气 B . 增强硬度 C . 增强导热性 D . 提高耐磨性
-
(3) 皿天全方罍堪称是“方罍之王”,是古代青铜器的一种,青铜是由铜与锡
 制成的合金。现有铜丝和锡丝,下列能探究二者金属活动性顺序的试剂有______
A . 稀盐酸 B . 硫酸铜溶液 C . 硝酸银溶液 D . 氯化镁溶液
制成的合金。现有铜丝和锡丝,下列能探究二者金属活动性顺序的试剂有______
A . 稀盐酸 B . 硫酸铜溶液 C . 硝酸银溶液 D . 氯化镁溶液 -
(4) 铝是近几十年来应用仅次于钢的金属。将一定量的铝条投入硝酸锌和硝酸铜的混合溶液中,充分反应后过滤。若滤液中只含有一种溶质,则滤渣中一定含有
 填物质名称
填物质名称  写出该过程中首先发生的化学反应方程式。
写出该过程中首先发生的化学反应方程式。
-
(1) 铝有很好的抗腐蚀性,其原因:。(化学方程式表示)
-
(2) 铁制品生锈的条件是 。
-
(3) 我国是世界上最早采用湿法冶金提取铜的国家,铁和硫酸铜溶液反应的化学方程式为。
- 关于人体体温调节的叙述,错误的是 ( ) A.呼气是人体的主要散热途径 B.骨骼肌和肝脏是人体的主要产热器官 C
- 对于有理数x、y ,规定新运算x*y=ax-by,其中a,b是常数,等式右边是通常的加减法和乘法运算,已知2*3=6,5
- 利用单摆验证小球平抛运动规律,设计方案如图(a)所示,在悬点O正下方有水平放置的炽热的电热丝P,当悬线摆至电热丝处时能轻
- 【10乌鲁木齐市1】.“低碳生活”、“低碳经济”、“碳减排”等日常出现在电视新闻或报纸上,其中关于“低碳生活”中的“低碳
- 读世界某区域图,回答6题。20080801 6.甲区域是世界重要农业区,该地( )
- “打倒列强,除军阀”、“星星之火,可以燎原”、“将革命进行到底”。上述口号所反映的历史发展主题是 A.工农武装割据
- (一)文言文阅读(14分) 阅读下面的文言文,完成后面的题。 李纲,字伯纪,邵武人也。登政和二年进士第,积官至监察御史兼
- 读我国能源调运图,回答4~6题。4.图中①②③三条运输路线输送的主要能源分别是 A.煤炭、石油和天然气
- 阅读下面的文字,完成以下各题。 生物发光的奥秘 说
- 在国际社会中,任何国家都不得以任何方式强迫他国接受自己的意志,各国在外交文件上有使用本国文字的权利。这体现了主权国家在国
- 阅读下列材料: 材料一 哀公问政于孔子,孔子对曰: “政之急者,莫大乎使民富且寿也。”公曰:“为之奈何?”孔子曰:“省力
- (10分)容积为2L的烧瓶,在压强为1.0×105Pa时,用塞子塞住,此时温度为27℃,当把它加热到127℃时,塞子被打
- 已知关于x的方程有增根,则m的值为() A.﹣3 B.1 C.1或0 D.3或﹣5
- 我国的根本政治制度是 A.人民代表大会制度 B.基层群众自治制度C.多党合作制度 D.民族区域自治制度
- 如图17所示,电源电压保持不变,小灯泡L标有“6V 3W”的字样,其电阻不随温,滑片P从b端向a端滑过三分之一时,小灯泡
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的以下短文。短文中共有10处错误,每句中最多有两处。错误涉及一
- 第一次不结盟首脑会议通过大会宣言,表示“参加这次会议的不结盟国家无意组成一个新的集团而且也不能成为一个集团”。对此理解不
- 做平抛运动的物体,在水平方向通过的最大距离取决于 ( )A.物体的高度和受到的重力 B.物体受到
- 当公共权力被滥用,政府官员不尽职时,作为公民,应当立即举起手中的利剑,依法同腐败分子作斗争。这里,公民能够立即举起的利剑
- 如图所示,根据通电螺线管的磁感线方向,可判断通电螺线管左端为______极,电源的a端为______极,小磁针静止时的b



