到实验室去 探究金属的性质 知识点题库

-
(1) 地壳中含量最多的金属元素是.
-
(2) 用铜、铝做导线,利用了它们的性.
-
(3) 铁锅易生锈,铁生锈的条件是铁与空气中的水和共同作用的结果,防止家中铁锅锈蚀的方法是(答一种).
-
(4) “曾青得铁则化为铜”(西汉•刘安《淮南万毕术》)被誉为现代湿法冶金的先驱.意思是铁与天然存在的硫酸铜溶液发生反应置换生成单质铜,该反应的化学方程式为.
-
(1) 铸造硬币用到的材料是(填“合成材料”或“金属材料”);
-
(2) 写出Ni与CuSO4溶液发生置换反应的方程式.
 向一定质量的氢氧化钠溶液中加入稀硫酸至过量
B .
向一定质量的氢氧化钠溶液中加入稀硫酸至过量
B .  向一定质量的稀硫酸中加入锌片
C .
向一定质量的稀硫酸中加入锌片
C .  加热一定质量的高锰酸钾固体
D .
加热一定质量的高锰酸钾固体
D .  向一定质量的二氧化锰中加入过氧化氢溶液
向一定质量的二氧化锰中加入过氧化氢溶液
请你用所学的化学原理解释.

-
(1) 如图中“──”表示两端的物质间能发生化学反应,其中 X 是初中化学中常见的化合物,请回答:
①试写出 X 与 Na2CO3 反应的化学方程式.
②如图所示的三个反应中,有一个不属于复分解反应,请写出该反应的化学方程式.
-
(2) 铝在空气中抗腐蚀的原因(用化学方程式表示).
-
(3) 甲醇(CH3OH)和乙醇一样,也能在空气中燃烧,其在空气中燃烧的化学方程式.
 加水稀释氢氧化钠
B .
加水稀释氢氧化钠
B .  等质量等浓度的过氧化氢溶液分别制取氧气
C .
等质量等浓度的过氧化氢溶液分别制取氧气
C .  等质量的铁粉、镁粉、锌粉分别跟同浓度的盐酸反应
D .
等质量的铁粉、镁粉、锌粉分别跟同浓度的盐酸反应
D .  某温度下,向一定量的不饱和硝酸钾溶液中加入硝酸钾固体
某温度下,向一定量的不饱和硝酸钾溶液中加入硝酸钾固体
① |
| 地壳中含量最多的金属元素是; | ② |
| 松花江跨江桥的建设中用到了钢,钢的含碳量范围是; |
③ |
| 很多宝石中含有才使它们变得绚丽多彩; | ④ |
| 钛合金与人体有很好的,因此可以用来制造人造骨; |
⑤ |
| 菱铁矿主要成分的化学式为; | |||
 向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
B .
向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
B .  向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
C .
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
C .  用等质量、等溶液的过氧化氢溶液在有无催化剂条件下制氧气
D .
用等质量、等溶液的过氧化氢溶液在有无催化剂条件下制氧气
D .  一定质量稀盐酸中逐滴加入氢氧化钠溶液
一定质量稀盐酸中逐滴加入氢氧化钠溶液
-
(1) Ⅰ探究CO与Fe2O3的反应产物(夹持仪器已略去)

【实验过程】步骤1 在通风橱中,按图Ⅰ连接装置并检验装置的气密性.
步骤2 装入试剂:玻璃管内装入Fe2O3粉末,试管Ⅰ中装入澄清石灰水.
步骤3 从a端通入CO一段时间,待,再点燃酒精灯.
-
(2) 【实验现象】反应一段时间后,玻璃管内粉末由色变成黑色,生成的黑色固体均能被玻璃管上方的磁铁吸引.试管Ⅰ中出现白色沉淀(用化学反应方程式表示:.
-
(3) 【查阅资料】铁粉、FeO、Fe3O4均为黑色固体;铁粉、Fe3O4均能被磁铁吸引.
【提出猜想】对磁铁吸引的黑色固体成分有以下三种猜想:
猜测Ⅰ:Fe;猜测Ⅱ:Fe3O4;猜测Ⅲ:Fe和Fe3O4
【实验验证】取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,观察到红色固体中混有黑色颗粒,说明(填“猜想Ⅰ”“猜想Ⅱ”或“猜想Ⅲ”)是正确的.
-
(4) 【拓展研究】进一步查阅资料,发现CO能溶于铜液[醋酸二氨合铜(Ⅰ)和氨水的混合液].因此可在装置Ⅰ后再连接下图装置Ⅱ,其目的是,装置Ⅰ、Ⅱ的连接顺序:b连接(填“c”或“d”).
-
(5) Ⅱ原料气CO的制备
方法一:加热MgCO3、Zn的混合物可快速制备CO,同时还得到两种金属氧化物:、(填化学式).
方法二:加热草酸晶体(H2C2O4•2H2O)制备CO:
H2C2O4•2H2O
 CO↑+CO2↑+3H2O
CO↑+CO2↑+3H2O已知:常压下,草酸晶体的熔点为101℃.比较草酸晶体的熔点和分解温度,
分析若选用装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是.
-
(1) 地壳中含量最高的金属元素是。
-
(2) 在建筑工地露天放置的钢铁容易生锈,钢铁生锈实际是铁与空气中的 和 (填化学式或名称)发生化学反应生成。根据铁生锈的条件,自行车支架采取的防锈措施是。
-
(3) 铝具有很好的抗腐蚀性能,原因是(用化学方程式表示)。
-
(4) 下列用品中,主要利用金属导电性的是 (填字母)A . 铂金饰品 B . 铁锅 C . 铝导线
-
(5) 为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是(填序号)
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中

-
(1) 按要求填空:
①表示3个氮分子的是(填序号),②表示铁离子的是(填序号),
③a与d两粒子结合形成的物质是(填化学式)。
-
(2) 人类的生产和生活都离不开金属。
①金属元素在自然界中分布很广,地壳中含量最多的金属元素是(填名称),写出其在空气中被氧化的化学方程式。
②使用过的菜刀、铁锅等铁制品,清洗后需要及时擦干放置,可以减少对铁锈蚀的影响。

-
(1) 常温下大多数金属都是固体,但体温计中的金属却是液体,该金属是
 写符号
写符号 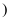 。
。
-
(2) 制作门窗的材料用铝合金,铝在空气中比铁更耐腐蚀。其原因是
 用化学方程式表示
用化学方程式表示 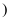 。
。
-
(3) 如图是生活中常用的铁锅。把铁制成铁锅利用了铁的延展性和性。为防止铁锅锈蚀,可采用的一种防锈方法是。
| 实验目的 | 方法一 | 方法二 | |
| A | 鉴别食盐水和蒸馏水 | 测导电性 | 加入肥皂水 |
| B | 检验铜粉中混有铁粉 | 加入稀盐酸 | 加入硫酸铜溶液 |
| C | 除去CO2中混有的CO | 通入适量O2 , 点燃 | 通过灼热的氧化铁 |
| D | 分离MnO2、KCl固体 | 溶解、过滤 | 蒸发 |
甲同学:将铁屑放入稀盐酸中;
乙同学:将氧化铁粉末放入稀盐酸中。
-
(1) 甲同学获得的溶液为色,所以大家一致认为这不是FeCl3溶液;
-
(2) 乙同学所做实验发生反应的化学方程式为;
-
(3) 乙同学向所得的溶液中逐滴加入氢氧化钠溶液,过一会儿才产生沉淀,则乙同学所得溶液中的溶质为。
-
(1) 铁可以做成铁锅炒菜,主要是利用了铁的(填“导电”或“导热”)性。
-
(2) 航母外壳用涂料覆盖,是为了防止钢铁材料与接触而锈蚀。
-
(3) 铁锈的主要成分是氧化铁,用盐酸可以除去自行车钢圈上的铁锈,其反应的化学方程式是。
-
(4) 在硝酸铜和硝酸银的混合溶液中,加入一定量铁粉,使之充分反应后,过滤,向所得滤渣中加入适量稀盐酸,没有气体产生,则滤渣中一定有(填化学式),滤液中的溶质一定含有(填化学式)。
-
(5) 某同学用称量法测定铁在氧气中燃烧的产物。将
 铁在一定量的氧气中燃烧得到
铁在一定量的氧气中燃烧得到  固体。则得到的固体产物可能是(填字母)。
固体。则得到的固体产物可能是(填字母)。 A
 B
B  和
和  的混合物
的混合物C
 和
和  的混合物 D
的混合物 D  、
、  和
和  的混合物
的混合物
- 如图,一次函数图象经过点A,且与正比例函数y=-x的图象交于点B,则该一次函数的表达式为( )A、y=-x+2
- 用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( ) A.18O只
- 阅读下面的文字,完成14—17题。 据美国物理学家组织网近日报道,斯坦福大学的研究人员将一种普通棉纱浸入银纳米线
- 甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )A.CH3Cl只有一种空间结构
- 下图为植物组织培养的基本过程,则制作人工种子,及生产治疗烫伤、割伤的药物紫草素,应分别选用的编号是 A.④②
- 已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻
- Group buying is one of the fastestgrowing trends in South Af
- 已知关于x的函数同时满足下列三个条件: ①函数的图象不经过第二象限; ②当时,对应的函数值; ③当时,函数值y随x的增大
- 鸟卵结构中,哪一部分是卵细胞的主要营养部分?( ) A.卵壳 B.卵白 C.胚盘
- Theproject ______ last month but unfortunately it had to be
- “北人避胡多在南,南人至今能晋语。”对唐朝张籍的这句诗理解最准确的是A.北方人大多害怕胡人 B.南方人
- The shop doesn’t open until 11 am, _______ it loses a lot of
- 依次填入下面横线处的词语,恰当的一项是() ①青春意味着勇气多于怯懦,青春意味着冒险多于________。 ②阅读使人充
- 5.A解析:因为函数有0,1,2三个零点,可设函数为f(x)=ax(x-1)(x-2)=ax3-3ax2+2ax 因此b
- He just does what he pleases and never _____ about anyone el
- 下列溶液中,微粒浓度关系正确的是() A.含有NH4+、Cl-、H+、OH-的溶液中,其离子浓度一定是:c(Cl-)&g
- 读“世界某区域某日某时海平面天气图”(单位:百帕),回答4~5题。 4、图中此时可能出现降水天气的地区是( )
- 某研究机构对我国北方草原一种主要害鼠——布氏田鼠进行调查,调查样方总面积为2 hm2(1 hm2=10000 m2),随
- 某地教育部门为了了解学生在数学答卷中的有关信息,从上次考试的10000名考生的数学试卷中,用分层抽样的方法抽取500人,
- 蘑菇(真菌)与光的关系是: A 它们的生长在任何情况下都需要光 B 它们的生长不需要光,但许多类型的蘑菇需要一定量的








