到实验室去 探究金属的性质 知识点题库
下图分别与相应的操作过程相对应,其中正确的是( )
A . 向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B . 向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片
C . 向pH=10的氢氧化钙溶液中不断加水稀释
D . 向含有硫酸的硫酸铜溶液中加入过量的氢氧化钠溶液
2.4g铁和镁的混合物,与50.0g盐酸恰好完全反应,则该盐酸的溶质质量分数可能是( )
A . 15.0%
B . 5.0%
C . 10.0%
D . 16.0%
下列对科学知识的应用错误的是( )
A . 铁由于导热性能好,用来做暖气片
B . 铅锑合金由于熔点低,用来做保险丝
C . 甲醛由于有防腐作用,用来保鲜食品
D . 洗洁精由于有乳化作用,用来除去餐具油污
下列有关金属材料的叙述错误的是( )
A . 回收利用废金属可减少对环境的污染
B . 铝块能制成铝箔是利用了铝的延展性
C . 铝比铁更容易跟氧气和其他物质反应,因而铝的抗腐蚀性能比铁差
D . 焊锡(锡铅合金)比锡熔点低
生活中处处有化学,化学与生活密切相关.
-
(1) 铝常用于制作导线,因为其具有良好的.
-
(2) 将纯铜片和黄铜片(铜锌合金)相互刻画,纯铜上留下明显划痕,说明.
-
(3) 胃酸里含有适量盐酸,服用含氢氧化铝[Al(OH)3]的药物可治疗胃酸过多症,反应的化学方程式为.
-
(4) 幼儿及青少年缺少元素可引发佝偻病和发育不良.
-
(5) 农作物种植过程中可以施用下列化肥,其中属于复合肥料的是 (填序号)A . NH4HCO3 B . KCl C . NH4H2PO4 .
请分别选用一种试剂,除去下列物质中少盘的杂质(括号内的为杂质).
-
(1) Cu (Zn)
-
(2) 硫酸亚铁溶液(硫酸铜).
下列图象与对应实验相符合的是( )
A .  加热一定质量的高锰酸钾制氧气
B .
加热一定质量的高锰酸钾制氧气
B .  用等质量的过氧化氢分别制取氧气
C .
用等质量的过氧化氢分别制取氧气
C .  碳酸氢铵受热完全分解
D .
碳酸氢铵受热完全分解
D .  少量的镁条放入足量的食醋中
少量的镁条放入足量的食醋中
 加热一定质量的高锰酸钾制氧气
B .
加热一定质量的高锰酸钾制氧气
B .  用等质量的过氧化氢分别制取氧气
C .
用等质量的过氧化氢分别制取氧气
C .  碳酸氢铵受热完全分解
D .
碳酸氢铵受热完全分解
D .  少量的镁条放入足量的食醋中
少量的镁条放入足量的食醋中
某化学兴趣小组做以下两个实验:A试管中固体有剩余,B试管中两种物质恰好完全反应,请回答:

-
(1) A试管中发生反应的化学方程式为.
-
(2) B试管中溶液的质量(填“增加”或“减小”).
-
(3) 实验结束后将两只试管中的物质倒入同一废液缸中,则废液缸中的固体一定有,废液中的溶质一定有,可能有.
欲除去不纯物质中的杂质(括号内为杂质),除去杂质所用方法不正确的是( )
选项 | 待提纯物质 | 除杂方法 |
A | O2(CO2) | 将混合气通入足量氢氧化钙溶液 |
B | CO2(CO) | 通过足量O2点燃 |
C | Cu粉(Fe粉) | 加足量稀硫酸,充分反应后过滤 |
D | N2(O2) | 通过灼热的铜网 |
A . A
B . B
C . C
D . D
为了除去物质内的杂质,需选用适当的试剂,其中正确的是( )
选项 | 物质(括号内为杂质) | 选用试剂 |
A | C(Fe) | 盐酸 |
B | CaCl2溶液(HCl) | Ba(OH)2溶液 |
C | CO2(CO) | 碱石灰(CaO和NaOH的混合物) |
D | NaOH溶液[Ca(OH)2] | K2CO3溶液 |
A . A
B . B
C . C
D . D
在已经调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入质量相等、溶质质量分数相同的稀盐酸,然后在左边烧杯中放入镁,在右边的烧杯中放人与镁质量相等的铝.待充分反应后,下列分析正确的是( )
A . 天平保持平衡,右边烧杯中,酸可能剩余,铝一定没剩余
B . 天平保持平衡,右边烧杯中,酸没有剩余,铝一定没剩余
C . 天平保持平衡,左边烧杯中,酸一定剩余,镁一定没剩余
D . 天平保持平衡,左边烧杯中,酸没有剩余,镁可能有剩余
根据要求填空:
-
(1) 用化学符号填空:
2个亚铁离子;高锰酸钾.
-
(2) 下列物质露置在空气中一段时间后,质量变大且变质的是(填序号).
①浓盐酸②浓硫酸③烧碱④食盐⑤稀硫酸
-
(3) 净化水的方法有:①过滤、②加明矾吸附沉降、③蒸馏、④消毒杀菌.要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为(填序号).
-
(4) 向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉和锌粉的混合物,充分反应后过滤,向滤液中加入足量的稀盐酸,有气泡产生,则滤渣中一定有,滤液中一定有的金属离子是(填离子符号).
近期开通的“南龙铁路”,极大方便了我市居民的出行。结合所学化学知识,回答下列问题:

-
(1) 图中标示的物质中为金属材料的是(填序号),动车电路中的导线大多选用铜制造的,这是利用了铜的延展性和性。
-
(2) 动车表面喷漆主要是为了防止外壳腐蚀,其原理是。
-
(3) 修建铁路所需的大量金属是以矿石为主要原料冶炼而得。下列矿石的主要成分属于氧化物的是________(填字母序号)。A . 铝土矿 (主要成分Al2O3) B . 辉铜矿(主要成分Cu2S) C . 菱铁矿 (主要成分FeCO3) D . 磁铁矿(主要成分Fe3O 4)
-
(4) 铁路焊接的原理为:高温下,铝与氧化铁(Fe2O 3)反应得到熔融的铁与一种氧化物。该反应的化学方程式为,基本反应类型为反应。
A-K为初中化学中的常见物质。已知G是应用最广泛的金属。它们之间的关系如图所示。
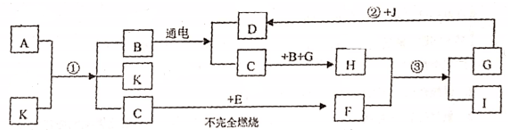
-
(1) 写出K的名称。
-
(2) 分别写出①和②反应的化学方程式:;②的基本反应类是。
-
(3) 生产、生活中为了防止C→H发生采取的措施是。
-
(4) 实验室中I的验满方法是。
下列四个图象能正确表示其变化过程的是( )
A .  表示相等质量的锌、铁与足量的稀硫酸反应
B .
表示相等质量的锌、铁与足量的稀硫酸反应
B .  表示电解水
C .
表示电解水
C .  表示用等体积、等浓度的过氧化氢溶液制取氧气
D .
表示用等体积、等浓度的过氧化氢溶液制取氧气
D .  表示加热一定量的高锰酸钾固体
表示加热一定量的高锰酸钾固体
 表示相等质量的锌、铁与足量的稀硫酸反应
B .
表示相等质量的锌、铁与足量的稀硫酸反应
B .  表示电解水
C .
表示电解水
C .  表示用等体积、等浓度的过氧化氢溶液制取氧气
D .
表示用等体积、等浓度的过氧化氢溶液制取氧气
D .  表示加热一定量的高锰酸钾固体
表示加热一定量的高锰酸钾固体
下列各方案不能证明Cu、Zn、Ag三种金属活动性的是( )
A . Zn、Ag、Cu(NO3)2溶液
B . Cu、Zn(NO3)2溶液、AgNO3溶液
C . Cu、Ag、Zn(NO3)2溶液
D . Zn、Cu、稀盐酸、AgNO3溶液
铜、铁、锌、金是比较常见的金属,与我们的生活关系密切。
-
(1) 下列金属制品的用途中,利用金属导热性的是____(填字母,可多选)。A .
 铜火锅
B .
铜火锅
B .  不锈钢炒锅
C .
不锈钢炒锅
C .  铁丝网
D .
铁丝网
D .  金牌
金牌
-
(2) 同学们在探究金属活动性的实验中,将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,为避免废液直接排放造成水污染,同时回收工业重要原料硫酸锌和有关金属。几位同学设计实验过程如下:

请回答:
①操作Ⅰ的名称是,该操作中加入的M是。
②滤液B中除水之外的物质是(填化学式)。
③该过程中涉及的基本反应类型是。
将等质量的镁、铁、锌,分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2质量与反应时间的关系如下图所示。请说出除反应速率外 , 由曲线图还能获得的信息(答三条)。

下列各组物质的鉴别方法中,不能达到预期实验目的的是( )
A . 二氧化碳和氮气——分别插入燃着的木条,观察现象
B . 硬水和软水——加入等量肥皂水、振荡,观察现象
C . 铁粉和碳粉——加入稀硫酸,观察现象
D . 稀盐酸和食盐水——加入石蕊溶液,观察现象
A~F为初中化学教材中常见的物质,它们之间有如图所示的转化关系,“→”表示物质间存在着相应的转化关系。“—”表示物质间能发生反应(部分反应物、生成物和反应条件未标出)。这些物质中只有A、B由两种元素组成,在空气中E的表面生成一层致密的氧化膜,因此E具有很好的抗腐蚀性能,F为紫红色固体。请分析后回答:

-
(1) E在空气中生成的氧化膜的化学式为。
-
(2) 写出A与B反应的化学方程式为。
最近更新
- 对性腺组织细胞进行荧光标记,等位基因A、a都被标记为黄色,等位基因B、b都被标记为绿色,在荧光显微镜下观察处于四分体时期
- 下列事例中,能说明液体传声的现象是:A、教室里书声朗朗;B、发声的鼓面在振动;C、耳朵贴在铁轨上能听见远处火车的声音;D
- 已知函数 (Ⅰ)当,求使恒成立的的取值范围; (Ⅱ)设方程的两根为,且函数H(x)在区间上的最大值比最小值大8,求的值。
- You’re in adepartment store and you see a couple of attracti
- (4分) 为了研究某种植物种子的储存条件,研究人员做了下列实验并得到相应的数据,请分析回答问题:实验操作方法储存时间(年
- 1861年俄国农奴制改革的主要进步作用是 ( ) A.造成了资本的集中 B.
- We shall ________ all schoolswith new computers in the next
- 鸟类的形态结构特征与飞行生活相适应,下列关于鸟类特征的叙述不正确的是A、飞行器官是翼 B、全身
- 选出下列各组语句中句意明确、没有语病的一句: A、像照耀每一个城市一样照耀赫尔辛基的阳光因为空气层的清净而
- 下列叙述正确的是( ) A.因为Na2CO3+SiO2Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强 B.碳和硅
- . He put it firmly that in no case _______ give in to others
- 已知函数f(x)=x2·eax,其中a<0,e为自然对数的底.(Ⅰ)讨论函数f(x)的单调性;(Ⅱ)求函数f(x)在区间
- 如图6-4-1所示是研究平抛运动规律时描绘的物体运动的轨迹,在图上已建立了以cm为单位的直角坐标系,原点O为平抛运动的出
- 写作(60分)以下两个文题任选其一 文题(一):在成长的岁月里 丈题(二):阅读下面材料,然后作文 早晨,一只
- 阅读下面的文字,完成5-7题(9分,每题3分) 太空行走 在地面上,行走是指用双腿克服地球引力,轮流迈步,从一处地面走向
- 由—C6H5、—C6H4—、—CH2—、—OH四种原子团(各1个)一起组成属于酚类物质的种类有( ) A.1种
- 函数()的最小正周期为,则满足( ) A. 在上单调递增 B. 图象关于直线对称 C. D. 当时有最
- 表1为“我国人口普查部分信息统计表”,读表完成12~13题。12. 第六次人口普查数据显示,我国人口总数已经突破(
- (8分) 下图所示为某女士的手指不小心碰到火焰后的缩手反应。请据图分析作答:(1)“手碰到火焰后立即缩回”的反应是一种神
- (08年四川卷理)已知是函数的一个极值点.(Ⅰ)求的值;(Ⅱ)求函数的单调区间;(Ⅲ)当直线与函数的图像有3个交点,求的



