到实验室去 探究金属的性质 知识点题库
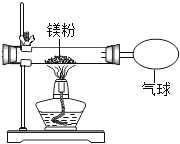
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
-
(1) (1)请写出镁条与氧气反应的化学方程式 .
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我 (“同意”或“不同意”)小明的观点,因为 .
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
-
(2) [提出问题]黄色固体是什么呢?
[查阅资料]
①氧化镁为白色固体
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
[做出猜想]黄色固体为Mg3N2
实验操作
实验现象及结论
-
(3) [反思与交流]空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,为什么?请给出合理的解释 .
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2 , 实验现象如下:
实验序号
实验1
实验2
实验3
/
镁条反应的溶液
NH4Cl
NaCl
Na2SO4
H2O
实验现象
有大量气泡产生
有较多气泡产生
有少量气泡产生
气泡极少
加热后实验现象
气泡明显增多.可闻到氨味
气泡增多
气泡增多
气泡增多
上表中,用水进行实验的目的是 .
根据上表中的实验现象,请写出三条结论,并分析可能的原因:
① ;
② ;
③ .
三种物质间只通过一步就能实现如箭头所指方向的转化,下列符合要求的组合是( )

(1)高层建筑常采用铝合金门窗,而不采用铁门窗, .
(2)富含维生素C的蔬菜烹调时不能加热时间过长,是因为维生素C .
(3)活性炭可用于除去色素或臭味,是因为活性炭具有 能力.
(4)50mL水和50mL酒精混合在一起,总体积小于100mL. .
有A,B,C三种物质,已知A是一种氯化物,B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:

-
(1) D的化学式为;
-
(2) A、B不能发生复分解反应的原因是;
-
(3) A、C反应的化学方程式为;
-
(4) 将一定质量镁、锌两种金属同时放入A溶液中充分反应,过滤、滤液为无色,则滤液中一定含有的阳离子为(写粒子符号);
-
(5) 若M、N分别为铁和锌中的一种,分别与等质量、等溶质质量分数的B溶液反应,产生氢气的质量与反应时间的关系如图乙所示,则M为,反应结束后只有一种金属有剩余,则剩余金属为.
物质的性质
A.氮气化学性质稳定 B.铜具有良好的导电性 C.浓硫酸具有吸水性 D.酒精具有可燃性 .E. 熟石灰具有碱性
物质的用途
a.保护气 b.干燥剂 c.电缆 d.改良酸性土壤 e.燃料
ABCDE
-
(1) 【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是.
【设计与实验】为了探究三种金属的活动性顺序,同学们取粗细相同的M丝、铝丝及相关溶液,进行了如图所示的实验:
观察到只有试管乙中发生明显变化,那么试管乙中观察到的现象是.
【交流与表达】同学们一致认为试管丙中也应该有明显变化,之所以出现这种情况的原因可能是.
-
(2) 于是同学们对实验进行了改进,把甲、丙中的铝丝打磨干净后又分别插入原试管中,结果甲、丙试管中都出现了明显变化,则丙试管中发生反应的化学方程式为.
-
(3) 【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序.
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:
同学们经过讨论后认为该实验可以优化,去掉试管(填试管编号)中的实验,也可以得出正确的结论.
除了上述实验外,还可以将铝丝、铜丝分别插入到盛有溶液的试管中,或将(填一种物质)分别插入到硫酸铝、硫酸铜溶液中,根据实验现象进行判断.

 向CaCl2和HCl混合溶液中加入Na2CO3溶液
B .
向CaCl2和HCl混合溶液中加入Na2CO3溶液
B .  向CuSO4和H2SO4混合溶液中加入NaOH 溶液
C .
向CuSO4和H2SO4混合溶液中加入NaOH 溶液
C .  分别向等质量的Fe和Mg中加入等浓度的稀硫酸
D .
分别向等质量的Fe和Mg中加入等浓度的稀硫酸
D .  向接近饱和的KNO3溶液中加KNO3固体
向接近饱和的KNO3溶液中加KNO3固体
-
(1) 生铁和钢都是铁的合金,其中含碳量较高的是。
-
(2) 探究Al与酸的反应前,用砂纸打磨铝条,是为了除去(填化学式)。
-
(3) 某合金中含有金属钪(Sc)。 相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快,则金属活动性ScZn(填“>”或“<”)。根据上述结论,下列说法错误的是(填序号)。
A.将Sc投入CuSO4溶液中有红色物质析出
B.仅用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag能验证钪和铁的活动性强弱
C.仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
-
(4) 已知Sc与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式。
-
(1) 人们通过食物获取各种营养素.①如图食品中富含维生素的是(填序号)。
A.米饭

B.馒头

C.西红柿

D.鸡蛋牛奶

②为了防止骨质疏松,人体每日必须摄入足够量的。
-
(2) 汽车是重要的交通工具.
①汽车电路导线大多是铜制的,这是利用金属铜的延展性和。
②在汽油中加入适量的乙醇就得到乙醇汽油,使用乙醇汽油的优点(答一点)。

请回答:
-
(1) 操作1是,固体A的成分。
-
(2) 固体C是。滤液1和滤液2中溶质相同,该溶质是。
-
(3) 写出加入过量锌粉的其中一个反应的化学方程式;加入足量稀硫酸发生反应的化学方程式。
 探究温度对分子运动快慢的影响
B .
探究温度对分子运动快慢的影响
B .  探究人呼出气体与空气中 CO2 的含量
C .
探究人呼出气体与空气中 CO2 的含量
C .  探究影响物质溶解性的因素
D .
探究影响物质溶解性的因素
D .  探究铁、银的活动性强弱
探究铁、银的活动性强弱

-
(1) 甲的化学式为;为了安全,点燃A气体之前要。
-
(2) 写出图中生成黑色固体甲的化学方程式。
-
(3) 写出蓝色溶液与E反应的化学方程式。
-
(4) 气体B还可用黑色固体与无色液体反应得到,化学方程式

-
(1) H的化学式为。B的用途是。
-
(2) C和D间发生的反应属于(填基本反应类型)反应。
-
(3) 写出A→E的化学方程式。
-
(4) 写出F→G的化学方程式。
-
(1) 人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属的位置移到最后,正好符合由弱到强的顺序。
-
(2) 汽车车体多用钢材制造。表面不仅美观,而且可有效防止生锈。
-
(3) 工业冶炼金属:
①工业上用CO还原赤铁矿冶炼金属铁的化学方程式为。工业冶铁的原料有石灰石、铁矿石、空气及焦炭,其中焦炭的作用有、;石灰石首先在高温下发生分解,其化学反应方程式为;其分解产物与铁矿石的杂质结合成炉渣。
②中国古老的冶铜方法“湿法冶铜”主要的反应原理是(写化学方程式)。
-
(4) 在实验室中探究铝、铜、银的金属活动性顺序,除铝、银外,还需要用到的试剂是。(填化学式)
-
(5) 铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图。

①使用铁锅是利用金属的,
②家庭用的燃料大多为天然气,写出天然气燃烧的化学方程式。炒菜时铁锅中的油着火可用锅盖盖灭,其原理是。
③铜也易生锈,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],是铜与空气中的共同作用的结果。

-
(1) 过程Ⅰ、Ⅲ、Ⅳ均涉及的操作是,该操作需要用到一种金属材料制成的仪器是。
-
(2) 写出过程Ⅱ中反应的化学方程式、。
-
(3) 写出过程Ⅲ中反应的化学方程式。
-
(4) 滤液4的主要成分(水除外)是。
- 函数的值域是( ) A. B. C.
- 马克思主义诞生的标志是A.《人权宣言》的发表 B.《宣言》的发表C.巴黎公社的成立
- 下图是容量为200的频率直方图,根据样本的频率分布直方图估计,样本数据落在内的频数为 ▲ .
- .Not until Dec. 2003 ___ caught by the US soldiers, and it w
- 参照事例,概括出下面两组人物姓名的特点。(4分)【示例】姓名:牛得草、马千里特点:姓与名巧妙组合出一个完整的意思,蕴含一
- President Obama held talks with Chinese President Hu Jintao
- 读下文,完成后面题。(12分) 赠黎安二生序 (宋)曾巩 ①赵郡苏轼,余之同年友也。自蜀以书至京师遗余,称蜀之士,曰黎生
- 以下关于“海上丝绸之路”的表述不正确的是( ) A.开辟于汉朝时期
- 当前我国政府立法针对性、可操作性不强;一些行政机关违法决策、随意决策的尊况仍然存 在;在行政执法活动中,乱执法、粗暴执法
- 元素周期表是学习化学的重要工具.如图是元素周期表中的一格,从中可知 ①该元素属于 (金属、非金属、或稀
- 设计试管婴儿所引发的主要问题是( ) A.不适合的胚胎的处理问题 B.将此技术用于设计婴
- 32、不同膜结构的膜之间可以相互转化。下列各项中,以囊泡的方式进行转化的是( ) A.核膜和内质网膜 B.
- 名句填空(每空1分,共7分)(1)种豆南山下, 。(陶渊明《归园田居(其三)》)(2)大漠孤烟直,
- 已知可逆反应AsO+2I-+2H+AsO+I2+H2O,设计如下图装置,进行下述操作:①向(Ⅱ)烧杯中逐滴加入浓盐酸,发
- ---Must I come for dinner before 6:00 p.m.? ---_____
- You will have to _________ these figures again, they don't a
- 除去下列物质中所含的少量杂质(括号内物质为杂质),方法正确的是( )。A.Na2O2(Na2O);加水B.Na2CO3
- 某小区最近经常发生失窃案件。某夜,居民李某深夜加班回家,他警惕地朝四周看看,然后轻声上楼回家,却被蹲守多时的小区保安怀疑
- (08年杭州市质检二) 在的二项展开式中,若只有系数最大,则n= 。
- 如图,x轴在水平地面内,y轴沿竖直方向。图中画出了从y轴上沿x轴正向抛出的三个小球a、b和c的运动轨迹,其中b和c是从同



