到实验室去 探究金属的性质 知识点题库
下列四个实验中只需要完成三个就可以证明铁、铜、银三种金属的活动性顺序。其中不必进行的是
A . 将铁片放入稀盐酸中
B . 将铜片放入稀硫酸中
C . 将铁片放入硝酸银溶液
D . 将铜片放入硝酸银溶液
下列说法中正确的是( )
A . 铝因为不和氧气反应,所以在空气中稳定存在
B . 使用明矾可以除去水中的重金属离子
C . 区分水硬度的大小,可以使用肥皂水
D . 活性炭颗粒越大吸附能力越强
下列图象分别与选项中的操作相对应,其中可能合理的是( )
A .  通电分解水
B .
通电分解水
B .  向一定量稀硫酸中加氧化铜
C .
向一定量稀硫酸中加氧化铜
C .  向一定量的硝酸银溶液中加铜
D .
向一定量的硝酸银溶液中加铜
D .  向一定量盐酸中滴加氢氧化钠溶液
向一定量盐酸中滴加氢氧化钠溶液
 通电分解水
B .
通电分解水
B .  向一定量稀硫酸中加氧化铜
C .
向一定量稀硫酸中加氧化铜
C .  向一定量的硝酸银溶液中加铜
D .
向一定量的硝酸银溶液中加铜
D .  向一定量盐酸中滴加氢氧化钠溶液
向一定量盐酸中滴加氢氧化钠溶液
如图所示的四个图象,能正确反映对应变化关系的是( )
|
|
|
|
A.镁在氧气中燃烧 | B.向二氧化锰中加入过氧化氢溶液 | C.向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 | D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应 |
A . A
B . B
C . C
D . D
质量相同的Mg和Al分别跟足量的稀盐酸反应,如果横坐标表示反应的时间,纵坐标表示生成氢气的质量,能正确表示两种金属反应情况的是如图中的( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
我们的祖先很早就掌握了用孔雀石(主要成分是Cu2(OH)2CO3和木炭一起加热进行火法炼铜的工艺,在3000多年前的商代就制造出“后母戊鼎”如图等许多精美的青铜器.有关化学反应是:
①Cu2(OH)2CO3  2CuO+H2O+CO2↑
2CuO+H2O+CO2↑
②C+2CuO  2Cu+CO2↑
2Cu+CO2↑
-
(1) 上述反应①属于反应(填“分解”“化合”“置换“复分解”之一”).
-
(2) 青铜属于(填“氧化物”“单质”“化合物”“合金”之一).
我国古人还发明了一种“湿法炼铜”的方法,流程如下:

-
(3) 写出CuSO4溶液和Fe反应的化学方程式.
-
(4) 以“绿色化学”的观点,对照火法炼铜,谈谈湿法炼铜的优点:.
随着科技的不断进步,太阳能路灯(如图所示)越来越多的出现在我们城市道路的两旁. 节约能源的同时减少了环境的污染,是实现“低碳生活”的一种典型措施.请你根据图中内容回答下列问题:

-
(1) 图中标示的物质属于金属材料的有(一个即可,填序号,下同);属于有机合成材料的是.
-
(2) 不锈钢属于(填“纯净物”或“混合物”).
-
(3) 请用一个化学方程式证明铝比铜活泼,写出实验方案.
如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A. | 铁粉 | 铜粉 | 加入过量稀盐酸,过滤 |
B. | 二氧化碳 | 一氧化碳 | 通入氧气,点燃 |
C. | 硝酸铜溶液 | 硝酸银 | 加入过量的铜粉,过滤 |
D. | 二氧化锰 | 氯化钾 | 加入水,过滤,蒸发 |
A . A
B . B
C . C
D . D
下列图形能正确反映实验事实的是( )

A . 向接近饱和的KNO3溶液中加入KNO3固体
B . 足量的Zn、Fe分别与等质量等质量分数的稀硫酸反应
C . 常温下向pH=10的氢氧化钠溶液中加水稀释
D . 向硫酸铜和硫酸混合液中滴入氢氧化钠溶液
下列除杂所选试剂合理的是( )
选项 | 物质 | 杂质 | 选用试剂 |
A | Fe | Zn | 稀盐酸 |
B | CO2 | H2O | 氢氧化钠溶液 |
C | Cu | CuO | 稀硫酸 |
D | Na2SO4溶液 | Na2CO3 | 氯化钡溶液 |
A . A
B . B
C . C
D . D
某学生在探究活动中,把一根铁钉放入烧杯中并注入一定量的硫酸铜溶液,一段时间后能观察到的现象有: ①生铁表面,②溶液逐渐由色变为色。
请写出该反应的化学方程式 ;
该反应的基本类型为反应
请写出该反应的化学方程式 ;
该反应的基本类型为反应
为探究Zn和Cu的金属活动性强弱,提供的试剂有:Zn、Cu、H2SO4溶液、ZnSO4溶液、CuSO4溶液。下列说法正确的是:( )
A . 根据Zn和Cu的硬度能判断它们的金属活动性强弱
B . ZnSO4溶液中加入Cu不能探究Zn和Cu的金属活动性强弱
C . 最多只能设计一种实验方案
D . 选用两种试剂就可实现实验目的
推理是化学学习中常用的思维方法。下列推理正确的是( )
A . 蔗糖的饱和溶液,不能再溶解蔗糖,也一定不能再溶解其他物质
B . 铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用
C . 碱溶液能使石蕊试液变蓝,则能使石蕊试液变蓝的溶液一定是碱
D . 酸和碱能发生中和反应,则硝酸与氢氧化钠也能发生中和反应
为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验。
(实验一)将三种金属丝分别与一节干电池和小电珠连接,小电珠发光。
(实验二)取粗细、长短相同的锌丝、铜丝、铬丝均与50mL稀硫酸反应,实验记录如下:
|
锌 |
铜 |
铬 |
铜 |
|
|
稀硫酸的质量分数 |
5% |
5% |
15% |
15% |
|
反应现象 |
少量气泡 |
无现象 |
许多气泡 |
无现象 |
(实验三)金属锌、铜和稀硫酸构成如图所示的化学电池装置,观察到铜片表面有气泡(H2),小电珠发光。

-
(1) 实验一的现象说明三种金属都具有性;
-
(2) 铬与稀硫酸反应生成硫酸亚铬(CrSO4)和氢气,反应的化学方程式是;该反应属于(填基本反应类型)反应;
-
(3) 要判断三种金属活动性强弱,必须在实验二的基础上增补一个实验才能得出结论,其实验内容是把粗细、长短相同的放入的50mL稀硫酸中,观察放出气泡的快慢;
-
(4) 金属活动性强弱是由金属物质的结构决定的,不会因某个实验而改变。下列关于实验三分析正确的是______(填序号)。A . 铜的金属活动性变得比锌强 B . 铜与稀盐酸发生了置换反应 C . 该装置将化学能转化为电能
回答下列与金属有关的问题。
-
(1) 金属铝耐腐蚀性较强的原因是;
-
(2) 已知
 ,则
,则 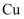 、
、  、
、  三种金属的金属活动性由强到弱的顺序为:;
三种金属的金属活动性由强到弱的顺序为:;
-
(3) 向
 和
和 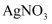 的混合溶液中加入一定量的
的混合溶液中加入一定量的  粉,充分反应后过滤,得到无色滤液和金属滤渣,此时所得金属滤渣的成分为。
粉,充分反应后过滤,得到无色滤液和金属滤渣,此时所得金属滤渣的成分为。
下列有关资源、能源的叙述正确的是( )
A . 铜是人类最早使用的金属,铬是硬度最大的金属
B . 地球上的淡水资源约占全球水储量的30.4%
C . 人们经常利用的能源有化石能源、水能和风能等
D . 空气是宝贵的自然资源,其中稀有气体约占总体积的0.03%
废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如下实验。
已知:Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。

-
(1) 将电路板粉碎成粉末的目的是。
-
(2) 滤液 A 中的溶质除硫酸外,还有。
-
(3) 步骤Ⅱ中的实验现象是:固体部分溶解,。
-
(4) 上述步骤(选填步骤编号)所包含的反应体现铁的活动性比铜强。
-
(5) 步骤 IV 中反应的化学方程式是;判断步骤Ⅳ中加入的稀硫酸过量的方法是。
A~J都是初中化学中的常见物质,其中D、E对维持自然界生命活动至关重要,A、B为黑色固体,C、G都是金属单质,I为无色气体,它们的相互转化关系如图所示:

请回答:
-
(1) 写出下列物质的化学式: A;B;
-
(2) 反应①中的现象为;
-
(3) 写出反应②的化学方程式;
-
(4) 写出反应⑤的化学方程式。
X、Y、Z三种金属,分别把X、Y放入稀硫酸中,只有X表面有气泡产生;分别把Y和Z放入硝酸银溶液中,只有Y表面有银析出。综上所述X、Y、Z的金属活动性由强到弱的顺序是( )
A . X>Y>Z
B . X>Z>Y
C . Y>X>Z
D . Y>Z>X
生锈的铁钉放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图,下列说法正确的是( )

A . CD 段压强变化的主要因素是反应速度减慢
B . AB 段的化学反应是:Fe+2HCl=FeCl2+H2↑
C . D 点反应结束
D . E 点温度等于 A 点
最近更新
- 如图所示,物体在恒力F作用下沿曲线从A运动到B,这时突然使它所受力反向、大小不变,即由F变为-F,在此力作用下,关于物体
- 杨莉是一名在你校学习的游泳运动员。请你根据对她的采访,为某报社写一篇100词左右的稿件。采访记录如下:问题 回答 希望
- 如图所示是安置在公路收费站栏杆的示意图,当在A处施加一个力时,可将栏杆逆时针拉起来,它是一根 (
- 在进行异体器官移植时,器官在被剥离后必须马上放入一种“特殊液体”中,对这种“特殊液体”的成分及其作用的分析,正确的是
- 在下列各项中,合作水平最高的区域性经济组织是() A.欧洲联盟 B.北美自由贸易区 C.石油输出组织 D.亚太经合组织
- 汉武帝“独尊儒术”,主要是利用了儒家的 A.“己所不欲,勿施于人”的主张 B.“民贵君轻”的思想 C.实践
- 已知函数y=2sinx的定义域为[a,b],值域为[-2,1],则b-a的值不可能是 ( ) A.
- 南北两半球分别有一个物体自西向东运动,下列有关其偏向的叙述正确的是 A.都向纬度较高的方向偏转 B.都向纬度较低的方
- 将阴生植物移至强光下,植物迅速发生萎蔫,此时比较图中①、②、③三个部位的细胞液浓度,正确的是()A.③>②>
- 阿斯匹林的结构简式为:把阿斯匹林放在足量的NaOH溶液中煮沸,能发生反应的化学键是 A.①④ B.①③C.②③
- 对于任何一种金属,必须满足下列哪种条件,才能发生光电效应A.入射光的强度大于某一极限强度 B.入射光的波长
- 一等腰三角形的两边长分别为4cm和6cm,则其底角的余弦值为 。
- 2010年4月17日,针对房地产市场过热发展,房价虚高,国务院办公厅发出《关于促进房地产市场平稳健康发展的通知》,以坚决
- 对于函数y=,下列说法错误的是() A.它的图象分布在一、三象限 B.它的图象与直线y=﹣x无交点 C.当x<0时,y的
- 某小组开展“探究生长素类似物促进插条生根的最适浓度”课题研究,在制定实验方案过程中,下列哪一项可以不考虑
- 小明同学在做“观察水的沸腾”实验中所用的实验装置如图11甲所示。(1)他所用的实验装置中的错误是
- 由乙烯推测丙烯的结构或性质正确的是( ) A.分子中所有原子在同一平面 B.与氯化氢加成只生成一种产物
- (07天津卷)1970年的一个冬日,联邦德国总理勃兰特在华沙被纳粹杀害的波兰人纪念碑前神色凝重地跪下了。这一举动的内涵表
- 下列对有关实验的描述中,错误的是
- 某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在a g HmX中所含质子的物质的量是 (







