初中 化学
-
(1) 乳酸的相对分子质量;
-
(2) 乳酸中各元素的质量比;
-
(3) 180g乳酸所含氢元素的质量是多少?

-
(1) B的化学式为,F的化学式为.
-
(2) 黑色固体甲与X反应的化学方程式为.
-
(3) 蓝色溶液与E反应的化学方程式为,它的化学反应基本类型为.

-
(1) 金属铝耐腐蚀性较强的原因是;
-
(2) 已知
 ,则
,则 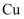 、
、  、
、  三种金属的金属活动性由强到弱的顺序为:;
三种金属的金属活动性由强到弱的顺序为:;
-
(3) 向
 和
和 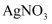 的混合溶液中加入一定量的
的混合溶液中加入一定量的  粉,充分反应后过滤,得到无色滤液和金属滤渣,此时所得金属滤渣的成分为。
粉,充分反应后过滤,得到无色滤液和金属滤渣,此时所得金属滤渣的成分为。
 B . 取用固体
B . 取用固体  C . 取用液体
C . 取用液体  D . 加热液体
D . 加热液体 
(1)双氧水分解的化学方程式是 .
(2)欲分离反应后得到的二氧化锰,用到的仪器除烧杯、玻璃棒外,还有 .
(3)实验室用此法代替氯酸钾和二氧化锰共热制取氧气,请你简述其优点:①;② .

【查阅资料】FeCl3的溶液呈黄色
甲同学认为生成的FeCl3可能与试管中的物质继续反应,进行了下列实验。
实验编号 | 实验1-1 | 实验1-2 | 实验1-3 |
实验操作 |
|
|
|
实验现象 | 长时间放置,溶液颜色始终为黄色 | 长时间放置,溶液逐渐从黄色变浅绿色 | 长时间放置,产生红褐色沉淀 |
-
(1) 用盐酸除铁锈的化学方程式为 。
-
(2) 实验1-1的目的是 。
-
(3) 综合分析实验1,溶液从黄色变浅绿色的可能原因是 。
乙同学用生锈程度相同的锈铁钉、5mL盐酸探究溶液颜色变化的影响因素。
实验编号
所用试剂
实验现象
反应开始时
24h后
2-1
铁锈和2%盐酸
铁锈、溶液均无明显变化
铁锈消失,溶液变黄色
2-2
生锈铁钉和2%盐酸
生锈铁钉、溶液均无明显变化
铁锈消失,溶液变浅绿色
2-3
生锈铁钉和6%盐酸
铁钉表面有少量气泡,铁锈逐渐消失,溶液逐渐由无色变浅黄色
溶液变为浅绿色
2-4
生锈铁钉和10%盐酸
铁钉表面产生大量气泡,铁锈逐渐消失,溶液很快由无色变黄色
溶液变为浅绿色
-
(4) 生锈铁钉与盐酸反应时,溶液的颜色变化与 有关。
-
(5) 2-2中始终未观察到溶液变黄色,结合实验1和实验2推测可能的原因为 。
-
(6) 基于上述实验推测,下列关于工业用盐酸除铁锈的说法合理的是 (填字母 序号)。
A 除铁锈时,所用盐酸的浓度越大越好
B 在除锈过程中,生成的FeCl3对铁也有腐蚀作用
C 用盐酸除锈时,应注意控制反应的时间
-
(1) 采用操作可除去污水中的碎菜叶、碎塑料薄膜、泥沙等。
-
(2) 用(填物质名称),可以除去污水中的臭味。
-
(3) 把生活污水回收处理,进行再利用的目的是。
-
(1) 人体中化学元素含量的多少直接影响人体的健康,缺少(填元素符号)元素有可能导致骨质疏松、畸形,易得佝偻病。
-
(2) 用洗洁精洗去餐具上的油污,这是利用了洗洁精的作用。
-
(3) 葡萄糖(化学式为C6H12O6)是一种重要的营养物质。葡萄糖由种元素组成,一个葡萄糖分子中有个原子,其中氢、氧元素质量比为。
-
(4) 目前,人类使用的燃科大多来自化石燃料。燃烧含硫化石燃料会产生二氧化硫,请写出硫在空气中燃烧的化学方程式:。大量二氧化硫释放到空气中会导致雨水的pH(填“大于”或“小于”)5.6,形成酸雨。

-
(1) 镁元素的相对原子质量为。
-
(2) B图中X = ,B微粒的符号是。
-
(3) 下图是镁在点燃条件下与某物质发生化学反应的微观示意图。

该反应的化学方程式为:。
①取样,加足量的水,充分搅拌后过滤,得到白色沉淀 A 和无色溶液 B.
②在白色沉淀 A 中加入足量的稀硝酸,沉淀部分溶解,并放出能使石灰水变浑浊的无色气体.
③在无色溶液 B 中加入足量的 Ba(OH)2溶液,又得到白色沉淀;再加入足量的稀硝酸,仅观察到沉淀部 分溶解的现象.
请回答:
-
(1) 原白色固体由组成.
-
(2) 实验③中沉淀溶解的化学方程式为:.
-
(1) 利用有关碳的知识完成下列填空。
①石墨因具有性可作干电池的正极。
②利用活性炭的性可进行食品添加剂的脱色;
③日常生活中人们常把煤做成蜂窝状的目的是。
-
(2) 香蕉、苹果、黄瓜等水果中,富含的主要营养素是。
-
(3) 下列疾病中,与缺少钙元素有关的是(填字母序号)。
A 骨质疏松 B 坏血病 C 佝偻病 D 贫血 F 大脖子病
-
(4) 洪涝地区的灾民将河水转化为可饮用水,以下处理顺序合理的是。
①化学沉降(用明矾)②消毒杀菌③自然沉降④加热煮沸
A ③②①④ B ③①②④ C ③①④② D ①③④②

给试管里的液体加热,液体体积一般不超过试管容积的____________;加热试管时要使用试管夹的____________,手握试管夹的,不要把拇指按在____________,而且应该从试管的____________往上套,固定在离试管口的____________处;加热时,试管倾斜跟桌面成____________,先使试管均匀受热,然后给试管里的液体的部位加热,并且不时地上下____________试管;为了避免伤人,加热时切记不可使试管口对着____________。
下列说法正确的是( )
A.电解水产生氢气和氧气,说明水是由氢分子和氧分子构成的
B.电解水中,正负极的气体质量比为1:2
C.电解水,说明原子是化学变化中最小微粒
D.电解水中,正负极产生的气体体积比为2:1
纯净物由_____________物质组成,混合_____________物由物质组成。
随着人们生活水平的提高,汽车已经走进了千家万户,成为许多家庭的代步工具.也许你的家庭就拥有一台不错得轿车,那就请根据你对汽车的了解及所学的化学知识回答下列问题:
(1)新能源电动汽车采用的电池为高铁蓄电池,其在行驶过程中能量转化是
(2)车体多用钢材制造,钢材生锈是铁与空气中的氧气、水蒸气等反应的结果,可以采取 的方法来防止钢材生锈.
(3)叠氮化钠{NaN3}被广泛应用于汽车气囊.制备工业级NaN3如下:将NaNH2与N2O气体反应可生成NaN3、NaOH和溶于水呈碱性的刺激性气味气体,该反应的化学方程式是 ,反应前氮元素的化合价分别为 .


- The people who (目击)the scene were still frightened
- We must plant _____ trees so that there will be_____polluti
- 指出:“国民党在1937年和1938年内, 抗战是比较努力的,同我党的关系也比较好。”国民党“比较努力”的抗战() A.
- 右图表示不同浓度生长素对芽生长的影响。当植物表现出顶端优势时,顶芽和最靠近顶芽的侧芽所含生长素的浓度依次分别为 A.a和
- Our desks _____ wood and this kind of paper for copying ____
- Apartments in cities can be quite high. Renters are paying u
- 下列作品中,绘画风格从注重写实变为注重意境的是 ( ) A B
- 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格
- 下列实例与基因的作用无关的是( ) A.细胞分裂素延迟植物衰老 B.极端低温导致细胞膜破裂 C.过量紫外线辐射导致皮肤
- 用来表示可逆反应:2A(g)+B(g)2C(g)△H<0 的正确图象是下图中的( )
- 如图16所示,R1=400Ω,R3的变阻范围是0~20Ω,电源电压U保持12V不变。(1)当K断开、滑片P滑到B点时,电
- 两份铝屑,一份与过量HCl反应,另一份与过量NaOH溶液反应,产生的氢气体积比为1:2,则两份铝屑的质量比为(
- 下列有关人的运动系统叙述中不正确的是 A.人体运动所需的能量直接来自ATP B.人的运动系统由
- 食物和气体的共同通道是A. 口腔 B.咽 C. 喉
- 下列关于染色体变异的叙述,正确的是( ) A.染色体增加某一片段可提高基因表达水平,是有利变异 B.染色体缺失有利于隐
- — Jack, whenshall we go to visit Mr. Smith? — It
- 下面关于甲骨文的叙述正确的有 ( ) ①商朝刻写在龟甲和兽骨上的卜辞称为甲骨文 ②甲骨文是我国现存最古老的文字,是一种
- 读《五带划分图》回答. (1)写出图中字母所处的温度带名称: A B C D E. (2)写出图中数码的纬线度数及符
- 完成下面两题。 (1)你班同学为活动拟了一副对联,但发现下联有一处不符合对联的要求,请你修改。 上联:
- 以下关于人体免疫的叙述正确的是 ( ) A.浆细胞分泌的抗体能特异性识别抗原 B.泪液中的溶菌






